下表显示了元素周期表中短周期的一部分,D、E、G、Q、M、X代表6种短周期元素,请回答以下问题。
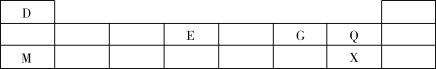
(1)E在元素周期表中的位置是第___________ 周期,第___________ 族,其原子结构示意图为___________ 。
(2)G的元素符号是___________ ,M的元素符号是___________ ,二者原子半径的关系是:G___________ M(填“>”“=”或“<”)。
(3)由M、X组成的化合物的电子式为___________ (用元素符号表示,下同),它属于___________ 化合物(填“离子”或“共价”)。
(4)用电子式表示DX的形成过程___________ ,DX中所含化学键的类型是___________ 。
(5)上述6种元素中,非金属性最强的是___________ 。

(1)E在元素周期表中的位置是第
(2)G的元素符号是
(3)由M、X组成的化合物的电子式为
(4)用电子式表示DX的形成过程
(5)上述6种元素中,非金属性最强的是
更新时间:2022-01-20 16:25:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知某粒子的核外电子排布式为 ,回答下列问题:
,回答下列问题:
(1)若该粒子为电中性粒子,则这种粒子的符号是______
(2)若该粒子形成的盐溶液能与溴水反应使溴水褪色,并出现浑浊,则这种粒子的符号是______
(3)若该粒子的还原性较弱,且这种元素的原子得到一个电子即达最外层8电子的稳定结构,则这种粒子的符号是______
 ,回答下列问题:
,回答下列问题:(1)若该粒子为电中性粒子,则这种粒子的符号是
(2)若该粒子形成的盐溶液能与溴水反应使溴水褪色,并出现浑浊,则这种粒子的符号是
(3)若该粒子的还原性较弱,且这种元素的原子得到一个电子即达最外层8电子的稳定结构,则这种粒子的符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锗(Ge)的原子结构示意图为: ,据此回答下列问题:
,据此回答下列问题:
(1)锗位于元素周期表中的第_________ 周期,第________ 族。
(2)锗的最高价氧化物化学式为___________ ,其最高价氧化物对应的水化物化学式为___________ 。
(3)根据示意图: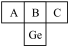 ,推得A、B、C依次为
,推得A、B、C依次为_______ 、_______ 、_______ 元素(填元素符号,下同)。A、B、C中,________ 是典型的非金属元素,________ 的最高价氧化物具有两性,常用来制农药的是________ 。
 ,据此回答下列问题:
,据此回答下列问题:(1)锗位于元素周期表中的第
(2)锗的最高价氧化物化学式为
(3)根据示意图:
 ,推得A、B、C依次为
,推得A、B、C依次为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)④、③、⑧三种元素中,离子半径由大到小的顺序为:___ (填离子符号)。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是:___ (填化学式)。
(3)⑥单质与⑨的最高价氧化物对应的水化物反应的化学方程式为:___ 。
(4)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___ 。
(5)能说明⑧的非金属性比⑨的非金属性弱的事实是:___ (用离子方程式说明)。
(6)①和③形成的18电子的化合物甲是一种应用广泛的化工原料,写出甲的结构式:___ 。实验室中可用次氯酸钠溶液与氨反应制备甲,反应的化学方程式为:___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是:
(3)⑥单质与⑨的最高价氧化物对应的水化物反应的化学方程式为:
(4)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(5)能说明⑧的非金属性比⑨的非金属性弱的事实是:
(6)①和③形成的18电子的化合物甲是一种应用广泛的化工原料,写出甲的结构式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.短周期元素X、Y、Z在元素周期表中的位置如图所示,回答下列问题。
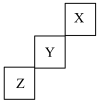
(1)元素X单质分子是________  写化学式
写化学式 。
。
(2) 在元素周期表中的第
在元素周期表中的第________ 周期第________ 族。
(3)Z的同主族下一周期的元素的原子序数是________ 。
Ⅱ.填写下列空白:
(1)写出表示含有6个质子、8个中子的原子的化学符号:________ 
(2)周期表中所含元素种数最多的纵行是第________ 纵行。
(3)周期表中铁元素的位置_____ 。
(4)周期表中原子序数为87的元素的位置_______________ 。
(5)已知A、B为同主族相邻周期的元素,原子序数 ,其中元素A位于第六周期,其原子序数为m,若为第ⅡA族,则B原子序数为
,其中元素A位于第六周期,其原子序数为m,若为第ⅡA族,则B原子序数为 __________ .
(6)由 ,D,T和
,D,T和 ,
,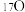 ,
, 共可以组成
共可以组成________ 种水分子。

(1)元素X单质分子是
 写化学式
写化学式 。
。 (2)
 在元素周期表中的第
在元素周期表中的第(3)Z的同主族下一周期的元素的原子序数是
Ⅱ.填写下列空白:
(1)写出表示含有6个质子、8个中子的原子的化学符号:

(2)周期表中所含元素种数最多的纵行是第
(3)周期表中铁元素的位置
(4)周期表中原子序数为87的元素的位置
(5)已知A、B为同主族相邻周期的元素,原子序数
 ,其中元素A位于第六周期,其原子序数为m,若为第ⅡA族,则B原子序数为
,其中元素A位于第六周期,其原子序数为m,若为第ⅡA族,则B原子序数为 (6)由
 ,D,T和
,D,T和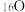 ,
,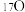 ,
, 共可以组成
共可以组成
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是元素周期表的一部分。回答下列问题:
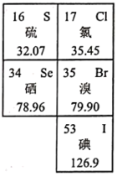
(1)溴被称为海洋元素。
①溴在元素周期表中位于第___________ 周期___________ 族。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是___________ (填化学式)。
③能够证明溴单质的氧化性强于碘单质的离子方程式是___________ 。
(2)硒是人体必需的微量元素。
①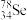 与
与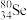 互称为
互称为___________ 。
②元素的气态氢化物的化学式为___________ 。
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:___________ 。
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是___________ (填字母)。
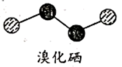
a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72

(1)溴被称为海洋元素。
①溴在元素周期表中位于第
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
③能够证明溴单质的氧化性强于碘单质的离子方程式是
(2)硒是人体必需的微量元素。
①
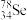 与
与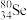 互称为
互称为②元素的气态氢化物的化学式为
③SeO2溶于水生成H2SeO3,向所得溶液中通入SO2气体发生反应,生成硒单质和H2SO4.写出SO2与H2SeO3的反应方程式:
(3)溴化硒是一种重要的电子元件材料,其分子的球棍模型如图所示。下列说法正确的是

a.溴化硒属于离子化合物 b.原子半径r:r(Se)>r(Br)
c. Se元素的非金属性比Br的强 d.溴化硒的相对分子质量为317.72
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】对于HCl、H2SO4、NaOH、NaCl、NH4Cl、Ne、N2、金刚石,回答下列问题:
(1)不存在化学键的是______ .
(2)属于共价化合物的是_________ .
(3)属于离子化合物的是____________ .
(4)既含离子键,又含共价键的是_____ .
(1)不存在化学键的是
(2)属于共价化合物的是
(3)属于离子化合物的是
(4)既含离子键,又含共价键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某“绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物如KCN,化学方程式为:KCN+H2O2+KOH→K2CO3+NH3↑。
(1)在化学方程式上标出电子转移方向和数目___ ;
(2)反应中被氧化的元素为___ ,KOH的电子式为___ ;
(3)NH3分子中N—H键为__ (填极性或非极性)共价键;
(4)H2O2属于___ (填共价或离子)化合物;
(5)写出溶液中发生该反应时,生成的化学键类型___ 。
(1)在化学方程式上标出电子转移方向和数目
(2)反应中被氧化的元素为
(3)NH3分子中N—H键为
(4)H2O2属于
(5)写出溶液中发生该反应时,生成的化学键类型
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是_____
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)极性共价键与非极性共价键的判断方法_____________________
(3)写出下列物质的电子式:CaF2:_______ CO2:_______ NH4Cl:__________
(4) 用电子式表示下列化合物的形成过程
H2S:__________________________________
MgF2:___________
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题_______________
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程
H2S:
MgF2:
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为___________ ,其电子占据的原子轨道数为 ___________ ,最高能层符号为 ___________ 。
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为___________ ,该离子更稳定的原因是 ___________ 。
(3)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是___________  填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是___________ ,属于共价化合物的是___________ 。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为
(3)基态S原子电子占据最高能级的电子云轮廓图为
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
 填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化碳CO2是工业中一种重要的原料气。
(1)碳原子L层中的电子数与氧原子L层中电子数之和是____ 。
(2)CO2的电子式是____ 。
(3)CO2中C的化合价是____ ;分子中化学键的类型是____ ;成键原子间的电子对偏向于____ 。
(4)14CO2与足量NaOH溶液反应的离子方程式是____ 。
(1)碳原子L层中的电子数与氧原子L层中电子数之和是
(2)CO2的电子式是
(3)CO2中C的化合价是
(4)14CO2与足量NaOH溶液反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有下列物质:①He;②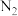 ;③
;③ ;④CaO;⑤
;④CaO;⑤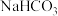 ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧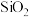 ;⑨
;⑨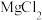 ;⑩KOH; ⑪
;⑩KOH; ⑪ ⑫
⑫ 。
。
请用序号填空:
(1)只含离子键的物质是______________ ;
(2)只含共价键的物质是______________ ;
(3)既含离子键又含共价键的物质是______________ ;
(4)只含极性键的物质是______________ ;
(5)既含离子键又含非极性键的物质是______________ ;
(6)不存在化学键的物质是______________ ;
(7)属于离子化合物的是______________ ;
(8)属于共价化合物的是______________ 。
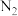 ;③
;③ ;④CaO;⑤
;④CaO;⑤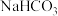 ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧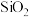 ;⑨
;⑨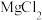 ;⑩KOH; ⑪
;⑩KOH; ⑪ ⑫
⑫ 。
。请用序号填空:
(1)只含离子键的物质是
(2)只含共价键的物质是
(3)既含离子键又含共价键的物质是
(4)只含极性键的物质是
(5)既含离子键又含非极性键的物质是
(6)不存在化学键的物质是
(7)属于离子化合物的是
(8)属于共价化合物的是
您最近一年使用:0次



