元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
更新时间:2023-01-04 11:16:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮化钠(Na3N)是一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式为______________________ ,该化合物是通过________ 键形成的。
(2)Na3N与盐酸反应生成________ 种盐,其电子式是_________________ 。
(3)Na3N与水的反应属于________ 反应。
(4)比较Na3N中两种粒子的半径大小________________________________ 。
(1)Na3N的电子式为
(2)Na3N与盐酸反应生成
(3)Na3N与水的反应属于
(4)比较Na3N中两种粒子的半径大小
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.化学工业为疫情防控提供了强有力的物质支撑。N元素的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。一氯胺(NH2Cl)在中性或酸性环境中会发生强烈水解,生成具有强烈杀菌作用的HClO,是重要的水消毒剂。
(1)写出NH2Cl的电子式:_______ 。
(2)写出NH2Cl水解的化学方程式:_____ 。
II. 含氮材料为人类提供便利的同时,人类活动和工业化进程产生的N2O、NO和NO2等氮氧化物却对空气产生了巨大污染。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2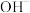 =2
=2 +H2O
+H2O
2NO2+2OH-= +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有______ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是_______ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是________ (填化学式)。
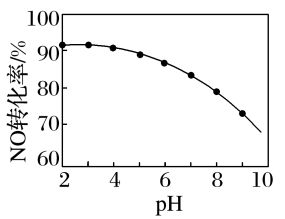
(3)NO的氧化吸收:用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成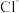 和
和 ,其离子方程式为
,其离子方程式为______ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________ 。
(1)写出NH2Cl的电子式:
(2)写出NH2Cl水解的化学方程式:
II. 含氮材料为人类提供便利的同时,人类活动和工业化进程产生的N2O、NO和NO2等氮氧化物却对空气产生了巨大污染。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2
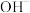 =2
=2 +H2O
+H2O2NO2+2OH-=
 +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收:用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成
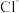 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】长征系列部分火箭采用了肼 作燃料,
作燃料, 与
与 有相似的化学性质,试回答下列问题:
有相似的化学性质,试回答下列问题:
(1)已知肼分子中所有原子最外层都满足稀有气体原子结构,则肼的结构式为_______ 。
(2)通常把拆开1mol某化学键吸收的能量看做是该化学键的键能。下表是常见的键能数据
已知合成氨反应
 则a为
则a为_______ (取整数),肼蒸汽在 中燃烧生成
中燃烧生成 与
与 时的热化学方程式为
时的热化学方程式为_______ 。
(3)火箭推进剂通常选择液态的 作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式
作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式_______ 。
(4)已知每12.8g的液态肼与足量的液态双氧水反应生成气态产物时放出热量256kJ,已知1mol液态水转化为水蒸气需要吸收44kJ的热量,则1mol的液态肼发生上述反应放出的热量为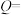
_______ 。
(5)常见的助燃剂有 、
、 、
、 等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为
等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为_______ ,实际的火箭选择的助燃剂是 ,主要考虑的因素可能是
,主要考虑的因素可能是_______ 。
 作燃料,
作燃料, 与
与 有相似的化学性质,试回答下列问题:
有相似的化学性质,试回答下列问题:(1)已知肼分子中所有原子最外层都满足稀有气体原子结构,则肼的结构式为
(2)通常把拆开1mol某化学键吸收的能量看做是该化学键的键能。下表是常见的键能数据
| 化学键 |  |  |  |  |  |  |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 | a |

 则a为
则a为 中燃烧生成
中燃烧生成 与
与 时的热化学方程式为
时的热化学方程式为(3)火箭推进剂通常选择液态的
 作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式
作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式(4)已知每12.8g的液态肼与足量的液态双氧水反应生成气态产物时放出热量256kJ,已知1mol液态水转化为水蒸气需要吸收44kJ的热量,则1mol的液态肼发生上述反应放出的热量为
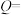
(5)常见的助燃剂有
 、
、 、
、 等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为
等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为 ,主要考虑的因素可能是
,主要考虑的因素可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】表为周期表的一部分,其中的编号代表对应的元素。
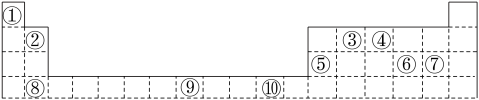
请回答下列问题:
(1)表中属于d区的元素是________ (填编号)。
(2)写出元素⑧的基态原子的电子排布式__________________________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为________ 对。
(4)元素④的氢化物的分子构型为________ ,中心原子的杂化形式为________ 。
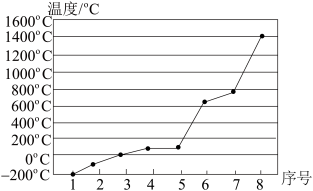
(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________ (填元素符号);其中电负性最大的是________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑧的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为

(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z是第ⅠA~ⅦA族的三种非金属元素,它们在元素周期表中的位置如图所示,试回答下列问题。
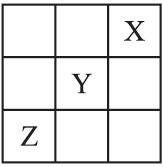
(1)X元素单质的化学式是________ 。
(2)Y元素的原子结构示意图是____________ ,Y与Na所形成化合物的电子式为________________________ 。
(3)Z元素的名称是________ ,从元素原子得失电子的角度看,Z元素具有________ 性;若从Z元素在元素周期表中所处位置看,它具有这种性质的原因是_________________________ ,其价电子排布式为__________ 。

(1)X元素单质的化学式是
(2)Y元素的原子结构示意图是
(3)Z元素的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表和元素周期律是学习化学的重要工具,可以帮助我们推测元素及其化合物的结构和性质,对工农业生产具有一定的指导意义。下表是元素周期表的部分片段(2、3周期)
(1)9种元素中,原子半径最小的是______ ,化学性质最不活泼的是____ 。
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是_______ 。
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:______ 和______ 。
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式_______________ 。
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
请你根据上表得出实验结论:_________ ;若比较⑥与⑧的单质的活泼性,请写出实验方案___________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑤ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑥ | ⑧ | ⑨ |
(1)9种元素中,原子半径最小的是
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
| 实验步骤 | 实验现象 |
| A、将一小块单质①放入滴有酚酞溶液的冷水中 | 剧烈反应,①浮于水面上,熔成小球,四处游动,发出“嘶嘶”声.随之消失,溶液变成红色 |
| B、将单质②投入冷水中,观察现象,再将水加热 | 开始无现象,加热后有气体产生 |
| C.将单质②投入稀盐酸中 | 迅速产生大量无色气体 |
| D.将单质③投入稀盐酸中 | 反应不十分剧烈,产生无色气体 |
请你根据上表得出实验结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了A-R9种元素在周期表中的位置(填元素符号)
(1)这9种元素中化学性质最不活泼的是___________ ;G的最高价氧化物的水化物化学式是___________ 。
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是___________ 。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。
(4)F元素氢化物的化学式是___________ ,该氢化物在常温下跟B发生反应的化学方程式是___________ ,所得溶液的pH___________ 7。(填“>”、“=”或“<”)
(5)H元素跟A元素形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | E | F | ||||||
3 | A | C | D | G | R | |||
4 | B | H |
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素跟A元素形成化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,请回答:
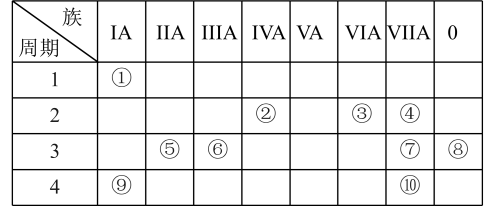
(1)元素⑦的原子结构示意图为___________ ;元素⑩的名称为___________ 。
(2)在这些元素中,化学性质最活泼的金属元素是___________ (填元素符号,下同),最不活泼的元素是___________ ;原子半径最小的元素是___________ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同);具有两性的是___________ 。

(1)元素⑦的原子结构示意图为
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中、金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)由元素②形成的单质的电子式为___________ ;元素⑤和⑧可形成化合物乙,请用电子式表示化合物乙的形成过程___________ 。
(4)元素③的最简单氢化物的化学式是___________ ,该氢化物在常温下与元素⑨发生反应的化学方程式是___________ ,所得溶液的pH___________ 7。
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
| 族周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | |||||||
(1)上述元素中、金属性最强的是
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是
(3)由元素②形成的单质的电子式为
(4)元素③的最简单氢化物的化学式是
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】土壤中的硝酸盐会被细菌分解。有一种细菌是利用土壤中的硫化物来分解硝酸盐,其主要化学反应原理是:
(1)配平上述反应方程式_________ 。
(2)K、S、N、O元素的原子半径从大到小的顺序是___________ 。
(3)写出上述反应中的共价化合物的电子式为___________ ;还原产物的结构式为___________ 。

(1)配平上述反应方程式
(2)K、S、N、O元素的原子半径从大到小的顺序是
(3)写出上述反应中的共价化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F六种元素(前20号元素)的核电荷数依次增大。C是地壳中含量最高的元素;D的最高价氧化物的水化物分别能与E、F的最高价氧化物的水化物反应;E原子的最外层电子数是其最内层电子数的3倍;F元素是化学肥料中一种重要元素,其原子的次外层电子数与倒数第三层的电子数相等;A与F具有相同的最外层电子数;B元素的某种单质常作为干电池中的电极材料。试回答下列问题:
(1)由A、B两元素按原子个数之比为1︰1组成的某分子,其相对分子质量小于30,请写出实验室制备该物质的化学反应方程式_____________________________________________ 。
(2)D、E、F三种元素的原子半径由大到小顺序是___________________ (用元素符号表示)。
(3)由C、D、E、F四种元素组成的某盐,可用作净水剂,也可用于制作膨化食品。该盐的化为_____ ,将该盐溶液与Ba(OH)2溶液按溶质物质的量之比1:2混合反应,此反应的离子方程式为_________________ 。
(1)由A、B两元素按原子个数之比为1︰1组成的某分子,其相对分子质量小于30,请写出实验室制备该物质的化学反应方程式
(2)D、E、F三种元素的原子半径由大到小顺序是
(3)由C、D、E、F四种元素组成的某盐,可用作净水剂,也可用于制作膨化食品。该盐的化为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】W、X、Y、Z是原子序数依次增大的同一周期元素,原子序数均小于18,W、X是金属元素,Y、Z是非金属元素。
(1)已知:W、X各自的氧化物对应的水化物可以反应生成盐和水,写出X的氧化物与过量氢氧化钠溶液反应的离子方程式____________________________________ 。
(2)W与Y可形成化合物W2Y,该化合物水溶液呈碱性,用离子方程式解释其原因:
____________________________________________________________________ 。
(3)Y的某氧化物通入Z单质的水溶液中,发生反应生成两种强酸的化学方程式为:
_______________________________________________________________________ 。
(4)写出Z-离子的核外电子排布式:_________________________________________ 。
(5)W、X、Y、Z四种元素简单离子的半径由小到大的顺序是
______ <______ <______ <_______ (写离子符号)。
(1)已知:W、X各自的氧化物对应的水化物可以反应生成盐和水,写出X的氧化物与过量氢氧化钠溶液反应的离子方程式
(2)W与Y可形成化合物W2Y,该化合物水溶液呈碱性,用离子方程式解释其原因:
(3)Y的某氧化物通入Z单质的水溶液中,发生反应生成两种强酸的化学方程式为:
(4)写出Z-离子的核外电子排布式:
(5)W、X、Y、Z四种元素简单离子的半径由小到大的顺序是
您最近一年使用:0次



