铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是___________(填标号)。
(2)长期放置的 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾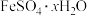 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入铁粉,其原因是
溶液变质,经常向其中加入铁粉,其原因是___________ (用离子方程式表示)。
(3)利用部分变质的 溶液制备
溶液制备 :
:
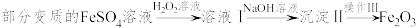
①H2O2溶液的作用是___________ 。
②写出由“溶液I”到“沉淀II”反应的离子方程式:___________ 。
③“操作III”的名称为___________ 。
(4)为测定某绿矾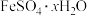 中结晶水的含量,将石英玻璃管(带两端开关
中结晶水的含量,将石英玻璃管(带两端开关 和
和 )(设为装置A)称重,记为
)(设为装置A)称重,记为 。将该绿矾
。将该绿矾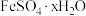 样品装入石英玻璃管中,再次将装置A称重,记为
样品装入石英玻璃管中,再次将装置A称重,记为 。按图示连接好装置进行实验。
。按图示连接好装置进行实验。
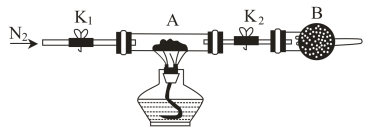
①将下列实验操作步骤正确排序:___________ (填标号);重复上述操作步骤,直至装置A恒重,记为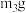 。
。
a.点燃酒精灯,加热b.熄灭酒精灯c.关闭K1和K2
d.打开K1和K2,缓缓通入N2e.称量装置Af.冷却至室温
②根据实验记录,计算绿矾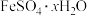 化学式中结晶水的数目x=
化学式中结晶水的数目x=_______ (列出计算式即可)。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是___________(填标号)。
A. | B. | C. | D. |
 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾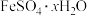 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入铁粉,其原因是
溶液变质,经常向其中加入铁粉,其原因是(3)利用部分变质的
 溶液制备
溶液制备 :
: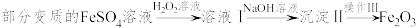
①H2O2溶液的作用是
②写出由“溶液I”到“沉淀II”反应的离子方程式:
③“操作III”的名称为
(4)为测定某绿矾
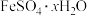 中结晶水的含量,将石英玻璃管(带两端开关
中结晶水的含量,将石英玻璃管(带两端开关 和
和 )(设为装置A)称重,记为
)(设为装置A)称重,记为 。将该绿矾
。将该绿矾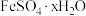 样品装入石英玻璃管中,再次将装置A称重,记为
样品装入石英玻璃管中,再次将装置A称重,记为 。按图示连接好装置进行实验。
。按图示连接好装置进行实验。
①将下列实验操作步骤正确排序:
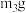 。
。a.点燃酒精灯,加热b.熄灭酒精灯c.关闭K1和K2
d.打开K1和K2,缓缓通入N2e.称量装置Af.冷却至室温
②根据实验记录,计算绿矾
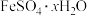 化学式中结晶水的数目x=
化学式中结晶水的数目x=
更新时间:2022-01-21 09:56:01
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】某同学在实验室研究Fe与H2SO4的反应
【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为__ .
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,
这一现象被称为__ .
(3)实验Ⅲ,已知:浓H2SO4的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体. A中产生的气体是__ ,装置C的作用是__ .
(4)实验Ⅲ结束后,
甲同学认为装置C中产生Na2SO3,
乙同学认为SO2过量,产物中还可能含有_________ ,
丙同学认为可能还含有Na2SO4,设计简单实验验证是否含有SO42-,正确的是( )
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的S元素,稀硫酸的氧化性源于________ .
②影响反应产物多样性的因素有_____________________ (至少填两个).

【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,
这一现象被称为
(3)实验Ⅲ,已知:浓H2SO4的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体. A中产生的气体是
(4)实验Ⅲ结束后,
甲同学认为装置C中产生Na2SO3,
乙同学认为SO2过量,产物中还可能含有
丙同学认为可能还含有Na2SO4,设计简单实验验证是否含有SO42-,正确的是
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的S元素,稀硫酸的氧化性源于
②影响反应产物多样性的因素有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知:常温常压下,D、E、F、I、J为气体; 1molE与含1molF的水溶液恰好反应生成B。B是一种常见的化肥。物质A—K之间有如下图所示转化关系(部分反应中生成的水已略去)。

试回答下列问题:(1)已知A中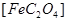 和C中Fe元素均为+2价,则
和C中Fe元素均为+2价,则 中碳元素的化合价为
中碳元素的化合价为______ 。
(2)B的化学式为________________________ 。
(3)写出反应③的化学方程式______________________________ 。
(4)写出过量单质H与K的稀溶液反应的离子方程式:__________________ 。

试回答下列问题:(1)已知A中
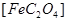 和C中Fe元素均为+2价,则
和C中Fe元素均为+2价,则 中碳元素的化合价为
中碳元素的化合价为(2)B的化学式为
(3)写出反应③的化学方程式
(4)写出过量单质H与K的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铬合金有重要的用途,从其废料中制取铬的流程如下:

已知: ① Cr+H2SO4=CrSO4+H2↑,
② 流程中铬元素浸出之后至生成Cr(OH)3之间均以自由移动离子状态存在于溶液中。
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有:________________________ (写一条即可) 。
(2)用纯碱调节滤液pH,得到某弱碱沉淀,若纯碱过量,则可能导致的后果是_:_____________ 。
(3)流程中的“副产物”中,可用作可溶性钡盐中毒解毒剂的物质的化学式是___________ ;可用作化肥的物质的化学式是_____________ 。
(4)加入草酸实现沉淀转化反应化学方程式为:_______________________________________ 。
(5)流程中利用铝热反应冶炼铬的化学方程式为:_____________________________________ 。
(6)流程中由滤液生成Cr(OH)3的化学方程式为:_____________________________________ 。
(7)除已知反应①之外,整个流程中涉及的主要氧化还原反应有_____ 个,分解反应有____ 个。

已知: ① Cr+H2SO4=CrSO4+H2↑,
② 流程中铬元素浸出之后至生成Cr(OH)3之间均以自由移动离子状态存在于溶液中。
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有:
(2)用纯碱调节滤液pH,得到某弱碱沉淀,若纯碱过量,则可能导致的后果是_:
(3)流程中的“副产物”中,可用作可溶性钡盐中毒解毒剂的物质的化学式是
(4)加入草酸实现沉淀转化反应化学方程式为:
(5)流程中利用铝热反应冶炼铬的化学方程式为:
(6)流程中由滤液生成Cr(OH)3的化学方程式为:
(7)除已知反应①之外,整个流程中涉及的主要氧化还原反应有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】结晶水合物X由六种元素组成,某学习小组按如下流程进行实验:
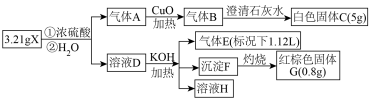
已知:
①第一步反应中元素价态没有发生变化;
②气体E能使湿润的红色石蕊试纸变蓝色;
③溶液D中含有三种正盐,其中一种即为溶液H中的唯一溶质,另一种盐M在高温灼烧时可得到相同物质的量的三种产物:红棕色G和两种组成元素相同的氧化物。
(1)X的组成中,非金属元素有___________ ,X的化学式___________ 。
(2)盐M高温分解生成三种氧化物的化学方程式___________ 。
(3)沉淀F和次氯酸钠、浓氢氧化钠反应可以制备一种能净水的钠盐,请写出该反应的离子方程式___________ 。
(4)溶液D在空气中敞口放置一段时间后,请设计实验检验溶液D中可能存在的金属阳离子:___________ 。

已知:
①第一步反应中元素价态没有发生变化;
②气体E能使湿润的红色石蕊试纸变蓝色;
③溶液D中含有三种正盐,其中一种即为溶液H中的唯一溶质,另一种盐M在高温灼烧时可得到相同物质的量的三种产物:红棕色G和两种组成元素相同的氧化物。
(1)X的组成中,非金属元素有
(2)盐M高温分解生成三种氧化物的化学方程式
(3)沉淀F和次氯酸钠、浓氢氧化钠反应可以制备一种能净水的钠盐,请写出该反应的离子方程式
(4)溶液D在空气中敞口放置一段时间后,请设计实验检验溶液D中可能存在的金属阳离子:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】五羧基全铁[Fe(CO)5]是一种浅黄色液体,熔点-20.5℃,沸点103℃,易溶于苯等有机溶剂,不溶于水,密度1.46—1.52g/cm3,有毒,光照时生成Fe2(CO)9,60℃发生自燃,可用着汽油抗爆剂,催化剂等。五羰基合铁的制备原理如下:
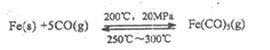
(1)五碳基合铁中铁的化合价为______________ 。
(2)下列说法正确的是_______________ 。
A.利用上述反应原理可制备高纯铁
B.制备Fe(CO)5应在隔绝空气的条件下进行
C.反应Fe(s)+5CO(g)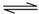 Fe(CO)5(g)的平衡常数表达式为
Fe(CO)5(g)的平衡常数表达式为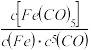
D.Fe(CO)5应密封、阴凉、避光并加少量蒸馏水液封贮存。
(3)五碳基合铁能与氢氧化钠溶液反应生成Na2Fe(CO)4和另两种常见无机物,该反应的化学方程式为________________ 。
(4)今将一定量的Fe(CO)5的苯溶液,用紫外线照射片颏。取照射后的溶液11.72g完全燃烧,得到30.536gCO2、5.4gH2O及1.6g红棕色粉末。
①红棕色粉末的化学式为____________ 。
②照射后的溶液中Fe(CO)5与Fe2(CO)9的物质的量之比为__________ 。
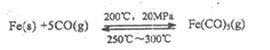
(1)五碳基合铁中铁的化合价为
(2)下列说法正确的是
A.利用上述反应原理可制备高纯铁
B.制备Fe(CO)5应在隔绝空气的条件下进行
C.反应Fe(s)+5CO(g)
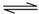 Fe(CO)5(g)的平衡常数表达式为
Fe(CO)5(g)的平衡常数表达式为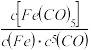
D.Fe(CO)5应密封、阴凉、避光并加少量蒸馏水液封贮存。
(3)五碳基合铁能与氢氧化钠溶液反应生成Na2Fe(CO)4和另两种常见无机物,该反应的化学方程式为
(4)今将一定量的Fe(CO)5的苯溶液,用紫外线照射片颏。取照射后的溶液11.72g完全燃烧,得到30.536gCO2、5.4gH2O及1.6g红棕色粉末。
①红棕色粉末的化学式为
②照射后的溶液中Fe(CO)5与Fe2(CO)9的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】粉煤灰是从煤燃烧后的烟气中收捕下来的细灰,主要成分有 、
、 、FeO和
、FeO和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米 等重要物质。
等重要物质。
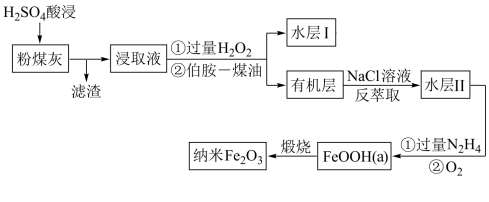
已知:
①伯胺 能与
能与 反应:
反应: ,生成易溶于煤油的产物。
,生成易溶于煤油的产物。
② 在水溶液中能与
在水溶液中能与 反应:
反应: 。
。
(1)“酸浸”过程中FeO发生反应的离子方程式为_______ ;滤渣的成分为_______ 。
(2)加入过量 的作用是
的作用是_______ 。
(3)伯胺-煤油可对浸取液进行分离,该操作的名称是_______ 。
(4)向水层Ⅱ中加入 可使
可使 转化为
转化为 并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为
并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为_______ ;向所得弱酸性溶液中再通入 即可生成FeOOH,其离子方程式为
即可生成FeOOH,其离子方程式为_______ 。
 、
、 、FeO和
、FeO和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米 等重要物质。
等重要物质。
已知:
①伯胺
 能与
能与 反应:
反应: ,生成易溶于煤油的产物。
,生成易溶于煤油的产物。②
 在水溶液中能与
在水溶液中能与 反应:
反应: 。
。(1)“酸浸”过程中FeO发生反应的离子方程式为
(2)加入过量
 的作用是
的作用是(3)伯胺-煤油可对浸取液进行分离,该操作的名称是
(4)向水层Ⅱ中加入
 可使
可使 转化为
转化为 并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为
并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为 即可生成FeOOH,其离子方程式为
即可生成FeOOH,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】合理利用工厂烟灰,变废为宝,对保护环境具有重要意义。以某工厂烟灰(主要成分为MgO、 、CuO、NiO、
、CuO、NiO、 等)为原料制备镁铝复合氧化物(
等)为原料制备镁铝复合氧化物(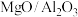 )为载体的负载型铜镍催化剂(
)为载体的负载型铜镍催化剂(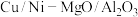 )的工艺流程如下:
)的工艺流程如下:

已知:25℃下,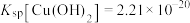 ,
,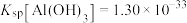 。
。
回答下列问题:
(1)为加快浸取速率,可采取的措施是_______ (写出一条即可)。
(2)“滤渣”是_______ 。
(3)加热时尿素 在水中发生水解反应,放出
在水中发生水解反应,放出 和
和_______ 气体(写化学式)。
(4)25℃下,若“悬浊液”中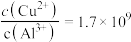 ,则溶液的
,则溶液的
_______ 。
(5)“晶化”过程中,需保持恒温70℃,采用的加热方式为_______ 。
(6)“洗涤干燥”之后的工序为_______ 。
 、CuO、NiO、
、CuO、NiO、 等)为原料制备镁铝复合氧化物(
等)为原料制备镁铝复合氧化物(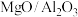 )为载体的负载型铜镍催化剂(
)为载体的负载型铜镍催化剂(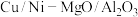 )的工艺流程如下:
)的工艺流程如下:
已知:25℃下,
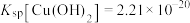 ,
,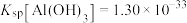 。
。回答下列问题:
(1)为加快浸取速率,可采取的措施是
(2)“滤渣”是
(3)加热时尿素
 在水中发生水解反应,放出
在水中发生水解反应,放出 和
和(4)25℃下,若“悬浊液”中
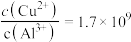 ,则溶液的
,则溶液的
(5)“晶化”过程中,需保持恒温70℃,采用的加热方式为
(6)“洗涤干燥”之后的工序为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·H2O),过程如下:

请回答下列问题:
(1)写出过程①中FeS和O2、H2SO4反应的化学方程式:____________________ 。
(2)将过程②中产生的气体通入下列溶液中,溶液会腿色的是____________________ 。
(3)过程③中,需要加入的物质是____________________ (化学式)。
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有____________________ 。
(5)过程⑥中,将溶液Z加热到70~80℃,目的是____________________ 。

请回答下列问题:
(1)写出过程①中FeS和O2、H2SO4反应的化学方程式:
(2)将过程②中产生的气体通入下列溶液中,溶液会腿色的是
| A.品红溶液 | B.紫色石蕊试液 | C.酸性高锰酸钾溶液 | D.溴水 |
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有
(5)过程⑥中,将溶液Z加热到70~80℃,目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】某兴趣小组研究FeSO4溶液与NaOH溶液反应过程中物质的变化。
(1)小组实验
如图,向2mL0.1mol/L新制FeSO4溶液中滴加少量0.1mol/LNaOH溶液,生成白色沉淀,迅速变成灰绿色,最终变为红褐色。写出沉淀由白色变成红褐色的化学方程式________ 。
(2)探究灰绿色沉淀的成因
猜想1:白色沉淀吸附Fe2+,呈现灰绿色。
猜想2:铁元素部分被氧化后,Fe(Ⅱ)、Fe(Ⅲ)形成的共沉淀为灰绿色。
①将试剂i补充完整_________ 。
②根据实验现象得出结论,猜想_______ 正确。
(3)探究灰绿色沉淀的结构和组成
资料:i.Fe(OH)2层状结构示意图如图,OH-位于八面体的顶点,Fe2+占据八面体中心。当部分Fe(Ⅱ)被氧化为Fe(Ⅲ)时,层状结构不被破坏。

ii.Fe2+在强酸性条件下不易被空气氧化;低浓度Cl-难以体现还原性。
iii.I2+2 =2I-+
=2I-+ 。
。
称取一定量灰绿色沉淀,用稀盐酸完全溶解后,定容至250mL得样品液。
①小组同学根据资料推测:灰绿色沉淀的层间可能嵌入了 ,理由是
,理由是___________ 。通过实验证实了该推测正确,实验操作和现象是___________ 。
②取样品液100.00mL,测得其中 的物质的量为6.4×10-4mol。
的物质的量为6.4×10-4mol。
③取样品液25.00mL,用0.0050mol/L酸性KMnO4溶液滴定至终点,消耗KMnO4溶液25.60mL,写出该滴定过程中反应的离子方程式___________ 。
④取样品液25.00mL,加适量水及KI固体静置后,立即以0.0250mol/LNa2S2O3溶液滴定至浅黄色,在加入淀粉溶液滴定至蓝色恰好消失,消耗Na2S2O3溶液12.80mL。
结论:用Fe(Ⅱ)xFe(Ⅲ)y(OH)z(SO4)m表示灰绿色沉淀的组成,则此样品中x:y:z:m=___________ (取最简整数比)。
(1)小组实验
如图,向2mL0.1mol/L新制FeSO4溶液中滴加少量0.1mol/LNaOH溶液,生成白色沉淀,迅速变成灰绿色,最终变为红褐色。写出沉淀由白色变成红褐色的化学方程式

(2)探究灰绿色沉淀的成因
猜想1:白色沉淀吸附Fe2+,呈现灰绿色。
猜想2:铁元素部分被氧化后,Fe(Ⅱ)、Fe(Ⅲ)形成的共沉淀为灰绿色。
| 实验 | 操作 | 试剂(均为0.1mol/L) | 实验现象 |
| I |  向两片玻璃片中心分别滴加试剂i和ii,面对面快速夹紧 | i. ii.2滴NaOH溶液 | 玻璃片夹缝中有白色浑浊。分开玻璃片白色浑浊迅速变为灰绿色 |
| Ⅱ | i.2滴FeSO4溶液, 1滴Fe2(SO4)3溶液 ii.2滴NaOH溶液 | 玻璃片夹缝中立即有灰绿色浑浊 |
②根据实验现象得出结论,猜想
(3)探究灰绿色沉淀的结构和组成
资料:i.Fe(OH)2层状结构示意图如图,OH-位于八面体的顶点,Fe2+占据八面体中心。当部分Fe(Ⅱ)被氧化为Fe(Ⅲ)时,层状结构不被破坏。

ii.Fe2+在强酸性条件下不易被空气氧化;低浓度Cl-难以体现还原性。
iii.I2+2
 =2I-+
=2I-+ 。
。称取一定量灰绿色沉淀,用稀盐酸完全溶解后,定容至250mL得样品液。
①小组同学根据资料推测:灰绿色沉淀的层间可能嵌入了
 ,理由是
,理由是②取样品液100.00mL,测得其中
 的物质的量为6.4×10-4mol。
的物质的量为6.4×10-4mol。③取样品液25.00mL,用0.0050mol/L酸性KMnO4溶液滴定至终点,消耗KMnO4溶液25.60mL,写出该滴定过程中反应的离子方程式
④取样品液25.00mL,加适量水及KI固体静置后,立即以0.0250mol/LNa2S2O3溶液滴定至浅黄色,在加入淀粉溶液滴定至蓝色恰好消失,消耗Na2S2O3溶液12.80mL。
结论:用Fe(Ⅱ)xFe(Ⅲ)y(OH)z(SO4)m表示灰绿色沉淀的组成,则此样品中x:y:z:m=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组同学用下图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。
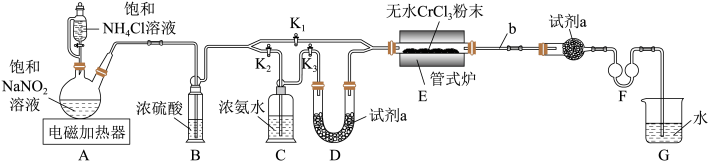
已知:实验室中常用 溶液与
溶液与 溶液反应制取N2;CrCl3能溶于水和乙醇。
溶液反应制取N2;CrCl3能溶于水和乙醇。
回答下列问题:
(1)实验准备就绪后,打开K1,关闭K2、K,此时应先加热___________ (填装置代号)装置。
(2)实验中制取N2的化学反应方程式为___________ ,在该反应中,氧化产物与还原产物的物质的量之比为___________ 。
(3)改变K1、K2、K3的状态,加热E装置。试剂a的名称是___________ ,写出装置E中发生反应的化学方程式___________ 。
(4)实验过程中需间歇性微热b处导管的目的是___________ 。
(5)向7.0g所得CrN中加入足量NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用60mL1mol·L-1H2SO4溶液完全吸收,剩余的H2SO4用10mL2mol·L-1NaOH溶液恰好中和,则所得产品中CrN的质量分数为___________ (保留三位有效数字)。

已知:实验室中常用
 溶液与
溶液与 溶液反应制取N2;CrCl3能溶于水和乙醇。
溶液反应制取N2;CrCl3能溶于水和乙醇。回答下列问题:
(1)实验准备就绪后,打开K1,关闭K2、K,此时应先加热
(2)实验中制取N2的化学反应方程式为
(3)改变K1、K2、K3的状态,加热E装置。试剂a的名称是
(4)实验过程中需间歇性微热b处导管的目的是
(5)向7.0g所得CrN中加入足量NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用60mL1mol·L-1H2SO4溶液完全吸收,剩余的H2SO4用10mL2mol·L-1NaOH溶液恰好中和,则所得产品中CrN的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。
(1)实验室在40℃、pH﹦4的条件下用Na2SO3溶液和SO2反应制取Na2S2O5:Na2SO3+SO2=Na2S2O5实验时先用CO2气体尽可能排除装置内空气的目的是_____________ 。
(2)若制备19 g Na2S2O5至少需标准状况下SO2_____________ L。
(3)为了检验某抗氧化剂产品中Na2S2O5的质量分数,某研究小组进行如下实验:
步骤I:称取抗氧化剂产品0.2 g,将其加入到含I2浓度为0.05000 mol·L−1 的100 mL稀盐酸和碘水的混合溶液中,然后加水稀释至500 mL。
步骤II:取稀释后的溶液100 mL,加入几滴淀粉溶液,用0.1000 mol·L−1 Na2S2O3标准溶液进行滴定,共消耗Na2S2O3标准溶液12.00 mL(2S2O32- + I2=2I- + S4O62-)。
①写出步骤I中Na2S2O5和I2反应的离子方程式_____________ 。
②计算抗氧化剂产品中Na2S2O5质量分数,写出计算过程_____________ 。
(1)实验室在40℃、pH﹦4的条件下用Na2SO3溶液和SO2反应制取Na2S2O5:Na2SO3+SO2=Na2S2O5实验时先用CO2气体尽可能排除装置内空气的目的是
(2)若制备19 g Na2S2O5至少需标准状况下SO2
(3)为了检验某抗氧化剂产品中Na2S2O5的质量分数,某研究小组进行如下实验:
步骤I:称取抗氧化剂产品0.2 g,将其加入到含I2浓度为0.05000 mol·L−1 的100 mL稀盐酸和碘水的混合溶液中,然后加水稀释至500 mL。
步骤II:取稀释后的溶液100 mL,加入几滴淀粉溶液,用0.1000 mol·L−1 Na2S2O3标准溶液进行滴定,共消耗Na2S2O3标准溶液12.00 mL(2S2O32- + I2=2I- + S4O62-)。
①写出步骤I中Na2S2O5和I2反应的离子方程式
②计算抗氧化剂产品中Na2S2O5质量分数,写出计算过程
您最近一年使用:0次




