某化学兴趣小组进行了实验:向2支试管中分别加入0.5 g Na2CO3固体和0.5 gNaHCO3固体,再分别加入30 mL 0.3 mol·L-1盐酸,充分反应后,用手触摸试管,明显感觉到加Na2CO3固体的试管变热了,加NaHCO3固体的试管变冷了。甲同学由此得出结论:CO (aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO
(aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO (aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?_____ (填“甲”或“乙”) ,理由是_______ 。
(2)查阅资料:
反应I :CO (aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
(aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
反应II :HCO (aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
(aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
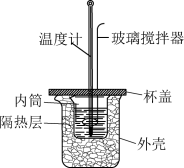
(3)该化学兴趣小组用如图所示装置设计了实验,验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。
表格一:
表格二:
表格三:
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是_______________ 。
②表格二对应实验得出的结论是________________ 。
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1______ (填“>”、“< ”或“=”,下同) △H3,△H2______ △H4。
 (aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO
(aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO (aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?
(2)查阅资料:
反应I :CO
 (aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
(aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;反应II :HCO
 (aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
(aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
A.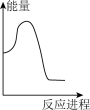 | B.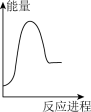 | C.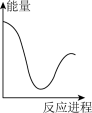 | D.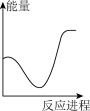 |

表格一:
试剂1 | 试剂2混合前温度/℃ | 混合后温度/℃ |
0.5 g Na2CO3 | 40mL HCl 19.0 | 21.7 |
0.5 g NaHCO3 | 40 mL HCl 19.0 | 18.1 |
表格二:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22. 3 | 19.0 | 10mL H2O 19.0 | 19.0 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL H2O 19.0 | 19.0 |
表格三:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22.3 | 19.0 | 10mL HCl 19.0 | 20.5 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL HCl19.0 | 18.3 |
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是
②表格二对应实验得出的结论是
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1
更新时间:2022-01-23 18:08:52
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】化学反应中的能量和速率变化对生产生活有着重要意义。某研究学习小组进行下列探究。
(1)甲同学探究反应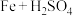 (稀)
(稀)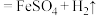 中的能量变化。向装有铁片的试管中加入
中的能量变化。向装有铁片的试管中加入 的
的 ,观察到试管内有气泡产生,触摸试管外壁,温度升高。
,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为___________ (填“放热”或“吸热”)反应。
②该反应反应物的总能量___________ (填“>”或“<”)生成物的总能量。
(2)乙同学认为原电池原理也可加快化学反应速率,他设计如图所示实验装置。铁片上的电极反应式为___________ ,溶液中 浓度
浓度___________ (填“增大”、“减小”或“不变”)。___________ (填序号)。
①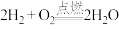 ;②
;② ;③
;③
(1)甲同学探究反应
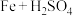 (稀)
(稀)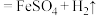 中的能量变化。向装有铁片的试管中加入
中的能量变化。向装有铁片的试管中加入 的
的 ,观察到试管内有气泡产生,触摸试管外壁,温度升高。
,观察到试管内有气泡产生,触摸试管外壁,温度升高。①该反应为
②该反应反应物的总能量
(2)乙同学认为原电池原理也可加快化学反应速率,他设计如图所示实验装置。铁片上的电极反应式为
 浓度
浓度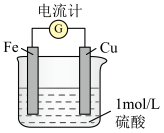
①
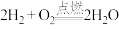 ;②
;② ;③
;③
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)下列反应属于放热反应的是___________
A.铝片与稀H2SO4反应制取H2
B.碳酸钙高温分解成氧化钙和二氧化碳
C.葡萄糖在人体内氧化分解
D.氢氧化钾和硫酸中和
E.Ba(OH)2∙8H2O与NH4Cl固体反应
(2)一定条件下,某恒容密闭容器中充入SO2与O2反应,经5min后,若SO2和SO3物质的量浓度分别为2mol/L和5mol/L,则SO2起始物质的量浓度为___________ :用SO3表示这段时间该化学反应速率为___________ ,以下操作会引起化学反应速率变快的是___________ 。
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
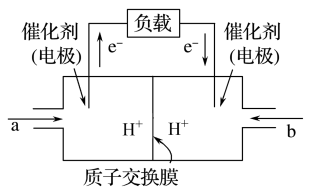
(3)如图是某笔记本电脑使用的甲醇空气燃料电池的结构示意图。放电时甲醇应从___________ 处通入(填“a”或“b”),电池内部H+向___________ (填“左”或“右”)移动,写出负极的电极反应式___________ 。
(1)下列反应属于放热反应的是
A.铝片与稀H2SO4反应制取H2
B.碳酸钙高温分解成氧化钙和二氧化碳
C.葡萄糖在人体内氧化分解
D.氢氧化钾和硫酸中和
E.Ba(OH)2∙8H2O与NH4Cl固体反应
(2)一定条件下,某恒容密闭容器中充入SO2与O2反应,经5min后,若SO2和SO3物质的量浓度分别为2mol/L和5mol/L,则SO2起始物质的量浓度为
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
(3)如图是某笔记本电脑使用的甲醇空气燃料电池的结构示意图。放电时甲醇应从

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】硫酰氯( )是工业合成的氯化剂,在生产中有广泛应用。制备原理是
)是工业合成的氯化剂,在生产中有广泛应用。制备原理是 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和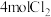 只发生上述反应。测得
只发生上述反应。测得 的物质的量变化如图所示。回答下列问题:
的物质的量变化如图所示。回答下列问题:

(1)经测定,生成物的总能量低于反应物的总能量。该反应的正反应是________ (填“吸热”或“放热”)反应。
(2)a点正反应速率________ (填“大于”“小于”或“等于”)逆反应速率。此时 的转化率为
的转化率为________ %。
(3)在上述条件下,a、b、c点中,反应达到最大限度的点是________ 。b点逆反应速率________ c点正反应速率(填“>”“=”或“<”)。
(4)从反应开始到c点时间内平均速率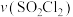 为
为________  。
。
(5)温度不变,加入催化剂, 最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
(6)c点时各组成浓度比值
________ 。
 )是工业合成的氯化剂,在生产中有广泛应用。制备原理是
)是工业合成的氯化剂,在生产中有广泛应用。制备原理是 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和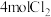 只发生上述反应。测得
只发生上述反应。测得 的物质的量变化如图所示。回答下列问题:
的物质的量变化如图所示。回答下列问题:
(1)经测定,生成物的总能量低于反应物的总能量。该反应的正反应是
(2)a点正反应速率
 的转化率为
的转化率为(3)在上述条件下,a、b、c点中,反应达到最大限度的点是
(4)从反应开始到c点时间内平均速率
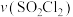 为
为 。
。(5)温度不变,加入催化剂,
 最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。
最大限度为75%。加入催化剂后,上述图像中c点移动正确的是________(填字母)。| A.水平右移 | B.水平左移 | C.向左下方移动 | D.向右上方移动 |

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为________________ 。
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为____________________ 。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ·mol-1
写出肼和N2O4反应的热化学方程式________________________________________ 。
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为________________________________________ 。
(1)氮元素原子的L层电子数为
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ·mol-1
写出肼和N2O4反应的热化学方程式
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
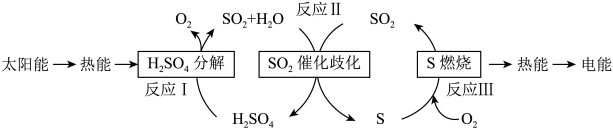
反应Ⅰ:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) △H3=-297kJ/mol
反应Ⅱ的热化学方程式为:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) △H=____ 。
(2)工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,SO2被空气中的O2氧化为SO3。V2O5是钒催化剂的活性成分,郭汗贤等提出:V2O5在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
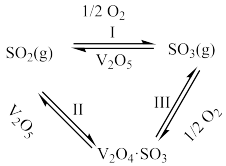
①有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
由此计算反应Ⅰ的△H=______ kJ/mol。
②反应Ⅱ、Ⅲ的化学方程式为__________ 、_____________ 。
(3)室温下,用50mL0.50mol/L盐酸50mL0.55mol/LNaOH溶液在如图所示装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。回答下列问题:
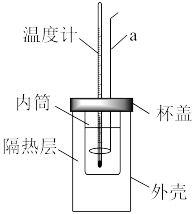
①仪器a的名称为_________ 。
②_____ (填“能”或“不能”)用相同形状的细铜丝代替仪器a进行相应的实验操作。
③上述实验测得中和热的数值小于57.3kJ/mol,产生偏差的原因可能是____ (填字母)。
A.量取NaOH溶液时仰视读数
B.为了使反应充分,向酸溶液中分次加入碱溶液
C.实验装置保温隔热效果差
D.用铜丝代替玻璃搅拌器搅拌
(1)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应Ⅰ:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) △H3=-297kJ/mol
反应Ⅱ的热化学方程式为:3SO2(g)+2H2O(g)=2H2SO4(l)+S(s) △H=
(2)工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,SO2被空气中的O2氧化为SO3。V2O5是钒催化剂的活性成分,郭汗贤等提出:V2O5在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:

①有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
| 化学键 | S=O(SO2) | O=O(O2) | S=O(SO3) |
| 能量/kJ | 535 | 496 | 472 |
②反应Ⅱ、Ⅲ的化学方程式为
(3)室温下,用50mL0.50mol/L盐酸50mL0.55mol/LNaOH溶液在如图所示装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。回答下列问题:

①仪器a的名称为
②
③上述实验测得中和热的数值小于57.3kJ/mol,产生偏差的原因可能是
A.量取NaOH溶液时仰视读数
B.为了使反应充分,向酸溶液中分次加入碱溶液
C.实验装置保温隔热效果差
D.用铜丝代替玻璃搅拌器搅拌
您最近一年使用:0次
【推荐3】雾霾、温室效应、光化学污染等环境问题引起了全世界的高度重视。科学家对大气中NO,、SO2、CO、CxHy进行综合研究与治理具有重要意义。
(1)已知:①CH4(g) +2NO2(g)=N2(g) + CO2(g) + 2H2O(g) ΔH= -867 kJ·mol-1
②2NO2(g) N2O4(g) ΔH= -56.9 kJ·mol-1
N2O4(g) ΔH= -56.9 kJ·mol-1
③H2O(g) H2O(l) ΔH = -44.0 kJ·mol-1
H2O(l) ΔH = -44.0 kJ·mol-1
写出CH4催化还原N2O4( g)生成N2(g)、CO2(g)和H2O(1)的热化学方程式_______ 。
(2)CO2与H2一定条件下可以合成C2H4反应原理为6H2(g) + 2CO2( g) CH2=CH2(g) +4H2O(g)。 一定条件下,不同温度对CO2的平衡转化率及催化剂的催化效率影响如图1所示,下列说法不正确的是
CH2=CH2(g) +4H2O(g)。 一定条件下,不同温度对CO2的平衡转化率及催化剂的催化效率影响如图1所示,下列说法不正确的是____________ (填序号)。
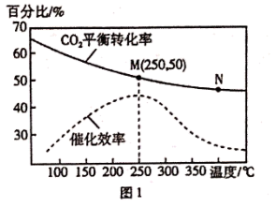
A.M点的反应速率最大
B. 温度低于250 ℃ 时,温度升高,乙烯的平衡产率增大
C. M点时平衡常数比N点时平衡常数大
D. 为提高CO2的平衡转化率,应在尽可能低的温度下进行反应
(3)化工生产中采用甲醇与CO反应来制备乙酸。在一个恒压密闭容器中加入0. 20 mol CH3OH和0. 22 mol CO混合气体,发生反应CH3OH(g) + CO(g) CH3COOH(1) ,测得甲醇的转化率随温度的变化关系如图2所示,曲线1表示在不同温度下,经过5min时测得的甲醇的转化率变化曲线,曲线I表示不同温度下甲醇的平衡转化率变化曲线,已知在T2 K温度下,达到平衡时容器的体积为2 L。
CH3COOH(1) ,测得甲醇的转化率随温度的变化关系如图2所示,曲线1表示在不同温度下,经过5min时测得的甲醇的转化率变化曲线,曲线I表示不同温度下甲醇的平衡转化率变化曲线,已知在T2 K温度下,达到平衡时容器的体积为2 L。
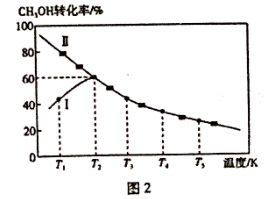
①温度为T2 K,反应达到平衡时,向该恒压密闭容器中瞬时通入0.12molCH3OH和0.06molCO混合气体,此时平衡___________ (填“向左移动”“向右移动”或“不移动”)。
②在温度为T1 K时,乙酸的物质的量随时间的变化关系如下图所示。在t1时,将该反应体系温度迅速上升到T3 K,并维持该温度。请在下图中画出t1时刻后乙酸物质的量的变化曲线_________ 。

(4)甲烷燃料电池可以提高能量利用率。如下图为利用甲烷燃料电池电解100 mL1 mol·L-1食盐水,常温下,电解一段时间后收集到标准状况下2.24 L氢气(忽略溶液体积变化)。
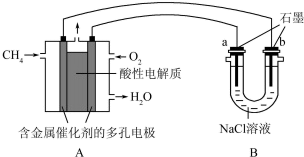
①甲烷燃料电池的负极反应式为___________ 。
②电解后溶液的pH =____________ (忽略氯气与氢氧化钠溶液的反应)
(1)已知:①CH4(g) +2NO2(g)=N2(g) + CO2(g) + 2H2O(g) ΔH= -867 kJ·mol-1
②2NO2(g)
 N2O4(g) ΔH= -56.9 kJ·mol-1
N2O4(g) ΔH= -56.9 kJ·mol-1③H2O(g)
 H2O(l) ΔH = -44.0 kJ·mol-1
H2O(l) ΔH = -44.0 kJ·mol-1写出CH4催化还原N2O4( g)生成N2(g)、CO2(g)和H2O(1)的热化学方程式
(2)CO2与H2一定条件下可以合成C2H4反应原理为6H2(g) + 2CO2( g)
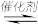 CH2=CH2(g) +4H2O(g)。 一定条件下,不同温度对CO2的平衡转化率及催化剂的催化效率影响如图1所示,下列说法不正确的是
CH2=CH2(g) +4H2O(g)。 一定条件下,不同温度对CO2的平衡转化率及催化剂的催化效率影响如图1所示,下列说法不正确的是
A.M点的反应速率最大
B. 温度低于250 ℃ 时,温度升高,乙烯的平衡产率增大
C. M点时平衡常数比N点时平衡常数大
D. 为提高CO2的平衡转化率,应在尽可能低的温度下进行反应
(3)化工生产中采用甲醇与CO反应来制备乙酸。在一个恒压密闭容器中加入0. 20 mol CH3OH和0. 22 mol CO混合气体,发生反应CH3OH(g) + CO(g)
 CH3COOH(1) ,测得甲醇的转化率随温度的变化关系如图2所示,曲线1表示在不同温度下,经过5min时测得的甲醇的转化率变化曲线,曲线I表示不同温度下甲醇的平衡转化率变化曲线,已知在T2 K温度下,达到平衡时容器的体积为2 L。
CH3COOH(1) ,测得甲醇的转化率随温度的变化关系如图2所示,曲线1表示在不同温度下,经过5min时测得的甲醇的转化率变化曲线,曲线I表示不同温度下甲醇的平衡转化率变化曲线,已知在T2 K温度下,达到平衡时容器的体积为2 L。
①温度为T2 K,反应达到平衡时,向该恒压密闭容器中瞬时通入0.12molCH3OH和0.06molCO混合气体,此时平衡
②在温度为T1 K时,乙酸的物质的量随时间的变化关系如下图所示。在t1时,将该反应体系温度迅速上升到T3 K,并维持该温度。请在下图中画出t1时刻后乙酸物质的量的变化曲线

(4)甲烷燃料电池可以提高能量利用率。如下图为利用甲烷燃料电池电解100 mL1 mol·L-1食盐水,常温下,电解一段时间后收集到标准状况下2.24 L氢气(忽略溶液体积变化)。

①甲烷燃料电池的负极反应式为
②电解后溶液的pH =
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】人们通过化学方法可以开辟新能源和提高能源的利用率,根据情景回答下列问题:
(1)工业合成氨反应 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量___________ (填“大于”“小于”或“等于”)46kJ。
(2)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol
①用 表示的化学反应速率为
表示的化学反应速率为___________ 
②一定条件下,能说明该反应进行到最大限度的是___________ 。
a. 的转化率达到最大值
的转化率达到最大值
b. 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
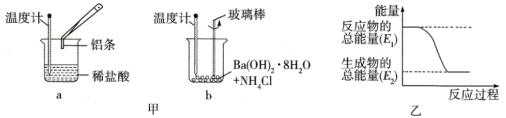
(3)某实验小组进行如图甲所示实验。请判断b中的温度___________ (填“升高”或“降低”)。反应过程___________ (填“a”或“b”)的能量变化可用图乙表示。
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:

①电极c是___________ (填“正极”或“负极”),电极d的电极反应式为___________ 。
②若线路中转移1mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(1)工业合成氨反应
 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量(2)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol

①用
 表示的化学反应速率为
表示的化学反应速率为
②一定条件下,能说明该反应进行到最大限度的是
a.
 的转化率达到最大值
的转化率达到最大值b.
 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组进行如图甲所示实验。请判断b中的温度

(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①电极c是
②若线路中转移1mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图___ ,E元素在周期表中的位置是____ 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为____ 。
(3)D与C按原子个数比为1:1形成化合物的电子式是____ 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是____ (填化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式____ 。
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl____ ΔH2(填“>”或“<”或“=”)。
(1)画出D的原子结构示意图
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为
(3)D与C按原子个数比为1:1形成化合物的电子式是
(4)B、C所形成氢化物的稳定性由强到弱的顺序是
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________ 。
(2)大烧杯上如不盖硬纸板,求得的中和热数值将_______ (填“偏大”、“偏小”或“无影响”)。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量________ (填“相等”或“不相等”),但中和热应_________ (填“相等”或“不相等”),简述理由_________________________________ 。

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)大烧杯上如不盖硬纸板,求得的中和热数值将
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量
您最近一年使用:0次



