2021年10月16日,神舟十三号载人飞船顺利进入预定轨道。飞船的轨道舱内安装盛有Na2O2颗粒的装置,为宇航员供氧。回答下列问题:

(1)Na2O2的制取。将金属钠加热至熔化,通入一定量已除去CO2的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成Na2O,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠的电子式为___________ ,过氧化钠和氧化钠中含有相同的化学键是___________ 。
(2)Na2O2的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为_______ ,该反应中的还原剂是_______ (填写化学式)。
(3)反应后组成的探究。Na2O2使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是Na2CO3或NaHCO3或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学反应方程式为___________ 。
②称取19.0g“失效供氧剂”加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰增重8.8g,该“失效供氧剂”的化学组成为___________ (只填写化学式)。

(1)Na2O2的制取。将金属钠加热至熔化,通入一定量已除去CO2的干燥空气,加热并维持温度在180~200℃之间,钠被氧化成Na2O,进而增加空气流量,迅速升温至300~400℃,制得过氧化钠。过氧化钠的电子式为
(2)Na2O2的供氧。过氧化钠能与人体呼出的酸性氧化物发生反应,其化学方程式为
(3)反应后组成的探究。Na2O2使用后会失去供氧能力(又称失效供氧剂),某“失效供氧剂”的化学组成可能是Na2CO3或NaHCO3或两者的混合物。为探究“失效供氧剂”的化学组成,化学探究小组进行如下实验:
①取适量“失效供氧剂”于试管中,加热,产生能使澄清石灰水变浑浊的气体,产生该气体的化学反应方程式为
②称取19.0g“失效供氧剂”加入足量稀硫酸,将生成的气体用浓硫酸干燥后,再用碱石灰完全吸收,碱石灰增重8.8g,该“失效供氧剂”的化学组成为
更新时间:2022-01-24 14:25:44
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)要确定一瓶药品为氯化钠,可用焰色试验确定______ 的存在,用硝酸银溶液和稀硝酸确定______ 的存在。
(2)制取氢氧化铁胶体时应向沸腾的蒸馏水中滴加几滴______ 溶液,然后用激光笔来照射生成的胶体,并从侧面观察,这个实验叫______ 。
(3)实验室保存过氧化钠时应密封保存,主要是隔绝二氧化碳和______ 。
(2)制取氢氧化铁胶体时应向沸腾的蒸馏水中滴加几滴
(3)实验室保存过氧化钠时应密封保存,主要是隔绝二氧化碳和
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】书写下列反应的离子反应方程式
(1)醋酸与碳酸钙反应:___________
(2)过氧化钠与水反应:___________
(3)硫酸与氢氧化钡反应:___________
(4)铝与氢氧化钠溶液反应:___________
(5)设计实验检验实验室粗盐中是否存在SO :
:___________
(1)醋酸与碳酸钙反应:
(2)过氧化钠与水反应:
(3)硫酸与氢氧化钡反应:
(4)铝与氢氧化钠溶液反应:
(5)设计实验检验实验室粗盐中是否存在SO
 :
:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求书写下列反应并回答有关问题。
(1)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目___________ 。
(2)写出Cu与AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目___________ 。
(3)写出Na2O2与CO2反应的化学方程式___________ ,并指明该反应的氧化剂和还原剂分别是___________ 、___________ 。
(4)写出NaHCO3固体加热分解的化学方程式___________ 。
(5)写出Na2O与盐酸反应的离子方程式___________ 。
(1)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目
(2)写出Cu与AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目
(3)写出Na2O2与CO2反应的化学方程式
(4)写出NaHCO3固体加热分解的化学方程式
(5)写出Na2O与盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)下面是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是_______ 、_______ 、_______ (填化学式)。
(2)写出Na2O2与CO2反应的方程式_______ (并用双线桥法标出电子转移情况)
(3)KHSO4在水溶液中的电离方程式可以表示为_______ ;
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是_______ ,反应的离子方程式为_______ 。
(5)向KHSO4溶液中加入锌片,反应的离子方程式为_______ 。
(1)下面是某同学对有关物质进行分类的列表:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O2 | SO3 |
| 第三组 | KOH | CH3COOH | CaF2 | Al2O3 | SO2 |
(2)写出Na2O2与CO2反应的方程式
(3)KHSO4在水溶液中的电离方程式可以表示为
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是
(5)向KHSO4溶液中加入锌片,反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为 ,钠在反应中容易
,钠在反应中容易_____ 电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在_____ 里,以隔绝空气。
(3)汽车安全气囊的气体发生剂 NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 NaN3分解 2NaN3 = 2Na + 3N2,从而为气囊充气,该反应属于____ 反应(填基本反应类型)。
ⅱ.产生的Na 立即与Fe2O3发生置换反应生成Na2O,化学方程式是_____ 。
ⅲ.NaHCO3是冷却剂,吸收产气过程释放的热量。NaHCO3起冷却作用时发生反应的化学方程式为_____ 。
ⅳ.一个安全气囊通常装有 50 g NaN3,其完全分解所释放的 N2为_____ mol。
(1)钠的原子结构示意图为
 ,钠在反应中容易
,钠在反应中容易(2)金属钠非常活泼,通常保存在
(3)汽车安全气囊的气体发生剂 NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 NaN3分解 2NaN3 = 2Na + 3N2,从而为气囊充气,该反应属于
ⅱ.产生的Na 立即与Fe2O3发生置换反应生成Na2O,化学方程式是
ⅲ.NaHCO3是冷却剂,吸收产气过程释放的热量。NaHCO3起冷却作用时发生反应的化学方程式为
ⅳ.一个安全气囊通常装有 50 g NaN3,其完全分解所释放的 N2为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】简要回答下列问题。
(1)除去Na2CO3固体中混有少量NaHCO3的方法是___________ 。
(2)用食醋除去水壶内壁的水垢主要成分是CaCO3和Mg(OH)2的原因是___________ 。
(3)写出一种防止自行车上金属部件腐蚀的方法是___________
(1)除去Na2CO3固体中混有少量NaHCO3的方法是
(2)用食醋除去水壶内壁的水垢主要成分是CaCO3和Mg(OH)2的原因是
(3)写出一种防止自行车上金属部件腐蚀的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是_______ (用离子方程式表示)。
(2)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液 溶液I
溶液I  沉淀II
沉淀II  Fe2O3
Fe2O3
①H2O2溶液的作用是_______ 。
②“溶液I”的溶质为_______ (填化学式),写 出由“溶液I”到“沉淀II”反应的离子方程式:_______ 。
③“操作III”的名称为_______ 。
(3)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:_______ (填标号);重复上述操作步骤,直至装置A恒重,记为m3 g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=_______ (列出计算式即可)。
(1)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是
(2)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液
 溶液I
溶液I  沉淀II
沉淀II  Fe2O3
Fe2O3①H2O2溶液的作用是
②“溶液I”的溶质为
③“操作III”的名称为
(3)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】钴盐在生活和生产中有着重要应用。
(1)干燥剂变色硅胶常含有 。常见氯化钴晶体的颜色如下:
。常见氯化钴晶体的颜色如下:
变色硅胶吸水饱和后颜色变成__________ ,硅胶中添加 的作用
的作用__________ 。
(2)草酸钴是制备钴氧化物的重要原料,常用 溶液和
溶液和 溶液制取难溶于水的
溶液制取难溶于水的 晶体。
晶体。
①常温下, 溶液的
溶液的
__________ 7(填“>”“=”或“<”)。(已知:常温下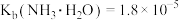 ,
, ,
,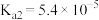 。)
。)
②制取 晶体时,还需加入适量氨水,其作用是
晶体时,还需加入适量氨水,其作用是__________ 。
③在空气中加热 二水合草酸钴
二水合草酸钴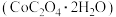 ,受热过程中在不同温度范围内分别得到一种固体物质。已知
,受热过程中在不同温度范围内分别得到一种固体物质。已知 的两种常见化合价为
的两种常见化合价为 价和
价和 价,
价,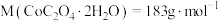 。
。
ⅰ.温度在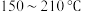 范围内,固体物质为
范围内,固体物质为__________ (填化学式,下同);
ⅱ.从 加热到
加热到 时生成一种钴的氧化物和
时生成一种钴的氧化物和 ,此过程发生反应的化学方程式是
,此过程发生反应的化学方程式是__________ 。
(1)干燥剂变色硅胶常含有
 。常见氯化钴晶体的颜色如下:
。常见氯化钴晶体的颜色如下:化学式 |
|
|
|
|
颜色 | 蓝色 | 蓝紫色 | 紫红色 | 粉红色 |
变色硅胶吸水饱和后颜色变成
 的作用
的作用(2)草酸钴是制备钴氧化物的重要原料,常用
 溶液和
溶液和 溶液制取难溶于水的
溶液制取难溶于水的 晶体。
晶体。①常温下,
 溶液的
溶液的
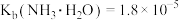 ,
, ,
,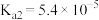 。)
。)②制取
 晶体时,还需加入适量氨水,其作用是
晶体时,还需加入适量氨水,其作用是③在空气中加热
 二水合草酸钴
二水合草酸钴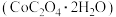 ,受热过程中在不同温度范围内分别得到一种固体物质。已知
,受热过程中在不同温度范围内分别得到一种固体物质。已知 的两种常见化合价为
的两种常见化合价为 价和
价和 价,
价,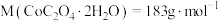 。
。温度范围/ | 150~210 | 290~320 |
固体质量/g | 8.82 | 4.82 |
ⅰ.温度在
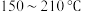 范围内,固体物质为
范围内,固体物质为ⅱ.从
 加热到
加热到 时生成一种钴的氧化物和
时生成一种钴的氧化物和 ,此过程发生反应的化学方程式是
,此过程发生反应的化学方程式是
您最近一年使用:0次


 X+H2O+CO2↑
X+H2O+CO2↑ 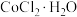
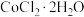


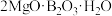 ,含
,含 、
、 、铁和铝的氧化物等杂质)生产硼酸
、铁和铝的氧化物等杂质)生产硼酸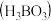 并回收硫酸镁的工艺流程如图:
并回收硫酸镁的工艺流程如图: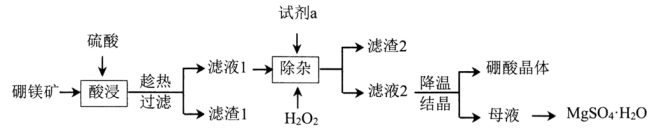
 硫酸镁晶体,得到
硫酸镁晶体,得到 硫酸镁固体,则硫酸镁晶体的结晶水含量x=
硫酸镁固体,则硫酸镁晶体的结晶水含量x=

