高中化学课本必修一中出现的部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
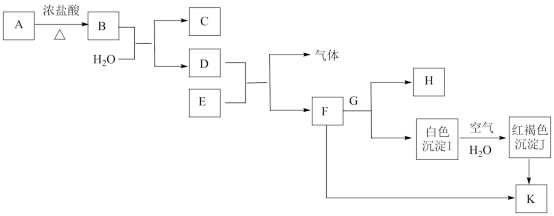
(1)E和H的化学式为:E___________ ;H___________ 。
(2)检验K溶液中阳离子的试剂是___________ 。若K中含有F的杂质,应加入___________ (填化学式)除杂。
(3)I转化为J的化学方程式为___________ 。
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
(5)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为___________ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是___________ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是___________ 。
④ 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为___________ 。

(1)E和H的化学式为:E
(2)检验K溶液中阳离子的试剂是
(3)I转化为J的化学方程式为
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
A.胶体L的分散质粒子直径为 | B.胶体L比K的饱和溶液颜色深 |
| C.胶体L是均一的分散系 | D.胶体L具有丁达尔效应 |
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是
④
 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
更新时间:2022-01-27 19:32:36
|
相似题推荐
【推荐1】Ⅰ.由三种常见元素组成的化合物A,按如下流程进行实验。气体B、C、D均无色、无臭,B、D是纯净物;浓硫酸增重3.60g,碱石灰增重17.60g;溶液F焰色反应呈黄色。

请回答:
(1)组成A的非金属元素是_____ ,气体B的结构简式_____ 。
(2)固体A与足量水反应的化学方程式是_____ 。
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程式_____ 。
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,向NaBr溶液中通入一定量Cl2,将少量分液漏斗中溶液滴入试管中,取试管振荡,静止后观察现象。实验装置如图:

(4)说明氧化性 Br2>I2的实验现象是_____ 。
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗中通入Cl2 未过量。试设计简单实验方案检____ 。

请回答:
(1)组成A的非金属元素是
(2)固体A与足量水反应的化学方程式是
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程式
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,向NaBr溶液中通入一定量Cl2,将少量分液漏斗中溶液滴入试管中,取试管振荡,静止后观察现象。实验装置如图:

(4)说明氧化性 Br2>I2的实验现象是
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗中通入Cl2 未过量。试设计简单实验方案检
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.化学试剂的妥善保存十分重要,共价化合物A由三种常见的短周期元素组成,常温常压下是一种有特殊气味的无色液体,易与强氧化剂反应,实验室必须率封避光保存。按以下流程进行实验(以下反应都为充分反应,气体F溶于水部分忽略不计);

(1)组成A的元素的元素符号为___________ ;G的化学式为___________ 。
(2)液体A反应生成B和C的化学方程式为___________ 。
Ⅱ.Na2S2O3,又名大苏打、海波,可用以除去自来水中的多余氯气,在实验室可以用新制氯水模拟含多余氯气的自来水,向新制氯水中滴入Na2S2O3溶液。
(3)新制氯水与Na2S2O3溶液反应的离子方程式为___________ 。
(4)新制氯水中的氯气被全部除尽后,如果继续滴入Na2S2O3溶液有可能发生反应的离子方程式为___________ 。

(1)组成A的元素的元素符号为
(2)液体A反应生成B和C的化学方程式为
Ⅱ.Na2S2O3,又名大苏打、海波,可用以除去自来水中的多余氯气,在实验室可以用新制氯水模拟含多余氯气的自来水,向新制氯水中滴入Na2S2O3溶液。
(3)新制氯水与Na2S2O3溶液反应的离子方程式为
(4)新制氯水中的氯气被全部除尽后,如果继续滴入Na2S2O3溶液有可能发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】盐X由三种元素组成,其具有良好的热电性能,在热电转换领域具有广阔的应用前景。为研究它的组成和性质,现取12.30 g化合物X进行如下实验:

试根据以上内容回答下列问题:
(1)组成X的三种元素中除了O元素外的另外两种是_______ (写元素符号)。
(2)无色溶液B中通入过量 产生白色沉淀C的离子方程式为
产生白色沉淀C的离子方程式为_______ 。
(3)蓝色溶液F中通入中 气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为
气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为_______ 。
(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,并释放出一种无色无味的气体,其化学方程式为_______ 。
(5)写出简要实验步骤检验无色溶液E中的主要阴离子:_______ 。

试根据以上内容回答下列问题:
(1)组成X的三种元素中除了O元素外的另外两种是
(2)无色溶液B中通入过量
 产生白色沉淀C的离子方程式为
产生白色沉淀C的离子方程式为(3)蓝色溶液F中通入中
 气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为
气体会产生白色沉淀,该沉淀仅含两种元素其中氯元素质量分数为35.7%,其离子方程式为(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,并释放出一种无色无味的气体,其化学方程式为
(5)写出简要实验步骤检验无色溶液E中的主要阴离子:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究NaClO的性质。
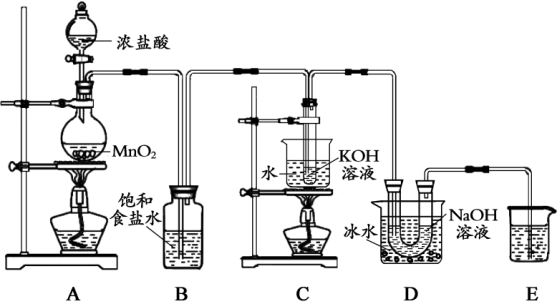
回答下列问题:
(1)A中反应的化学方程式是___________ 。
(2)C中反应的离子方程式为:□Cl2+□OH- □
□ +□_____+□______,
+□_____+□______,___________ 。
(3)D中采用冰水浴冷却的目的是___________ 。
(4)探究NaClO的性质。
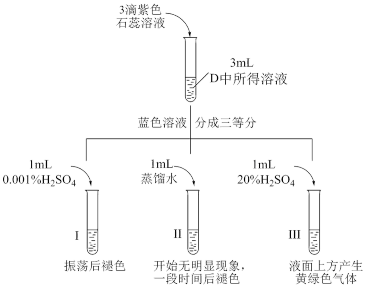
①I中溶液褪色的原因是___________ 。
②III中产生黄绿色气体的原因是___________ (写离子方程式)。
(5)通过上述实验可知,影响氧化还原反应的因素有______ 。

回答下列问题:
(1)A中反应的化学方程式是
(2)C中反应的离子方程式为:□Cl2+□OH-
 □
□ +□_____+□______,
+□_____+□______,(3)D中采用冰水浴冷却的目的是
(4)探究NaClO的性质。

①I中溶液褪色的原因是
②III中产生黄绿色气体的原因是
(5)通过上述实验可知,影响氧化还原反应的因素有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学实验小组为探究和比较 和氯水的漂白性,设计了如下的实验装置。
和氯水的漂白性,设计了如下的实验装置。

回答下列问题:
(1)装置A中盛装浓硫酸的仪器名称是_______ ,实验室用装置A制备 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。
(2)实验室用装置E制备 ,其反应的离子方程式为
,其反应的离子方程式为_______ ,若有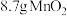 参加反应,则转移的电子总数为
参加反应,则转移的电子总数为_______ 。
(3)小组中甲同学认为 和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将
和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将 和
和 等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是
等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是_______ (用离子方程式表示)。
(4)SO2使酸性KMnO4溶液褪色的离子方程式_______ 。
(5)SO2通入到氢硫酸中产生淡黄色沉淀的化学方程式_______ ,该反应中氧化产物与还原产物的的物质的量之比是_______ 。
 和氯水的漂白性,设计了如下的实验装置。
和氯水的漂白性,设计了如下的实验装置。
回答下列问题:
(1)装置A中盛装浓硫酸的仪器名称是
 ,发生反应的化学方程式为
,发生反应的化学方程式为(2)实验室用装置E制备
 ,其反应的离子方程式为
,其反应的离子方程式为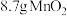 参加反应,则转移的电子总数为
参加反应,则转移的电子总数为(3)小组中甲同学认为
 和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将
和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将 和
和 等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是
等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是(4)SO2使酸性KMnO4溶液褪色的离子方程式
(5)SO2通入到氢硫酸中产生淡黄色沉淀的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】下图是实验室制备氯气的装置图。

(1)实验室用浓盐酸和二氧化锰固体制取氯气,制得的氯气中往往混有___________ 气体。
(2)D 中浓硫酸的作用是:___________ 。
(3)氯气的收集方法是:___________ 。
(4)F 中盛放的是___________ 溶液,作用是___________ 。
(5)将氯气通入氢氧化钙悬浊液中,可以得到漂粉精,漂粉精的有效成分是___________ 。
(6)检验氯气的方法是,使用湿润的___________ 试纸靠近气体,试纸___________ 。
(7)已知 3Cl2+8NH3=6NH4Cl+N2,将制得的氯气靠近装有浓氨水的试剂瓶口,可以在试剂瓶口观察到的现象是:___________ 。

(1)实验室用浓盐酸和二氧化锰固体制取氯气,制得的氯气中往往混有
(2)D 中浓硫酸的作用是:
(3)氯气的收集方法是:
(4)F 中盛放的是
(5)将氯气通入氢氧化钙悬浊液中,可以得到漂粉精,漂粉精的有效成分是
(6)检验氯气的方法是,使用湿润的
(7)已知 3Cl2+8NH3=6NH4Cl+N2,将制得的氯气靠近装有浓氨水的试剂瓶口,可以在试剂瓶口观察到的现象是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】某一无色澄清透明溶液,可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,实验:
中的一种或几种,实验:
①用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色
②取少量该溶液加入 溶液有白色沉淀生成,过滤,往沉淀中加入足量盐酸后,沉淀部分溶解,并有气体生成。
溶液有白色沉淀生成,过滤,往沉淀中加入足量盐酸后,沉淀部分溶解,并有气体生成。
③在滤液中滴加 溶液,产生白色沉淀。
溶液,产生白色沉淀。
(1)由此推断,该溶液中肯定含有的离子为_______ ,肯定不含有的离子为_______ ,可能含有的离子为_______ 。
(2)②中沉淀加入足量盐酸后,沉淀部分溶解,并有气体生成的离子方程式_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,实验:
中的一种或几种,实验:①用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色
②取少量该溶液加入
 溶液有白色沉淀生成,过滤,往沉淀中加入足量盐酸后,沉淀部分溶解,并有气体生成。
溶液有白色沉淀生成,过滤,往沉淀中加入足量盐酸后,沉淀部分溶解,并有气体生成。③在滤液中滴加
 溶液,产生白色沉淀。
溶液,产生白色沉淀。(1)由此推断,该溶液中肯定含有的离子为
(2)②中沉淀加入足量盐酸后,沉淀部分溶解,并有气体生成的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】紫色固体化合物X由3种元素组成,能溶于水,具有强氧化性,与盐酸反应有黄绿色气体产生,得到的溶液滴加KSCN溶液呈血红色,用透过蓝色钴玻璃观察焰色试验的火焰呈紫色。取1.98gX按如下流程完成实验:

请回答:
(1)紫色固体X的化学式是___________ ,固体混合物Y的成分___________ (用化学式表示)。
(2)X与足量的盐酸反应的离子方程式___________ 。
(3)已知: ;为验证化合物
;为验证化合物 中
中 元素的含量,某同学设计并完成了如下实验:
元素的含量,某同学设计并完成了如下实验: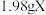 与足量的氢碘酸反应得到棕黄色溶液,
与足量的氢碘酸反应得到棕黄色溶液, 萃取,标准
萃取,标准 滴定至终点,换算得
滴定至终点,换算得 的物质的量,再换算得到固体X中Z元素的质量小于
的物质的量,再换算得到固体X中Z元素的质量小于 。用标准
。用标准 溶液滴定达到终点时的实验现象是
溶液滴定达到终点时的实验现象是___________ 。该滴定方法得到的结果: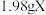 中
中 元素的质量小于
元素的质量小于 ,分析原因
,分析原因___________ (不考虑实验操作上的误差)。

请回答:
(1)紫色固体X的化学式是
(2)X与足量的盐酸反应的离子方程式
(3)已知:
 ;为验证化合物
;为验证化合物 中
中 元素的含量,某同学设计并完成了如下实验:
元素的含量,某同学设计并完成了如下实验: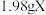 与足量的氢碘酸反应得到棕黄色溶液,
与足量的氢碘酸反应得到棕黄色溶液, 萃取,标准
萃取,标准 滴定至终点,换算得
滴定至终点,换算得 的物质的量,再换算得到固体X中Z元素的质量小于
的物质的量,再换算得到固体X中Z元素的质量小于 。用标准
。用标准 溶液滴定达到终点时的实验现象是
溶液滴定达到终点时的实验现象是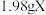 中
中 元素的质量小于
元素的质量小于 ,分析原因
,分析原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表中的28号元素 Ni有重要的用途,它有良好的耐高温、耐腐蚀、防锈功能,在电池、催化剂方面也有广泛应用。工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:

已知:电极电位(E)能体现微粒的氧化还原能力强弱,如:H2-2e-=2H+ E=0.00V Cu-2e-=Cu2+ E=0.34V Fe-2e-=Fe2+ E=-0.44V Ni-2e-=Ni2+ E= -0.25V
请回答下列问题:
(1)镍在周期表中的位置为_______________ 。焰色反应实验可以用光洁无锈的镍丝代替铂丝蘸取化学试剂灼烧,原因是___________ 。
(2)石英造渣除铁时主要发生的化学反应方程式:________________ (产物以氧化物的形式表示)。
(3)电解制粗镍时阳极发生的主要电极反应式:________________ 。
(4)工业上由 NiSO4溶液制得 Ni(OH)2后,再滴加 NaClO溶液制NiO(OH),滴加过程中发生反应的离子方程式为________________ 。
(5)电解精炼镍的过程需控制pH 为2~5,原因是pH 太小_________ ;pH太大 ________ 。

已知:电极电位(E)能体现微粒的氧化还原能力强弱,如:H2-2e-=2H+ E=0.00V Cu-2e-=Cu2+ E=0.34V Fe-2e-=Fe2+ E=-0.44V Ni-2e-=Ni2+ E= -0.25V
请回答下列问题:
(1)镍在周期表中的位置为
(2)石英造渣除铁时主要发生的化学反应方程式:
(3)电解制粗镍时阳极发生的主要电极反应式:
(4)工业上由 NiSO4溶液制得 Ni(OH)2后,再滴加 NaClO溶液制NiO(OH),滴加过程中发生反应的离子方程式为
(5)电解精炼镍的过程需控制pH 为2~5,原因是pH 太小
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】电子工业中常用覆铜板为基材制作印刷电路板,原理是利用 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
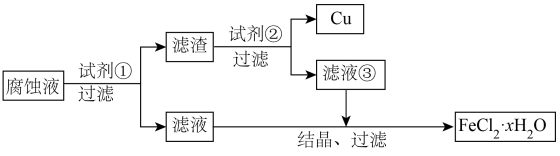
(1) 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为___________ 。
(2)过量试剂①为___________ ;过量试剂②为___________ 。
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是___________ ,现象是___________ 。 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是___________ 。
(4)取 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:
 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
(1)
 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为(2)过量试剂①为
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是
 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是(4)取
 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:| 序号 | 现象 | 用方程式解释现象 |
| ① | 开始无明显现象 | |
| ② | 稍后出现白色沉淀 |  |
| ③ | 空气中放置一段时间后,出现红褐色沉淀 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用______ 来区分Fe(OH)3胶体和FeCl3溶液。
(2)向盛有FeSO4溶液的试管中滴加NaOH溶液,请描述发生的现象______ 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是______ 。
(4)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:
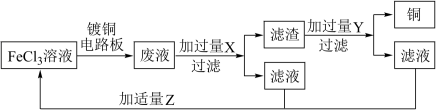
①请写出FeCl3溶液与铜反应的离子方程式______ 。
②试剂X在反应中体现______ (填“氧化性”或“还原性”)。
③Z可选用的试剂有______ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
(2)向盛有FeSO4溶液的试管中滴加NaOH溶液,请描述发生的现象
(3)铁粉与水蒸气在高温条件下反应的化学方程式是
(4)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收
 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:
①请写出FeCl3溶液与铜反应的离子方程式
②试剂X在反应中体现
③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】I.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
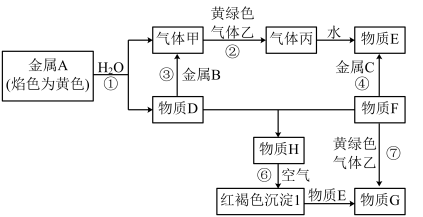
请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:_______ ;
(2)反应③的离子方程式:_______ ;
(3)反应⑦的离子方程式:_______ ;
(4)反应⑥的化学方程式:_______ 。
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
(5)铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是_______ 的质量分数;当合金熔点最低时,合金中铅与锡的质量比为_______ 。

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
(7)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿[主要成分Cu2(OH)2CO3],从其化学式可知铜绿是铜与_______ (填物质的化学式)长期作用的结果。

请回答下列问题:
(1)D溶液和F溶液在空气中混合的现象:
(2)反应③的离子方程式:
(3)反应⑦的离子方程式:
(4)反应⑥的化学方程式:
II.合金是由两种或两种以上的金属(或金属或非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |

(6)保险丝由铋、铅、锡、镉等金属组成,其熔点约为_______。
| A.20~40℃ | B.60~80℃ | C.230~250℃ | D.300~320℃ |
您最近一年使用:0次



