回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是___________ (填序号,下同);能导电的是___________ ;属于电解质的是___________ ;属于非电解质的是___________ 。分别写出④和⑤的电离方程式:___________ 。
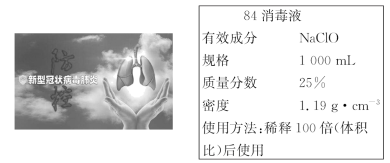
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是___________ 。38gCH3COOOH中含有的O原子数为___________ NA,含有的H原子的物质的量为___________ 。
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式___________ 。过氧化氢的水溶液叫双氧水,2mol/L的双氧水500mL完全分解生成氧气的体积为___________ L(标准状态),转移电子数为___________ NA
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为___________ ,原子个数之比为___________ ,密度之比为___________ 。
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =___________ mol/L。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =
更新时间:2022-01-07 23:22:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知铜和浓硫酸可以在加热条件下发生反应
(1)请写出该反应化学方程式___________ 。
(2)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为___________ 。
(3)一定量的铜片与含1.2mol的 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为___________ L(假设气体全部逸出)。
(4)将(3)中反应后所得的溶液稀释后与足量的 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为___________ g。
(1)请写出该反应化学方程式
(2)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为
(3)一定量的铜片与含1.2mol的
 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的气体在标准状况下的体积为(4)将(3)中反应后所得的溶液稀释后与足量的
 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。
(1) 元素有
元素有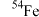 、
、 、
、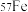 、
、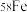 四种核素,它们互为
四种核素,它们互为___________ ,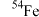 的中子数为
的中子数为___________ ,1个 原子的质量是
原子的质量是___________ 。
(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:___________ 。
(3)氯化铁溶于水后,电离方程式为___________ 。检验氧化铁溶液中的溶质负离子的操作、现象和结论是:___________ 。
(4)将少量饱和 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。

用红色激光灯分别照射分散系甲和丙,现象的差异为:___________ 。向丙中加入少量稀盐酸,会出现和乙中相同的现象,原因是:___________ 。
(5)5.410g氧化铁晶体( )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(6)若用氯化铁晶体( )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为___________ 。(保留三位小数)
 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。(1)
 元素有
元素有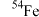 、
、 、
、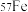 、
、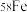 四种核素,它们互为
四种核素,它们互为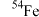 的中子数为
的中子数为 原子的质量是
原子的质量是(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:
(3)氯化铁溶于水后,电离方程式为
(4)将少量饱和
 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
用红色激光灯分别照射分散系甲和丙,现象的差异为:
(5)5.410g氧化铁晶体(
 )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为(6)若用氯化铁晶体(
 )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。| A.定容时,俯视凹液面最低点 |
| B.转移时,有少量液体溅出 |
C. 晶体已部分失水 晶体已部分失水 |
| D.烧杯、玻璃棒未洗涤 |
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】实验室进行以下实验。请回答下列问题:
(1)实验室配制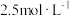 盐酸
盐酸 ,需要量取
,需要量取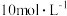 浓盐酸
浓盐酸_______  ,配制过程中需用的玻璃仪器有量筒、烧杯、玻璃棒、
,配制过程中需用的玻璃仪器有量筒、烧杯、玻璃棒、_______ 。配制过程中,多次用到玻璃棒,在此过程中玻璃棒的两个作用分别为_______ 、_______ 。
(2)下列操作会使所配制的盐酸浓度偏低的是_______(填标号)。
(3)称量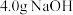 ,溶于
,溶于 水中,向其中滴加
水中,向其中滴加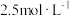 盐酸至恰好完全反应,消耗盐酸的体积为
盐酸至恰好完全反应,消耗盐酸的体积为_______  ,若称量的
,若称量的 中含有少量
中含有少量 ,则消耗盐酸的体积将
,则消耗盐酸的体积将_______ (填“偏大”“偏小”或“不变”)。
(1)实验室配制
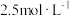 盐酸
盐酸 ,需要量取
,需要量取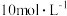 浓盐酸
浓盐酸 ,配制过程中需用的玻璃仪器有量筒、烧杯、玻璃棒、
,配制过程中需用的玻璃仪器有量筒、烧杯、玻璃棒、(2)下列操作会使所配制的盐酸浓度偏低的是_______(填标号)。
| A.量取浓盐酸时仰视量筒的刻度线 |
| B.转移溶液时,未洗涤烧杯和玻璃棒 |
| C.定容时俯视观察液面 |
| D.定容振荡后,发现液面低于刻度线,然后补加蒸馏水至刻度线 |
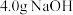 ,溶于
,溶于 水中,向其中滴加
水中,向其中滴加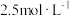 盐酸至恰好完全反应,消耗盐酸的体积为
盐酸至恰好完全反应,消耗盐酸的体积为 ,若称量的
,若称量的 中含有少量
中含有少量 ,则消耗盐酸的体积将
,则消耗盐酸的体积将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】判断下列溶液配制的误差(填“大于”“小于”或“等于”):
(1)将6.0g冰醋酸加水配成100mL溶液,所得溶液中H+的浓度_____ 1mol/L
(2)将18.4mol/L浓硫酸加等体积水稀释,所得溶液中 的浓度
的浓度_____ 9.2mol/L
(3)将46mL乙醇(密度0.8g/cm3)溶于500mL水,所得溶液的浓度_____ 1.6mol/L
(4)将某温度下的50mL 2mol/L CuSO4饱和溶液降温结晶,析出8g晶体,则剩余溶液的浓度____ 1mol/L
(1)将6.0g冰醋酸加水配成100mL溶液,所得溶液中H+的浓度
(2)将18.4mol/L浓硫酸加等体积水稀释,所得溶液中
 的浓度
的浓度(3)将46mL乙醇(密度0.8g/cm3)溶于500mL水,所得溶液的浓度
(4)将某温度下的50mL 2mol/L CuSO4饱和溶液降温结晶,析出8g晶体,则剩余溶液的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液0.2 L,部分离子的浓度如下表所示:
(1)该混合溶液中硝酸镁的物质的量浓度为_______ ,将该混合溶液加水稀释至体积为1 L,稀释后溶液中NO 的物质的量浓度为
的物质的量浓度为_______ 。
(2)混合液中硝酸铵的物质的量为_______ ,硝酸钾的质量为_______ 。
(3)向该溶液中加入_______ mol NaOH可以使Mg2+完全沉淀,写出该反应的化学方程式_______
| 离子种类 | NH | Mg2+ | NO |
| 离子的物质的量浓度( mol·L-1) | 0.2 | 0.1 | 0.6 |
(1)该混合溶液中硝酸镁的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为(2)混合液中硝酸铵的物质的量为
(3)向该溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)在下列物质中,是纯净物的是_______ (填序号,下同),可以导电的是_______ ,是电解质的有_______ 。
①固体氯化钠②熔融氢氧化钠③蔗糖晶体④乙醇⑤NaHSO4溶液⑥氢氧化钠溶液⑦盐酸⑧Ba(OH)2溶液
(2)向盛有⑧的烧杯中逐滴加入⑤,当溶液中的Ba2+恰好完全沉淀时,发生反应的离子方程式为_______ 。
(3)工业上利用电解①的饱和溶液可制备Cl2、H2和NaOH,发生反应的化学方程式为_______ 。
(4)某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、CO 、SO
、SO 、NO
、NO 。现进行如下实验:
。现进行如下实验:
①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定有_______ ,肯定没有_______ 。
(1)在下列物质中,是纯净物的是
①固体氯化钠②熔融氢氧化钠③蔗糖晶体④乙醇⑤NaHSO4溶液⑥氢氧化钠溶液⑦盐酸⑧Ba(OH)2溶液
(2)向盛有⑧的烧杯中逐滴加入⑤,当溶液中的Ba2+恰好完全沉淀时,发生反应的离子方程式为
(3)工业上利用电解①的饱和溶液可制备Cl2、H2和NaOH,发生反应的化学方程式为
(4)某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、CO
 、SO
、SO 、NO
、NO 。现进行如下实验:
。现进行如下实验:①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示为按树状分类法对一组物质进行的分类。回答下列问题。
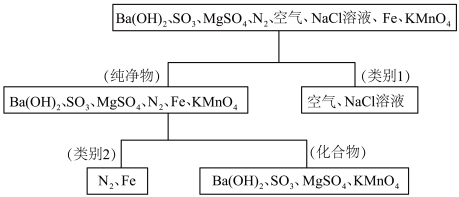
(1)类别2为___________ 。
(2)上述物质中属于电解质的是___________ 。
(3)将MgSO4溶液和Ba(OH)2溶液混合,溶液恰好呈中性,对应的离子方程式为___________ 。
(4)写出实验室利用上述物质制备O2的化学方程式:___________ 。

(1)类别2为
(2)上述物质中属于电解质的是
(3)将MgSO4溶液和Ba(OH)2溶液混合,溶液恰好呈中性,对应的离子方程式为
(4)写出实验室利用上述物质制备O2的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)现有以下物质(用编号填写下列空白):①Al;②液态氧;③硝酸钾溶液;④KOH固体;⑤蔗糖;⑥SiO2;⑦NaCl;⑧空气;⑨硫酸铜晶体(CuSO4·5H2O);⑩NO2;属于酸性氧化物的是:_______ ;能导电的有:_______ ;属于电解质的是:_______ ;属于盐的有:_______ ;属于混合物的有:_______
(2)有以下物质,按要求用编号填空①NH3 ②CO2 ③NaOH ④Na2O2 ⑤Cl2 ⑥NH4Cl ⑦NaCl;含有极性共价键的物质有:_______ ;含有非极性共价键的物质有:_______ ;属于离子化合物的是:_______ ;只含离子键的有:_______
(3)用双线桥法标出Br2+SO2+2H2O=2HBr+H2SO4反应电子转移的方向和数目:_______ 。此反应中氧化剂是_______ ,还原剂是_______ ,还原产物是_______ ,当消耗32gSO2时,生成的氧化产物物质的量为_______
(1)现有以下物质(用编号填写下列空白):①Al;②液态氧;③硝酸钾溶液;④KOH固体;⑤蔗糖;⑥SiO2;⑦NaCl;⑧空气;⑨硫酸铜晶体(CuSO4·5H2O);⑩NO2;属于酸性氧化物的是:
(2)有以下物质,按要求用编号填空①NH3 ②CO2 ③NaOH ④Na2O2 ⑤Cl2 ⑥NH4Cl ⑦NaCl;含有极性共价键的物质有:
(3)用双线桥法标出Br2+SO2+2H2O=2HBr+H2SO4反应电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列物质:①Fe②Br2③Na2O④CO⑤CO2⑥SO3⑦NH3⑧H2S⑨HCl⑩H2SO4⑪Ba(OH)2⑫NaCl⑬蔗糖⑭NaCl溶液。属于电解质的是___ ,属于非电解质的是___ ,能导电的是___ 。
(2)写出下列物质在水中的电离方程式:
NaHSO4:___ 。
H2SO4:___ 。
Ba(OH)2:___ 。
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现___ ,原因:___ ,随后___ ,原因(用离子方程式表示)__ 。
(4)将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图。回答下列问题:

①写出OA段和BC段反应的离子方程式:OA:___ ;BC:___ 。
②原Mg—Al合金的质量是___ 。
③原HCl溶液的物质的量浓度是___ 。
④所加NaOH溶液的物质的量浓度是___ 。
(1)下列物质:①Fe②Br2③Na2O④CO⑤CO2⑥SO3⑦NH3⑧H2S⑨HCl⑩H2SO4⑪Ba(OH)2⑫NaCl⑬蔗糖⑭NaCl溶液。属于电解质的是
(2)写出下列物质在水中的电离方程式:
NaHSO4:
H2SO4:
Ba(OH)2:
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现
(4)将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图。回答下列问题:

①写出OA段和BC段反应的离子方程式:OA:
②原Mg—Al合金的质量是
③原HCl溶液的物质的量浓度是
④所加NaOH溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求写出下列方程式
(1)NH4HSO4在水溶液中的电离方程式:_______ 。
(2)CH3COONa在水溶液中的电离方程式:_______ 。
(3)亚硫酸的电离方程式:_______ 、_______ 。
(4)Ca(OH)2溶液与少量NaHCO3溶液反应的离子方程式:_______ 。
(5)NaAlO2溶液中通入过量CO2的离子方程式:_______ 。
(1)NH4HSO4在水溶液中的电离方程式:
(2)CH3COONa在水溶液中的电离方程式:
(3)亚硫酸的电离方程式:
(4)Ca(OH)2溶液与少量NaHCO3溶液反应的离子方程式:
(5)NaAlO2溶液中通入过量CO2的离子方程式:
您最近一年使用:0次