物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。下图为氯元素的单质及其化合物的“价~类”二维图。请回答下列问题:

(1)二维图中X的化学式(分子式)为_______ 。
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式_______ 。
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式_______ ,实验室对Cl2进行尾气处理的离子方程式为_______ 。
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作_______ (填“氧化剂”或“还原剂”)。

(1)二维图中X的化学式(分子式)为
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作
更新时间:2022-02-24 16:36:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠( )属于
)属于_______ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为_______ 价。
(2)将上述反应的化学方程式改写成离子方程式:_______ 。
(3)该反应中NaOH_______ (填“是氧化产物”、“是还原产物”或“既不是氧化产物又不是还原产物”,下同),
_______ 。
(4)当生成48g 时,至少有
时,至少有_______ g水参与反应。
 )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:(1)高铁酸钠(
 )属于
)属于(2)将上述反应的化学方程式改写成离子方程式:
(3)该反应中NaOH

(4)当生成48g
 时,至少有
时,至少有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有代表就食品和药品行业存在的问题向“两会”提交议案,得到与会众多代表的关注。
(1)某品牌抗酸药的主要成分有糖衣、氢氧化镁、淀粉。试写出该抗酸药发挥功效时的离子方程式:___ 。
(2)甲状腺肿大俗称“大脖子病”,是由身体缺少______ (填元素符号)所致,该元素属____ (填“常量元素”或“微量元素”)
(3)药物“速力菲”(琥珀酸亚铁薄膜衣片) 适用于明确原因的缺铁性贫血。其主要活性成分是琥珀酸亚铁(含Fe2+ 34.0%-36.0%的无水碱式盐,不溶于水也不溶于乙醇)。性状为薄膜衣片,除去薄膜衣后显 暗黄色。使用时与维生素C同服有利于吸收等。该药品的薄膜衣的作用是______ ,该药品与维生素C同服效果更好,这是因为维生素C具有__ (填“氧化”或“还原”)性,薄膜衣是一种淀粉制品,淀粉在人体内水解最终转化为______ 。
(1)某品牌抗酸药的主要成分有糖衣、氢氧化镁、淀粉。试写出该抗酸药发挥功效时的离子方程式:
(2)甲状腺肿大俗称“大脖子病”,是由身体缺少
(3)药物“速力菲”(琥珀酸亚铁薄膜衣片) 适用于明确原因的缺铁性贫血。其主要活性成分是琥珀酸亚铁(含Fe2+ 34.0%-36.0%的无水碱式盐,不溶于水也不溶于乙醇)。性状为薄膜衣片,除去薄膜衣后显 暗黄色。使用时与维生素C同服有利于吸收等。该药品的薄膜衣的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据相关化学知识及原理回答下列问题:
(1)阅读并分析体检报告,可以初步诊断体检者的身体状况。
注:1mmol=10-3mol
①在图中所示的体检报告中,表示葡萄糖指标的物理量是___ (填字母)。
a.质量分数 b.溶解度 c.摩尔质量 d.物质的量浓度
②科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颗粒(直径为20~60nm)。检测时NaAuCl4发生了__ (填“氧化”或“还原”)反应。
(2)氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。
①在氧化还原反应中,氧化剂___ 电子,发生___ 反应。
②下列物质在氧化还原反应中,常作还原剂的有__ ;常作氧化剂的有__ (均填序号)。
a.KMnO4 b.铝 c.氯气 d.FeCl3 e.一氧化碳
③已知钠与冷水剧烈反应,离子方程式是__ 。铁与水蒸气发生反应:3Fe+4H2O(g) Fe3O4+4H2。钠与水反应中,若消耗4.6g钠,则生成氢气的体积为
Fe3O4+4H2。钠与水反应中,若消耗4.6g钠,则生成氢气的体积为__ L(标准状况下)。事实证明,铁的还原性比钠的还原性__ (填“强”或“弱”)。
(1)阅读并分析体检报告,可以初步诊断体检者的身体状况。
| 序号 | 项目名称 | 英文缩写 | 检查结果 | 单位 | 参考范围 |
| 15 | *钙 | Ca | 0.68 | mmol/L | 213~270 |
| 16 | 胱抑素C | CysC | 0.78 | mg/L | 0.59~1.03 |
| 17 | *尿素 | Urea | 4.18 | mmol/L | 2.78~7.14 |
| 18 | *葡萄糖 | Olu | 5.1 | mmol/L | 3.9~6.1 |
| 19 | *无机磷 | P | 1.19 | mmol/L | 0.81~1.45 |
注:1mmol=10-3mol
①在图中所示的体检报告中,表示葡萄糖指标的物理量是
a.质量分数 b.溶解度 c.摩尔质量 d.物质的量浓度
②科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颗粒(直径为20~60nm)。检测时NaAuCl4发生了
(2)氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。
①在氧化还原反应中,氧化剂
②下列物质在氧化还原反应中,常作还原剂的有
a.KMnO4 b.铝 c.氯气 d.FeCl3 e.一氧化碳
③已知钠与冷水剧烈反应,离子方程式是
 Fe3O4+4H2。钠与水反应中,若消耗4.6g钠,则生成氢气的体积为
Fe3O4+4H2。钠与水反应中,若消耗4.6g钠,则生成氢气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下列变化中,涉及氧化还原反应的是_______ (填序号)。
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为 ,该反应所属基本反应类型是
,该反应所属基本反应类型是_______ (填4种基本反应类型中的一种),在反应中铁元素的化合价_______ (填“升高”或“降低”),该元素的原子_______ (填“失去”或“得到”)电子。该反应还原剂是_______ (填化学式,下同),氧化剂是_______ 。
(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作_______ 剂(填“氧化”或“还原”)。
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具_______ 性。(填“氧化”或“还原”)
(1)下列变化中,涉及氧化还原反应的是
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为
 ,该反应所属基本反应类型是
,该反应所属基本反应类型是(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为不可能实现的是___________ (填序号)。
(3)下列三个氧化还原反应中,由反应③可知KMnO4的氧化性比Cl2__________________ (“强”或“弱”)。反应②的离子方程式为___________ ,反应①的还原剂为___________ 。
①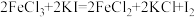 ②
②
③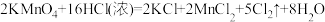
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为不可能实现的是
(3)下列三个氧化还原反应中,由反应③可知KMnO4的氧化性比Cl2
①
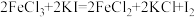 ②
②
③
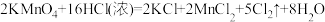
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室里用二氧化锰与浓盐酸反应来制取适量的氯气。现用浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为11.2升,(假设HCl全部参加反应)
(MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O)计算:
MnCl2+Cl2↑+2H2O)计算:
(1)参加的二氧化锰的质量_____________ 。
(2)被氧化的HCl的物质的量________________ 。
(MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O)计算:
MnCl2+Cl2↑+2H2O)计算:(1)参加的二氧化锰的质量
(2)被氧化的HCl的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)写出纯碱的化学式:_______ 。
(2)写出氯气和水反应的化学方程式:_______ 。
(3)写出碳酸氢钠与氢氧化钠反应的离子方程式:_______ 。
(4)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+8H2O+5Cl2↑,
则①氧化剂为:_______ 。
②反应中氯化氢表现出的性质是_______ (填写字母)。
a.还原性 b.酸性 c.氧化性
③若生成标准状况下22.4 Cl2则转移电子总数是_______ mol。
(1)写出纯碱的化学式:
(2)写出氯气和水反应的化学方程式:
(3)写出碳酸氢钠与氢氧化钠反应的离子方程式:
(4)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+8H2O+5Cl2↑,
则①氧化剂为:
②反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
③若生成标准状况下22.4 Cl2则转移电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据信息书写下列反应的方程式
(1)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:______ 。
(2)锶(Sr)原子的结构示意图如图所示: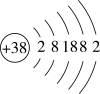 ,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:______ 。
(3)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅰ”的化学方程式:______ 。
②写出“反应Ⅱ”的离子方程式:______ 。
(1)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
(2)锶(Sr)原子的结构示意图如图所示:
 ,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:(3)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅰ”的化学方程式:
②写出“反应Ⅱ”的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列问题:
(1)请写出NaCl的电子式___________ ,甲烷的结构式___________ 。
(2)用反应方程式表示制备漂白粉的原理为:___________ 。
(3)漂白粉的有效成分是___________ ,小苏打的化学式为___________ 。
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示___________ 。
(1)请写出NaCl的电子式
(2)用反应方程式表示制备漂白粉的原理为:
(3)漂白粉的有效成分是
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次

 的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依次为
的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依次为

