下列说法正确的是
| A.可逆反应的化学反应限度不会随反应条件的改变而改变 |
| B.化学反应的限度决定了反应物在该条件下的最大转化率 |
| C.化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率 |
| D.在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值 |
20-21高一上·广东潮州·期末 查看更多[2]
更新时间:2022-02-27 12:50:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在一定条件下,向某 恒容密闭容器中充入
恒容密闭容器中充入 、
、 ,发生反应
,发生反应 ,测得反应
,测得反应 时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程
时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程 、
、 ,
, 、
、 只与温度有关]
只与温度有关]
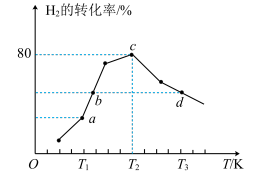
下列说法错误的是
 恒容密闭容器中充入
恒容密闭容器中充入 、
、 ,发生反应
,发生反应 ,测得反应
,测得反应 时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程
时,不同温度下氢气的转化率如图所示。[已知:该反应的速率方程 、
、 ,
, 、
、 只与温度有关]
只与温度有关]
下列说法错误的是
A.图中a、b、c三点对应的 由大到小的顺序为 由大到小的顺序为 |
| B.该反应的ΔH<0 |
C. 温度下,起始时容器内的压强为 温度下,起始时容器内的压强为 , ,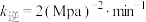 ,则该温度下 ,则该温度下 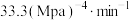 |
| D.升高温度或增大压强,都可以提高反应物的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
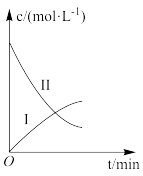
【推荐2】某实验探究小组研究320K时 的分解反应:
的分解反应: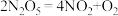 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
 的分解反应:
的分解反应: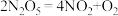 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
| t/min | 0 | 1 | 2 | 3 | 4 |
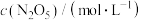 | 0.160 | 0.114 | 0.080 | 0.056 | 0.040 |
 | 0 | 0.023 | 0.040 | 0.052 | 0.060 |
A.曲线Ⅰ是 的浓度变化曲线 的浓度变化曲线 |
B.曲线Ⅱ是 的浓度变化曲线 的浓度变化曲线 |
C. 的浓度越大,反应速率越快 的浓度越大,反应速率越快 |
D. 的浓度越大,反应速率越快 的浓度越大,反应速率越快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】T°C时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见表。下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见表。下列说法正确的是
 PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见表。下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见表。下列说法正确的是| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A.反应在前50s内的平均速率为v(PCl3)=0.0032mol·L-1·s-1 |
| B.反应350s时,反应放出的Cl2的体积为4.48L |
| C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2达到平衡前: v正>v逆 |
| D.平衡时,再充入1.0molPCl5(g),平衡正向移动,K增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】工业合成氨的反应为: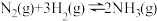 ,在
,在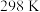 时,
时,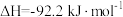 ,
,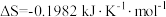 ,特定条件下的速率可表示为
,特定条件下的速率可表示为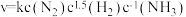 ,其中k为反应速率常数,下列叙述正确的是
,其中k为反应速率常数,下列叙述正确的是
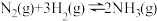 ,在
,在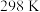 时,
时,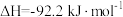 ,
,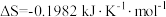 ,特定条件下的速率可表示为
,特定条件下的速率可表示为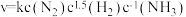 ,其中k为反应速率常数,下列叙述正确的是
,其中k为反应速率常数,下列叙述正确的是A.该反应在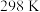 时不能正向自发进行 时不能正向自发进行 |
| B.升高温度、增大压强有利于化学平衡向生成氨的方向移动 |
C.反应体系的三种物质中, 的浓度对反应速率影响最大 的浓度对反应速率影响最大 |
D.反应达到一定转化率时将 从混合气中分离出去会降低反应速率 从混合气中分离出去会降低反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O的分解速率方程v=k·c(N2O)·c0.5(I2)(k为速率常数)。下列表述正确的是
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O的分解速率方程v=k·c(N2O)·c0.5(I2)(k为速率常数)。下列表述正确的是
| A.I2浓度与N2O分解速率无关 | B.第三步对总反应速率起决定作用 |
| C.IO为反应的中间产物 | D.第二步活化能比第三步小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列四个数据都表示反应2SO2(g)+O2(g) 2SO3(g)的正反应速率,其中反应速率相同的是
2SO3(g)的正反应速率,其中反应速率相同的是
①v(SO2)=0.3mol•L-1•min-1②v(SO3)=0.9mol•L-1•min-1③v(O2)=0.15mol•L-1•min-1④v(O2)=2.25mol•L-1•min-1
 2SO3(g)的正反应速率,其中反应速率相同的是
2SO3(g)的正反应速率,其中反应速率相同的是①v(SO2)=0.3mol•L-1•min-1②v(SO3)=0.9mol•L-1•min-1③v(O2)=0.15mol•L-1•min-1④v(O2)=2.25mol•L-1•min-1
| A.①② | B.①③ | C.③④ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上,可采用还原法处理尾气中NO,其原理:2NO(g)+2H2(g) N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
下列有关推断正确的是
 N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:| 实验 | c(NO)/mol·L-1 | c(H2)/mol·L-1 | v(正)/mol·L-1·min-1 |
| ① | 0.10 | 0.10 | 0.414k |
| ② | 0.10 | 0.40 | 1.656k |
| ③ | 0.20 | 0.10 | 1.656k |
| A.上述反应中,正反应活化能大于逆反应活化能 |
| B.若升高温度,则k(正)增大,k(逆)减小 |
| C.在上述反应中,反应级数:m=2,n=1 |
| D.在一定温度下,NO、H2的浓度对正反应速率影响程度相同 |
您最近一年使用:0次

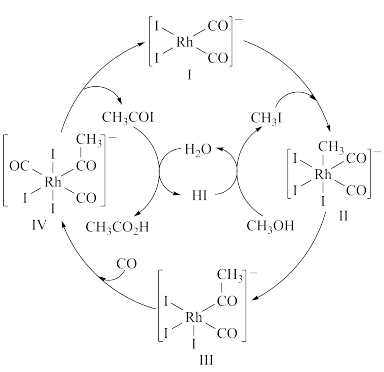
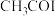 是反应中间体,
是反应中间体, 能提升催化效果
能提升催化效果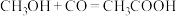
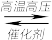 2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol/L,在该段时间内用H2表示的平均反应速率为0.45mol/(L·s)。则反应所经过的时间是(
2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol/L,在该段时间内用H2表示的平均反应速率为0.45mol/(L·s)。则反应所经过的时间是(

