回答下列问题:
(1)在一 定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+C12(g) =2HCl(g) ΔH= - 184.6 kJ•mol-1;该反应属于___________ (填“热吸”或“放热”)反应 。
(2)常温常压下,1 mol乙醇完全燃烧生成CO2气体和液态水放出的热量为1367 kJ,写出乙醇燃烧热的热化学方程式:___________
(3)根据盖斯定律计算
P4(白磷,s)+5O2(g)=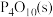 △H=-2983.2 kJ·mol-1 ①
△H=-2983.2 kJ·mol-1 ①
P(红磷,s)+ O2(g)=
O2(g)=
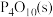 △H=-738.5 kJ·mol-1 ②
△H=-738.5 kJ·mol-1 ②
则白磷转化为红磷的热化学方程式为___________
(4)已知破坏1 mol H-H 键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ 。则由氢气和碘单质反应生成2molHI 需要放出___________ kJ 的热量。
(1)在一 定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+C12(g) =2HCl(g) ΔH= - 184.6 kJ•mol-1;该反应属于
(2)常温常压下,1 mol乙醇完全燃烧生成CO2气体和液态水放出的热量为1367 kJ,写出乙醇燃烧热的热化学方程式:
(3)根据盖斯定律计算
P4(白磷,s)+5O2(g)=
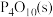 △H=-2983.2 kJ·mol-1 ①
△H=-2983.2 kJ·mol-1 ①P(红磷,s)+
 O2(g)=
O2(g)=
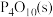 △H=-738.5 kJ·mol-1 ②
△H=-738.5 kJ·mol-1 ②则白磷转化为红磷的热化学方程式为
(4)已知破坏1 mol H-H 键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ 。则由氢气和碘单质反应生成2molHI 需要放出
更新时间:2022-03-19 19:51:05
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】化学反应的实质:旧键的断裂和新键的形成。断键___________ ,成键___________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】从微观角度理解反应热产生的原因
化学反应的本质:___________ 。
化学反应的本质:
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】从化学能的角度分析化学反应中能量变化
下图中能表示反应能量的变化,a图表示的是___________ 能量,b图表示的是___________ 能量。
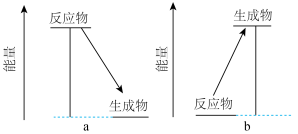
下图中能表示反应能量的变化,a图表示的是

您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】焓与焓变
(1)焓(H):是一个与内能有关的_____ 。
(2)焓变(△H):在恒压下,化学反应过程中_____ 的热量称为该反应的焓变。常用单位kJ/mol或kJ·mol-1.
(3)反应热与焓变的关系
在_____ 条件下进行的化学反应的反应热等于反应的_____ ,因此常用_____ 表示反应热。
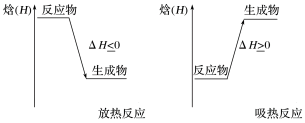
(4)焓变与吸热反应和放热反应的关系
①放热反应:反应体系向环境_____ 能量,反应体系的焓_____ ,ΔH为负值,即ΔH<0。
②吸热反应:反应体系从环境中_____ 能量,反应体系的焓_____ ,ΔH为正值,即ΔH>0。
(1)焓(H):是一个与内能有关的
(2)焓变(△H):在恒压下,化学反应过程中
(3)反应热与焓变的关系
在
(4)焓变与吸热反应和放热反应的关系
①放热反应:反应体系向环境
②吸热反应:反应体系从环境中

您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】热化学方程式概念:表示化学反应中_______ 或_______ 热的化学方程式。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】热化学方程式意义:不仅表明了化学反应中的_______ 变化,也表明了化学反应中的_______ 变化。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】CO、 SO2、NO均为大气污染物,通过下列反应可以实现可持续发展。已知:
①2CO(g)+SO2(g)=S(g)+2CO2(g)ΔH=+8.0kJ/mol-1
②2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=+90.4kJ·mol -1
③2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.5kJ·mol -1
请回答:
(1)反应①属于_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(2)反应②生成0.5mol S(g)时,ΔH=_______ kJ·mol -1。
(3)反应③消耗30g NO(g)时,ΔH=_______ kJ·mol -1。
(4)反应CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=_______ kJ·mol -1。
①2CO(g)+SO2(g)=S(g)+2CO2(g)ΔH=+8.0kJ/mol-1
②2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=+90.4kJ·mol -1
③2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.5kJ·mol -1
请回答:
(1)反应①属于
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(2)反应②生成0.5mol S(g)时,ΔH=
(3)反应③消耗30g NO(g)时,ΔH=
(4)反应CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) ΔH1=-574kJ•mol-1
CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) ΔH2=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为_______ 。
CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) ΔH1=-574kJ•mol-1
CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) ΔH2=-1160kJ•mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。已知:
2N2O5(g)=2N2O4(g)+O2(g) ΔH1=−4.4 kJ·mol−1
2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1
则反应N2O5(g)=2NO2(g)+ O2(g)的ΔH =
O2(g)的ΔH =_______ kJ·mol−1。
2N2O5(g)=2N2O4(g)+O2(g) ΔH1=−4.4 kJ·mol−1
2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1
则反应N2O5(g)=2NO2(g)+
 O2(g)的ΔH =
O2(g)的ΔH =
您最近一年使用:0次


 的
的 =
=

