回答下列问题:
(1)将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
②2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
③Zn+H2SO4=ZnSO4+H2↑
④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
⑥3Fe+2O2 Fe3O4
Fe3O4
⑦CuO+H2 Cu十H2O
Cu十H2O
属于化合反应的是_______ ,属于分解反应的是_______ ,属于复分解反应的是_______ ,属于置换反应的是_______ ,属于氧化还原反应的是_______ 。
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是_______ (填化学式)。
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是_______。(双选,漏选错选无分填字母序号)
(4)当反应2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,有1个FeO 离子生成时,转移的电子数是
离子生成时,转移的电子数是_______ 个。
(5)铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目_______ 。
(1)将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO
 3Fe+4CO2
3Fe+4CO2②2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑③Zn+H2SO4=ZnSO4+H2↑
④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O⑥3Fe+2O2
 Fe3O4
Fe3O4⑦CuO+H2
 Cu十H2O
Cu十H2O属于化合反应的是
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是_______。(双选,漏选错选无分填字母序号)
| A.Cl2+2NaOH=NaCl+NaClO+H2O |
B.4P+5O2 2P2O5 2P2O5 |
| C.Zn+CuCl2=Cu+ZnCl2 |
| D.3NO2+H2O=2HNO3+NO |
 离子生成时,转移的电子数是
离子生成时,转移的电子数是(5)铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
更新时间:2022-02-18 18:07:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填空
(1)有钠、氢、氧、硫四种元素,用其中的一种或几种元素可以组成多种物质,写出符合下列要求的化学式或化学方程式(各写一个):
①酸式盐________ ②非电解质________ ③置换反应:________ ;
(2)配平反应________  ________
________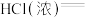 ________
________ ________
________ ________
________ ________
________ 。还原产物为
。还原产物为________ ,若有 参加反应,则参加反应的HCl为
参加反应,则参加反应的HCl为________ mol,其中被氧化的HCl为________ mol,转移电子的物质的量为________ mol
(1)有钠、氢、氧、硫四种元素,用其中的一种或几种元素可以组成多种物质,写出符合下列要求的化学式或化学方程式(各写一个):
①酸式盐
(2)配平反应
 ________
________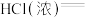 ________
________ ________
________ ________
________ ________
________ 。还原产物为
。还原产物为 参加反应,则参加反应的HCl为
参加反应,则参加反应的HCl为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】推断题善于归纳元素及其化合物之间的转化关系,对学习元素化合物具有重要意义。现有下列物质:金属铁、钠、镁、氯气、氧气、二氧化硫、二氧化碳、水、NaOH溶液、氨水、HCl溶液、KI溶液、稀HNO3、FeCl2溶液。根据要求回答问题:
(1)置换反应是中学常见基本反应类型之一。
①写出非金属单质置换出非金属单质的离子方程式___________________ 。
②写出金属单质置换出非金属单质的化学反应方程式(任写一个)_________ 。
(2)“三角转化”是上述单质及其化合物间常见的转化关系之一。现有如图转化关系:
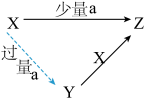
①若X是一种强碱,a是一种酸性氧化物,则Z为________ (填“化学式)。
②若Z是一种能够与血红蛋白结合造成人体缺氧的气体,则a的名称为_____ 。
③若X是常见金属单质,a为含氧酸,则Y Z的离子方程式为
Z的离子方程式为__________
请写出检验Z中金属离子的操作:____________________________
(1)置换反应是中学常见基本反应类型之一。
①写出非金属单质置换出非金属单质的离子方程式
②写出金属单质置换出非金属单质的化学反应方程式(任写一个)
(2)“三角转化”是上述单质及其化合物间常见的转化关系之一。现有如图转化关系:

①若X是一种强碱,a是一种酸性氧化物,则Z为
②若Z是一种能够与血红蛋白结合造成人体缺氧的气体,则a的名称为
③若X是常见金属单质,a为含氧酸,则Y
 Z的离子方程式为
Z的离子方程式为请写出检验Z中金属离子的操作:
您最近一年使用:0次
【推荐3】Ⅰ.写出下列反应的化学方程式:
(1)煅烧石灰石的反应___________
(2)铁单质与稀盐酸的反应___________
(3)三氧化硫与水的反应___________
(4)高温下,一氧化碳与氧化铜的反应__________
(5)氯化钡溶液与稀硫酸的反应___________
Ⅱ.请指出上述反应的反应类型:(填序号)
分解反应___________ ;化合反应___________ ;置换反应___________ ;氧化还原反应___________ ;非氧化还原反应___________ 。
(1)煅烧石灰石的反应
(2)铁单质与稀盐酸的反应
(3)三氧化硫与水的反应
(4)高温下,一氧化碳与氧化铜的反应
(5)氯化钡溶液与稀硫酸的反应
Ⅱ.请指出上述反应的反应类型:(填序号)
分解反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铬及其化合物常被应用于冶金、化工、电镀、制药等行业,但使用后的废水因其中含高价铬的化合物而毒性很强,必须进行处理。工业上往往采取下列循环工艺防止铬的污染:

(1)上述各步反应中属于氧化还原反应的是___________ (填序号)。
(2)第①步,含 的废水在酸性条件下用绿矾(FeSO4·7H2O)处理,写出并配平反应的离子方程式:
的废水在酸性条件下用绿矾(FeSO4·7H2O)处理,写出并配平反应的离子方程式:___________ 。
(3)第②步,向(2)中反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH)3沉淀。处理后沉淀物中除了Cr(OH)3外,还有___________ 、___________ (写化学式)。
(4)回收所得的Cr(OH)3,经③④⑤步处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于测定与检测,例如K2Cr2O7可用于酒驾中的酒精检测,检验酒精时,溶液由橙红色变成灰绿色。已知在该反应过程中,乙醇CH3CH2OH被氧化成醋酸CH3COOH,则氧化剂与还原剂的个数比为___________ 。
(5)铬能缓慢溶于稀盐酸生成蓝色溶液,与空气接触很快变成绿色,这是因为先生成蓝色的Cr2+,被空气中的氧进一步氧化成绿色的Cr3+的缘故。CrCl2固体在保存时应注意的重要问题是___________ ,写出上述变绿过程的化学方程式___________ 。

(1)上述各步反应中属于氧化还原反应的是
(2)第①步,含
 的废水在酸性条件下用绿矾(FeSO4·7H2O)处理,写出并配平反应的离子方程式:
的废水在酸性条件下用绿矾(FeSO4·7H2O)处理,写出并配平反应的离子方程式:(3)第②步,向(2)中反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH)3沉淀。处理后沉淀物中除了Cr(OH)3外,还有
(4)回收所得的Cr(OH)3,经③④⑤步处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于测定与检测,例如K2Cr2O7可用于酒驾中的酒精检测,检验酒精时,溶液由橙红色变成灰绿色。已知在该反应过程中,乙醇CH3CH2OH被氧化成醋酸CH3COOH,则氧化剂与还原剂的个数比为
(5)铬能缓慢溶于稀盐酸生成蓝色溶液,与空气接触很快变成绿色,这是因为先生成蓝色的Cr2+,被空气中的氧进一步氧化成绿色的Cr3+的缘故。CrCl2固体在保存时应注意的重要问题是
您最近一年使用:0次
【推荐2】过氧化氢被称为绿色氧化剂,在实验、医疗、化工、生产工艺等方面有广泛的应用,请回答下列有关H2O2的问题:
(1)H2O2中O的化合价为_______ 价,具有_______ (填“氧化性”或“还原性”或“氧化性和还原性”)。
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是:_______H2O2 +_______KMnO4 +_______H2SO4= _______+_______MnSO4 +_______O2↑ +_______H2O
已知:稀 溶液几乎无色。
溶液几乎无色。
①请将上述化学方程式配平;___________
②上述反应中的还原剂为_______ (填化学式),被还原的元素是_______ (填元素符号)。
③向酸性 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是_______ ,反应后溶液的pH_______ (填“增大”“减小”或“不变”)。
④0.3mol 参加上述反应,转移电子
参加上述反应,转移电子_______ mol。
(3)酸性条件下,在FeCl3和FeCl2的混合溶液中加入H2O2以除去Fe2+,反应的离子方程式_______ 。
(4)H2O2可用于SO2的尾气处理,请写出反应的化学方程式_______ 。
(1)H2O2中O的化合价为
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是:_______H2O2 +_______KMnO4 +_______H2SO4= _______+_______MnSO4 +_______O2↑ +_______H2O
已知:稀
 溶液几乎无色。
溶液几乎无色。①请将上述化学方程式配平;
②上述反应中的还原剂为
③向酸性
 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是④0.3mol
 参加上述反应,转移电子
参加上述反应,转移电子(3)酸性条件下,在FeCl3和FeCl2的混合溶液中加入H2O2以除去Fe2+,反应的离子方程式
(4)H2O2可用于SO2的尾气处理,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.煤炭中的硫以 的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
① ;
;
②_______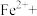 _______
_______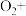 _______H+
_______H+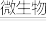 _______
_______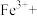 _______;
_______;
③ ;
;
④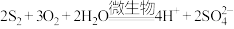 。
。
已知: 中的硫元素为-1价。
中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②的离子方程式配平并补充完整________ 。
(2)反应③中的还原剂是_______ 。
(3)观察上述反应,硫元素最终转化为_______ 从煤炭中分离出来。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化培烧的化学反应为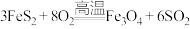 、
、 。若
。若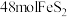 完全反应耗用氧气2934.4L(标准状况),则反应产物中
完全反应耗用氧气2934.4L(标准状况),则反应产物中 与
与 的物质的量之比为
的物质的量之比为_______ 。
Ⅱ.高炉炼铁是冶炼铁的主要方法。
(5)高炉炼铁的尾气中通常含有较多的 气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收
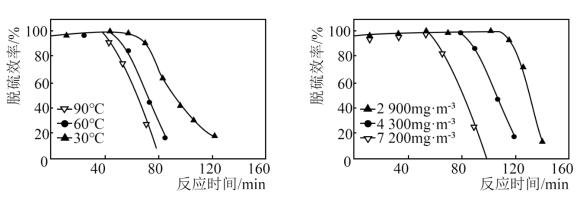
气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收 气体,脱硫效率、尾气中
气体,脱硫效率、尾气中 的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是
的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是_______ ℃;选择合适的质量浓度,经测定40min内共处理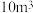 废气,则40min内平均脱硫速率为
废气,则40min内平均脱硫速率为_______ 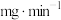 。
。
Ⅲ.完成下列问题
(6)工业上用黄铜矿( )冶炼铜,副产品中也有
)冶炼铜,副产品中也有 ,冶炼铜的化学反应为
,冶炼铜的化学反应为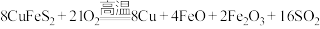 。当
。当 中Fe的化合价为+2价,反应中被还原的元素是
中Fe的化合价为+2价,反应中被还原的元素是_______ (填元素符号)。当生成0.8mol铜时,该反应转移的电子数是_______ 。
 的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为
的形式存在,在有水和空气及脱硫微生物存在的条件下发生氧化还原反应,有关反应的离子方程式依次为①
 ;
;②_______
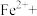 _______
_______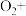 _______H+
_______H+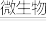 _______
_______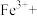 _______;
_______;③
 ;
;④
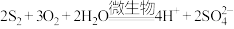 。
。已知:
 中的硫元素为-1价。
中的硫元素为-1价。回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②的离子方程式配平并补充完整
(2)反应③中的还原剂是
(3)观察上述反应,硫元素最终转化为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化培烧的化学反应为
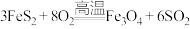 、
、 。若
。若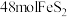 完全反应耗用氧气2934.4L(标准状况),则反应产物中
完全反应耗用氧气2934.4L(标准状况),则反应产物中 与
与 的物质的量之比为
的物质的量之比为Ⅱ.高炉炼铁是冶炼铁的主要方法。
(5)高炉炼铁的尾气中通常含有较多的
 气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收
气体。为减少污染,分离并回收气体,工业上用碱性工业废渣吸收 气体,脱硫效率、尾气中
气体,脱硫效率、尾气中 的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是
的质量浓度和温度的关系如图所示。依据图中数据分析,脱硫合适的温度是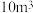 废气,则40min内平均脱硫速率为
废气,则40min内平均脱硫速率为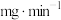 。
。
Ⅲ.完成下列问题
(6)工业上用黄铜矿(
 )冶炼铜,副产品中也有
)冶炼铜,副产品中也有 ,冶炼铜的化学反应为
,冶炼铜的化学反应为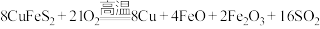 。当
。当 中Fe的化合价为+2价,反应中被还原的元素是
中Fe的化合价为+2价,反应中被还原的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
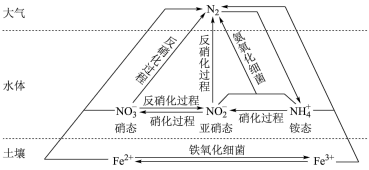
【推荐1】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
②检验氨态氮肥中 的实验方案是
的实验方案是_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为_______ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:_______ 、_______ 。
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中氨态氮的主要来源之一、
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
②检验氨态氮肥中
 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生
 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮和硝态氮的原理:
您最近一年使用:0次
【推荐2】回答下列问题:
(1)配平下列反应,并用双线桥标明电子转移方向和数目_______ 。
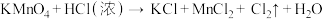
(2) 是一种新的消毒剂,工业上可用
是一种新的消毒剂,工业上可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
(3)二氧化氯( )是国际上公认的高效、安全的杀菌消毒剂。工业上制备
)是国际上公认的高效、安全的杀菌消毒剂。工业上制备 的反应原理常采用:
的反应原理常采用: 。
。
①浓盐酸在反应中显示出来的性质是_______ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ,则转移电子数约为
,则转移电子数约为_______ 。
(1)配平下列反应,并用双线桥标明电子转移方向和数目
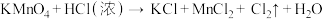
(2)
 是一种新的消毒剂,工业上可用
是一种新的消毒剂,工业上可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的化学方程式
,写出该反应的化学方程式(3)二氧化氯(
 )是国际上公认的高效、安全的杀菌消毒剂。工业上制备
)是国际上公认的高效、安全的杀菌消毒剂。工业上制备 的反应原理常采用:
的反应原理常采用: 。
。①浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol
 ,则转移电子数约为
,则转移电子数约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿 是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为
是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为 ,若有
,若有 参加反应,则转移
参加反应,则转移_______  电子。
电子。
(2)细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
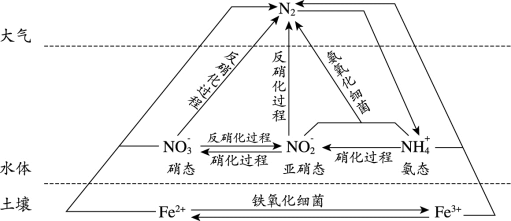
①如图所示氮循环中,属于氮的固定的有_______ (填字母序号)。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
②硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
③氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为_______  。
。
④土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理_______ 。(注:土壤中的铁循环脱除水体中氨态氮产生 )
)
(1)黄铁矿
 是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为
是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为 ,若有
,若有 参加反应,则转移
参加反应,则转移 电子。
电子。(2)细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。

①如图所示氮循环中,属于氮的固定的有
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程②硝化过程中,含氮物质发生
③氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生
 氮气时,转移的电子的物质的量为
氮气时,转移的电子的物质的量为 。
。④土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理
 )
)
您最近一年使用:0次



