通过电氧化合成法可制得特殊高价金属化合物高铜酸钠(化学式为NaCuO2)。关于该物质的推测,下列有关说法不正确的是
A. 具有强氧化性,是因为存在过氧根离子 具有强氧化性,是因为存在过氧根离子 |
B. 与浓盐酸作用会产生有刺激性气味的气体 与浓盐酸作用会产生有刺激性气味的气体 |
| C.该物质在酸性条件下不能稳定存在 |
D. 与氢气反应可能有紫红色固体生成 与氢气反应可能有紫红色固体生成 |
更新时间:2022-03-13 09:55:52
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列化学反应中,水作为还原剂的是
| A.CO+H2O高温CO2+H2 |
| B.3NO2+H2O=2HNO3+NO |
| C.CO2+H2O=H2CO3 |
| D.2F2+2H2O=4HF+O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】KNO3具有强氧化性,可发生反应:2KNO3+2NH4Cl 2KCl+2N2↑+O2↑+4H2O。下列说法
2KCl+2N2↑+O2↑+4H2O。下列说法不正确 的是(NA为阿伏加德罗常数的值)
 2KCl+2N2↑+O2↑+4H2O。下列说法
2KCl+2N2↑+O2↑+4H2O。下列说法| A.N2既是氧化产物,又是还原产物 |
| B.KNO3仅作氧化剂 |
| C.生成1molN2转移电子的数目为5NA |
| D.实验室不可用加热NH4NO3固体的方法制备NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下可用Co2O3为原料制备Cl2,反应前后总共存在六种微粒:Co2O3、H2O、Cl2、H+、Cl-和Co2+。下列有关该反应的叙述正确的是
| A.氧化产物为Cl2 | B.还原产物为Cl2 | C.还原产物为Cl- | D.氧化剂为Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知高铁酸钾能溶于水,微溶于浓KOH溶液,且能与水反应放出氧气。高铁酸钾有强氧化性,酸性条件下其氧化性更强,强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如图:

下列说法正确的是

下列说法正确的是
| A.“反应”时,氧化剂为Fe(NO3)3 |
| B.将K2FeO4与盐酸混合使用,可增强其杀菌消毒效果 |
| C.“转化”时,反应能进行的原因是该条件下K2FeO4的溶解度小于Na2FeO4 |
D.“过滤Ⅰ”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO 、FeO 、FeO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氰 ,硫氰
,硫氰 等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为:
等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: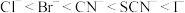 ,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是( )
,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是( )
 ,硫氰
,硫氰 等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为:
等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: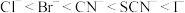 ,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是( )
,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是( )A. 浓 浓   |
B. |
C. |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将氯水逐滴滴入淀粉 KI溶液中至过量,溶液由无色变为蓝色又逐渐变为无色,由此能得出的结论是
| A.I- 被氧化为I2 | B.I2被氧化为 |
| C.氯水有漂白性 | D.HClO氧化I2为 |
您最近一年使用:0次

 (N为-2价),火箭升空时发生的化学反应为:
(N为-2价),火箭升空时发生的化学反应为: 。下列有关说法正确的是
。下列有关说法正确的是 ,下列说法正确的是
,下列说法正确的是

