目前,能较稳定存在的氯的氧化物有 、
、 、
、 等。有关数据见表:请回答下列问题:
等。有关数据见表:请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是_______ 。
(2) 属于酸性氧化物,它与水反应的离子方程式为
属于酸性氧化物,它与水反应的离子方程式为_______ 。
(3) 是一种常用的消毒剂,我国从2000年起逐步用
是一种常用的消毒剂,我国从2000年起逐步用 代替氯气对饮用水进行消毒。在消毒水时,
代替氯气对饮用水进行消毒。在消毒水时, 还可将水中的
还可将水中的 、
、 等转化成
等转化成 和
和 等难溶物除去,说明
等难溶物除去,说明 具有
具有_______ 性,试写出用 (
( 反应后的产物为
反应后的产物为 )氧化除去
)氧化除去 生成
生成 的离子方程式:
的离子方程式:_______ 。
(4)工业上可以用下列反应制备 :
: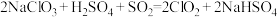 ,请用单线桥法表示出该反应电子转移的方向和数目
,请用单线桥法表示出该反应电子转移的方向和数目_______ 。
(5)工业上也可以用制备 的反应原理为:
的反应原理为: (浓)
(浓)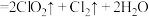
 。
。
①浓盐酸在反应中显示出来的性质是_______ (填序号)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生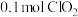 ,则转移的电子数为
,则转移的电子数为_______ 。
 、
、 、
、 等。有关数据见表:请回答下列问题:
等。有关数据见表:请回答下列问题:| 化学式 |  |  |  |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
(1)常温、常压下,三种氧化物中属于气体的是
(2)
 属于酸性氧化物,它与水反应的离子方程式为
属于酸性氧化物,它与水反应的离子方程式为(3)
 是一种常用的消毒剂,我国从2000年起逐步用
是一种常用的消毒剂,我国从2000年起逐步用 代替氯气对饮用水进行消毒。在消毒水时,
代替氯气对饮用水进行消毒。在消毒水时, 还可将水中的
还可将水中的 、
、 等转化成
等转化成 和
和 等难溶物除去,说明
等难溶物除去,说明 具有
具有 (
( 反应后的产物为
反应后的产物为 )氧化除去
)氧化除去 生成
生成 的离子方程式:
的离子方程式:(4)工业上可以用下列反应制备
 :
: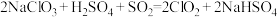 ,请用单线桥法表示出该反应电子转移的方向和数目
,请用单线桥法表示出该反应电子转移的方向和数目(5)工业上也可以用制备
 的反应原理为:
的反应原理为: (浓)
(浓)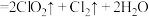
 。
。①浓盐酸在反应中显示出来的性质是
A.还原性 B.氧化性 C.酸性
②若上述反应中产生
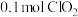 ,则转移的电子数为
,则转移的电子数为
更新时间:2022-03-13 15:22:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】判断下列离子方程式是否正确(填“对”或“错”),并将错误的离子方程式修改正确。
(1)铁粉溶于稀硫酸:2Fe2++6H+=2Fe3++H2 ↑_________ ,_____________________ 。
(2)用饱和氯化铁溶液制备氢氧化铁胶体:Fe3++3OH-=Fe(OH)3↓_________ ,_________________ 。
(3)氧化钙溶于盐酸反应:CaO+2H+=Ca2++H2O_________ ,____________________ 。
(4)BaCO3与稀硫酸反应:Ba2++ =BaSO4↓
=BaSO4↓_________ ,___________________ 。
(5)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-= Mg(OH)2↓_________ ,__________________ 。
(6)硝酸钙溶液和碳酸钾溶液混合:Ca2++ =CaCO3↓
=CaCO3↓_________ ,_________________ 。
(1)铁粉溶于稀硫酸:2Fe2++6H+=2Fe3++H2 ↑
(2)用饱和氯化铁溶液制备氢氧化铁胶体:Fe3++3OH-=Fe(OH)3↓
(3)氧化钙溶于盐酸反应:CaO+2H+=Ca2++H2O
(4)BaCO3与稀硫酸反应:Ba2++
 =BaSO4↓
=BaSO4↓(5)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-= Mg(OH)2↓
(6)硝酸钙溶液和碳酸钾溶液混合:Ca2++
 =CaCO3↓
=CaCO3↓
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高纯砷(As)常用于制造砷化镓、砷化锗等半导体材料。工业上用含砷废料(主要成分为 ,含少量
,含少量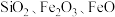 )为原料制取高纯砷的工艺流程(硫化—还原法)如下图所示:
)为原料制取高纯砷的工艺流程(硫化—还原法)如下图所示:
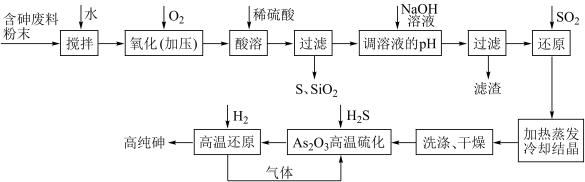
已知:砷酸(H3AsO4)在酸性条件下有强氧化性,能被 、氢碘酸等还原为亚砷酸(H3AsO3),H3AsO3在加热蒸发过程中会失水生成
、氢碘酸等还原为亚砷酸(H3AsO3),H3AsO3在加热蒸发过程中会失水生成 。
。 时
时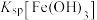 的值为
的值为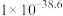 。
。
回答下列问题:
(1)半导体材料 中
中 元素的化合价为
元素的化合价为___ ,“氧化(加压)”时 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)“还原”过程发生反应的离子方程式为___ 。
 ,含少量
,含少量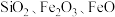 )为原料制取高纯砷的工艺流程(硫化—还原法)如下图所示:
)为原料制取高纯砷的工艺流程(硫化—还原法)如下图所示:
已知:砷酸(H3AsO4)在酸性条件下有强氧化性,能被
 、氢碘酸等还原为亚砷酸(H3AsO3),H3AsO3在加热蒸发过程中会失水生成
、氢碘酸等还原为亚砷酸(H3AsO3),H3AsO3在加热蒸发过程中会失水生成 。
。 时
时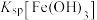 的值为
的值为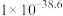 。
。回答下列问题:
(1)半导体材料
 中
中 元素的化合价为
元素的化合价为 发生反应的化学方程式为
发生反应的化学方程式为(2)“还原”过程发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硼单质在高温时是良好的导体,也是用途广泛的化工原料。镁单质可用于制造轻金属合金、球墨铸铁等。硼镁矿的主要成分为Mg2B2O5·H2O,可以制取单质硼和镁。制取工艺流程如图所示,已知硼砂的化学式为Na2B4O7·10H2O,硼镁泥是硼镁矿制硼砂过程中产生的废渣,其主要成分是MgCO3,还含有CaO、Al2O3、Fe2O3、FeO、MnO、SiO2等杂质。按要求回答问题:

(1)化合物Mg2B2O5·H2O中B的化合价为_____ 。
(2)将硼砂溶于热水后,常用稀硫酸调pH至2~3制取H3BO3,该反应的离子方程式为____ 。
(3)写出加NaClO的过程中发生反应的离子方程式:________ ;________ 。
(4)将硼镁泥中加入的硫酸改为盐酸是否可行?___ 。(填“是”或“否”),理由是____ 。

(1)化合物Mg2B2O5·H2O中B的化合价为
(2)将硼砂溶于热水后,常用稀硫酸调pH至2~3制取H3BO3,该反应的离子方程式为
(3)写出加NaClO的过程中发生反应的离子方程式:
(4)将硼镁泥中加入的硫酸改为盐酸是否可行?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质一碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式: 。
。
请回答下列问题:
①此反应的氧化剂是___________ ,氧化产物是___________ 。
② 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是___________ (填选项序号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
已知碳与浓硫酸在加热条件下反应生成 、
、 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:
①上述反应中,被氧化的元素___________ ,还原产物是___________ 。
②用双线桥法表示反应中电子转移的方向和数目:___________ 。
③请配平下列离子方程式:



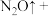
 ,
,___________ 。
(3)写出下列反应的离子方程式:
①用食醋除去水垢(水垢的主要成分为碳酸钙)___________ 。
②氢氧化铁溶于稀硫酸___________ 。
③硫酸铝溶液中加入氨水___________ 。
④钠与水的反应___________ 。
⑤在碱性条件下, 可将废水中的
可将废水中的 ,氧化为无毒的
,氧化为无毒的 、
、
___________ 。
(1)储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质一碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式:
 。
。请回答下列问题:
①此反应的氧化剂是
②
 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是A.酸性 B.氧化性 C.吸水性 D.脱水性
已知碳与浓硫酸在加热条件下反应生成
 、
、 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:①上述反应中,被氧化的元素
②用双线桥法表示反应中电子转移的方向和数目:
③请配平下列离子方程式:




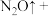
 ,
,(3)写出下列反应的离子方程式:
①用食醋除去水垢(水垢的主要成分为碳酸钙)
②氢氧化铁溶于稀硫酸
③硫酸铝溶液中加入氨水
④钠与水的反应
⑤在碱性条件下,
 可将废水中的
可将废水中的 ,氧化为无毒的
,氧化为无毒的 、
、
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分析下列氧化还原反应,用单线桥标出电子转移的方向和数目,并指出氧化剂、还原剂,氧化产物、还原产物。
(1) ,
,____________ ,氧化剂___________ ,氧化产物___________ 。
(2)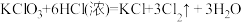 ,
,____________ ,还原剂___________ ,还原产物___________ 。
(3) ,
,____________ ,氧化剂___________ ,还原产物___________ 。
(1)
 ,
,(2)
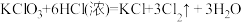 ,
,(3)
 ,
,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】储氢碳纳米管的成功研制体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
(1)请用上述物质填空,并配平化学方程式□C+□( )+□H2SO4=□( )+□( )+□Cr2(SO4)3+□H2O:_______________ 。
(2)上述反应中氧化剂是______ (填化学式),被氧化的元素是______ (填元素符号)。
(3) H2SO4在上述反应中表现的性质是______ (填字母)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(1)请用上述物质填空,并配平化学方程式□C+□( )+□H2SO4=□( )+□( )+□Cr2(SO4)3+□H2O:
(2)上述反应中氧化剂是
(3) H2SO4在上述反应中表现的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车安全气囊中填充物有NaN3(叠氮酸钠)、SiO2、KNO3等物质。
(1)汽车安全气囊填充物所涉及的5种元素中,原子半径最小的元素在元素周期表中的位置___________ 。
(2)当汽车受到猛烈碰撞时,瞬间引发反应:2NaN3=2Na+3N2↑,同时释放大量的热。NaN3为离子化合物,下列说法正确的是_________
(3)SiO2、KNO3能与金属钠发生反应生成Na2SiO3,配平下列化学方程式,并标出电子转移的方向和数目:_________
___________Na+___________KNO3+___________SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑
(4)某品牌汽车设计安全气囊受撞击时需产生35.84L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是___________ 。
(5)销毁NaN3可用NaClO溶液,反应生成对环境无害的气体,该销毁反应的离子方程式为___________ 。
(1)汽车安全气囊填充物所涉及的5种元素中,原子半径最小的元素在元素周期表中的位置
(2)当汽车受到猛烈碰撞时,瞬间引发反应:2NaN3=2Na+3N2↑,同时释放大量的热。NaN3为离子化合物,下列说法正确的是_________
| A.生成3mol N2时,转移2mol电子 |
| B.1个N3-中含有21个电子 |
| C.NaN3中只含离子键 |
D.N2的电子式为 |
(3)SiO2、KNO3能与金属钠发生反应生成Na2SiO3,配平下列化学方程式,并标出电子转移的方向和数目:
___________Na+___________KNO3+___________SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑
(4)某品牌汽车设计安全气囊受撞击时需产生35.84L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是
(5)销毁NaN3可用NaClO溶液,反应生成对环境无害的气体,该销毁反应的离子方程式为
您最近一年使用:0次
【推荐2】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)被氧化的元素是_____ ,被还原的元素是____________ ,氧化产物____________ ,还原产物____________ 。
(2)用双线桥法表示反应电子转移的方向和数目:________ 。
(3)用单线桥法表示反应电子转移的方向和数目:___________ 。
(1)被氧化的元素是
(2)用双线桥法表示反应电子转移的方向和数目:
(3)用单线桥法表示反应电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】膏是常见的日用化学品。磨擦剂是牙膏的主体原料,一般占配方的20%~50%,在牙膏中最重要的作用就是去除牙垢,减轻牙结石。
(1)下表列出了两种牙膏中的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(2)请根据用途推测二水磷酸氢钙(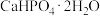 )的化学性质
)的化学性质___________ (填“活泼”或“稳定”)
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备,甲、乙两同学设计了不同的实验方案,按要求回答下列问题。
甲同学:
乙同学:
①乙同学设计的方案中属于电解质的物质是___________ (填字母)。
A.石灰石B.稀盐酸C.氯化钙D. 溶液E.碳酸钙
溶液E.碳酸钙
②乙同学设计的方案中第一步发生的反应是(写离子反应方程式)___________ 。
③若实际生产的过程中使用的 溶液的物质的量浓度是3mol/L,此时溶液中c(Na+)=
溶液的物质的量浓度是3mol/L,此时溶液中c(Na+)=___________ ;若取该溶液10mL,加水稀释至200mL,稀释后c(CO )
)____________ 。
(4)溶解石灰石的稀盐酸遇到 时,发生反应:
时,发生反应: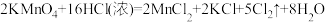 ,该反应中氧化剂和还原剂物质的量之比是
,该反应中氧化剂和还原剂物质的量之比是___________ ,氧化产物是___________ (填化学式),用单线桥法表示该反应电子转移___________ 。
(5)甲、乙两同学的方案中,你认为更为合理的是___________ ,理由:___________ (写两条)。
(1)下表列出了两种牙膏中的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
| 摩擦剂成分 | 氢氧化铝 | 二水磷酸氢钙(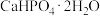 ) ) | 碳酸钙 | 二氧化硅 |
| 物质类别 |
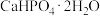 )的化学性质
)的化学性质(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备,甲、乙两同学设计了不同的实验方案,按要求回答下列问题。
甲同学:

乙同学:

①乙同学设计的方案中属于电解质的物质是
A.石灰石B.稀盐酸C.氯化钙D.
 溶液E.碳酸钙
溶液E.碳酸钙②乙同学设计的方案中第一步发生的反应是(写离子反应方程式)
③若实际生产的过程中使用的
 溶液的物质的量浓度是3mol/L,此时溶液中c(Na+)=
溶液的物质的量浓度是3mol/L,此时溶液中c(Na+)= )
)(4)溶解石灰石的稀盐酸遇到
 时,发生反应:
时,发生反应: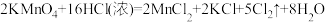 ,该反应中氧化剂和还原剂物质的量之比是
,该反应中氧化剂和还原剂物质的量之比是(5)甲、乙两同学的方案中,你认为更为合理的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答以下问题:
(1)下列描述的分别是胶体的性质或现象,按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔现象 D.胶体的稳定性
①用激光鉴别胶体和溶液,利用的胶体性质是____ (填字母)。
②工厂采用高压静电除尘,利用的胶体性质是_____ (填字母)。
(2)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,是一元弱酸,NaH2PO2属于____ (正盐、酸式盐、碱式盐),写出NaH2PO2的电离方程式____ 。
(3)已知:氧化性Cl2>Fe3+>I2,请写出过量Cl2通入到FeI2溶液中的化学方程式____ 。
(1)下列描述的分别是胶体的性质或现象,按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔现象 D.胶体的稳定性
①用激光鉴别胶体和溶液,利用的胶体性质是
②工厂采用高压静电除尘,利用的胶体性质是
(2)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,是一元弱酸,NaH2PO2属于
(3)已知:氧化性Cl2>Fe3+>I2,请写出过量Cl2通入到FeI2溶液中的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用广谱高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。
(1)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:_________________________ 。
(2)漂白剂亚氯酸钠(NaClO2)在常温黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1molHClO2发生分解反应时,转移的电子个数是_______ 。
(3)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是________ 。
(1)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:
(2)漂白剂亚氯酸钠(NaClO2)在常温黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1molHClO2发生分解反应时,转移的电子个数是
(3)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)在Al、Fe2+、H+、S2-、SO2五种微粒中,只有氧化性的是_________ ,只有还原性的是______________ 既有氧化性又有还原性的是______________ 。
(2)有下列反应:Fe+Cu2+=Fe2++Cu;2Fe3++Cu=2Fe2++Cu2+;在Cu2+、Fe2+、Fe3+中,其氧化性由强到弱顺序为_______________ 。
(3)根据反应MnO2+4HCl MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
①还原产物是____________
②该反应中盐酸的作用是________________ (填字母)
A.只氧化性B.只有酸性C.只有还原性 D.有氧化性也有酸性E.有还原性也有酸性
③ 用单线桥(或者双线桥)表示上述反应电子转移的方向和数目_______________
MnO2+ 4HCl=MnCl2+Cl2↑+2H2O
④该反应中氧化剂与还原剂物质的量之比为____________ 。
⑤如果该反应转移电子lmol,则生成标准状况下的气体体积为__________ L
(2)有下列反应:Fe+Cu2+=Fe2++Cu;2Fe3++Cu=2Fe2++Cu2+;在Cu2+、Fe2+、Fe3+中,其氧化性由强到弱顺序为
(3)根据反应MnO2+4HCl
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:①还原产物是
②该反应中盐酸的作用是
A.只氧化性B.只有酸性C.只有还原性 D.有氧化性也有酸性E.有还原性也有酸性
③ 用单线桥(或者双线桥)表示上述反应电子转移的方向和数目
MnO2+ 4HCl=MnCl2+Cl2↑+2H2O
④该反应中氧化剂与还原剂物质的量之比为
⑤如果该反应转移电子lmol,则生成标准状况下的气体体积为
您最近一年使用:0次



