某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置Ⅰ中仪器c的名称是___________ 。写出舍勒发现的,至今仍应用于实验室制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
① ②
②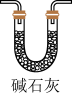 ③
③ ④
④ 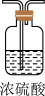
(5)有一种“地康法”制取氯气的反应原理如图所示:
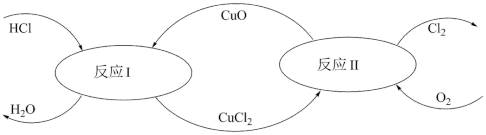
①反应Ⅰ属于___________ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为___________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④ 
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
更新时间:2022-03-14 23:38:47
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
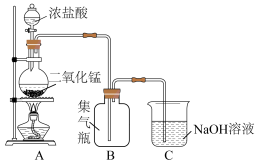
【推荐1】某中学化学兴趣小组同学用如图所示的装置研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
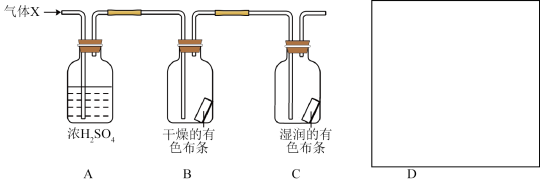
(1)该实验的主要目的是_________________________________________________________________ 。
(2)浓 的作用是
的作用是__________________________________________________________________ ,与实验目的直接相关的实验现象是B中________________________________________________ ;C中________________________________________________ 。
(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,还需在图所示的D处增加盛有__________________ (填试剂名称)的尾气处理装置。

(1)该实验的主要目的是
(2)浓
 的作用是
的作用是(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,还需在图所示的D处增加盛有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】现有X、Y、Z三种属于元素周期表前18种的元素,X的单质可以在Z的单质中燃烧,生成XZ,燃烧时火焰为苍白色;X的单质也可以与Y的单质化合,生成常温下为液体的X2Y;Z的单质溶于X2Y中,生成一种含X、Y、Z三种元素的物质,具有强氧化性,可用于自来水的消毒。根据以上信息,完成下列问题:
(1)画出Z的原子结构示意图___ 。
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为___ 。
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式___ ;若生成11.2L(标准状况)的Y的单质,则转移的电子的物质的量为___ 。
(4)试写出Z的单质溶于X2Y中反应的离子方程式___ 。
(5)XYZ在光照条件下不稳定,原因是___ (用化学方程式表示)。
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于___ 。
(1)画出Z的原子结构示意图
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式
(4)试写出Z的单质溶于X2Y中反应的离子方程式
(5)XYZ在光照条件下不稳定,原因是
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】氯水能使干燥的红色布条褪色.对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种成分都有可能.请你设计实验,得出正确结论。
(1)提出假设
假设一:H2O使红色布条褪色。
假设二:__________________________ 。
假设三:__________________________ 。
假设四:HCl使红色布条褪色。
(2)设计实验方案。基于提出的假设,设计出实验方案(不需要作答)。
(3)实验过程。
实验1:将红色布条放在水里,布条不褪色。
实验II:__________________________________ 。
实验Ⅲ:__________________________________ 。
(4)得出结论:__________________________________ 。
(1)提出假设
假设一:H2O使红色布条褪色。
假设二:
假设三:
假设四:HCl使红色布条褪色。
(2)设计实验方案。基于提出的假设,设计出实验方案(不需要作答)。
(3)实验过程。
实验1:将红色布条放在水里,布条不褪色。
实验II:
实验Ⅲ:
(4)得出结论:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学实验小组为了探究在实验室制备 的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置。
的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置。

资料1:氯气易溶于 ,HCl不溶于
,HCl不溶于
资料2:
请回答下列问题:
(1)装置A中连接橡皮管的目的是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。
(3)装置B中盛放的试剂是___________ 。
(4)装置D与E中出现的不同现象说明的问题是___________ 。
(5)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉-KI试纸的装置,其目的是________ 。
 的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置。
的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置。
资料1:氯气易溶于
 ,HCl不溶于
,HCl不溶于
资料2:

请回答下列问题:
(1)装置A中连接橡皮管的目的是
(2)装置A中发生反应的离子方程式为
(3)装置B中盛放的试剂是
(4)装置D与E中出现的不同现象说明的问题是
(5)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉-KI试纸的装置,其目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】含氯消毒剂、医用酒精、过氧化物等均能有效灭活病毒,为抗击新型冠状肺炎(COVID-19)作出了贡献。请回答下列问题:
(1)下列物质用作消毒剂时,原理与其它不同的是___________ (填字母)。
A.NaClO B.ClO2 C.医用酒精 D.H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作:取少量样品,溶解,加入___________ ,振荡,有白色沉淀产生,证明Na2O2已变质。
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是___________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为___________ 。
(4)兴趣小组设计如下图实验装置制取少量漂白液

①MnO2与浓盐酸反应的离子方程式为___________ 。
②充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有:
I.___________ (用文字简述)。
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为___________ 。
(1)下列物质用作消毒剂时,原理与其它不同的是
A.NaClO B.ClO2 C.医用酒精 D.H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作:取少量样品,溶解,加入
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(4)兴趣小组设计如下图实验装置制取少量漂白液

①MnO2与浓盐酸反应的离子方程式为
②充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有:
I.
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】瑞典化学家舍勒是最早发现氯气的人,他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气,装置如图所示,化学反应方程式为: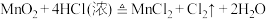
回答下列问题:
(1)实验室制取 的反应中,浓盐酸表现
的反应中,浓盐酸表现_________ (填“氧化性”、“还原性”或“酸性”)。
(2)请用单线桥表示该反应中电子转移的方向和数目_________ 。
(3)标况下,若生成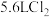 ,则转移电子的数目为
,则转移电子的数目为_________ 。
(4)装置C可吸收多余的 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式_________ 。所用 溶液一般为
溶液一般为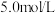 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、_________ 。
(5) 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是_________ 。
(6)装置C中也可能生成 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式_________ 。
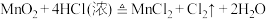

回答下列问题:
(1)实验室制取
 的反应中,浓盐酸表现
的反应中,浓盐酸表现(2)请用单线桥表示该反应中电子转移的方向和数目
(3)标况下,若生成
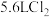 ,则转移电子的数目为
,则转移电子的数目为(4)装置C可吸收多余的
 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式 溶液一般为
溶液一般为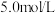 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、(5)
 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是(6)装置C中也可能生成
 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某研究小组为了制备“84消毒液”(主要成分为NaClO)设计了如图装置。查阅到下列资料:“卤素与水的反应是放热反应,在加热情况下卤素与碱液发生如下反应:3X2+6OH- 5X-+
5X-+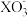 +3H2O”。
+3H2O”。

回答下列问题:
(1)装置中的圆底烧瓶内发生反应的化学方程式为_______ 。
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?_______ (填“能”或“不能”,下同),理由是_______ 。
(3)装置中能否省去盛浓硫酸的洗气瓶?_______ ,理由是_______ 。
(4)装置中能否省去盛冰水的烧杯?_______ ,理由是_______ 。
 5X-+
5X-+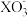 +3H2O”。
+3H2O”。
回答下列问题:
(1)装置中的圆底烧瓶内发生反应的化学方程式为
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?
(3)装置中能否省去盛浓硫酸的洗气瓶?
(4)装置中能否省去盛冰水的烧杯?
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应生成的白色沉淀可用于制备MgAl2O4,主要流程如图1所示:


(1)如图2所示,过滤操作中的一处错误是___________ 。
(2)高温焙烧时,用于盛放固体的仪器名称是___________ 。
(3)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
已知:实验室用MnO2固体和浓盐酸加热制氯气的原理为MnO2+4HCl MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。

①装置B中盛放饱和NaCl溶液,该装置的主要作用是___________ 。
②F中试剂是浓硫酸,若用一件仪器装填适当试剂后也可起到F和G的作用,则该仪器及所装填的试剂为___________ 。
③装置E的作用是___________ 。
(4)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式___________ 。


(1)如图2所示,过滤操作中的一处错误是
(2)高温焙烧时,用于盛放固体的仪器名称是
(3)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
已知:实验室用MnO2固体和浓盐酸加热制氯气的原理为MnO2+4HCl
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
①装置B中盛放饱和NaCl溶液,该装置的主要作用是
②F中试剂是浓硫酸,若用一件仪器装填适当试剂后也可起到F和G的作用,则该仪器及所装填的试剂为
③装置E的作用是
(4)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
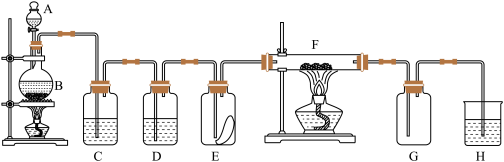
【推荐3】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。___________ 。
(2)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(3)E中红色布条是否褪色?___________ (填“是”或“否”),F中的反应产物为___________ 。
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式___________ ,___________ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)___________ 。
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组用Fe3+与I-间的反应探究氧化还原反应规律与平衡移动原理的关系,回答下列问题:
(1)用Fe2(SO4)3晶体配制100 mL 0.05 mol/L的溶液,配制时需先把Fe2(SO4)3晶体溶解在较浓的硫酸中,再用水稀释,加入硫酸的目的是_____ (结合化学方程式回答)。
(2)甲组同学将0.10 mol/L的KI溶液和0.05 mol/L的Fe2(SO4)3溶液各5 mL混合充分反应后,溶液变为棕黄色,现进行如下实验①②。
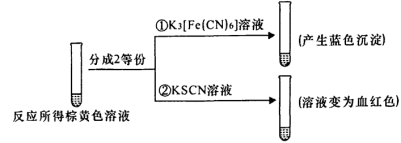
实验①中产生蓝色沉淀的离子方程式为_______ ,根据以上反应现象写出甲组同学实验中的离子方程式:_______ ,在甲组同学的反应中,I2和Fe3+的氧化性强弱顺序为_______ 。
(1)用Fe2(SO4)3晶体配制100 mL 0.05 mol/L的溶液,配制时需先把Fe2(SO4)3晶体溶解在较浓的硫酸中,再用水稀释,加入硫酸的目的是
(2)甲组同学将0.10 mol/L的KI溶液和0.05 mol/L的Fe2(SO4)3溶液各5 mL混合充分反应后,溶液变为棕黄色,现进行如下实验①②。

实验①中产生蓝色沉淀的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某实验小组学习化学反应速率后,联想到H2O2分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。
(1)实验乙中发生反应的化学方程式为_______ 。
(2)实验甲和实验乙的实验目的是_______ 。实验甲和实验丙的实验目的是_______ 。
(3)这种控制其他条件不变,只改变单一条件的方法叫做_______ 。
(4)实验过程中该同学对实验乙中产生的气体进行收集,并在2 min内6个时间点对注射器内气体进行读数,记录数据如下表。
(在反应环境相同时,可直接用体积变化量与反应时间的比值表示反应速率)
0~20 s的反应速率v1=_______ mL·s-1,100~120 s的反应速率v2=_______ mL·s-1。不考虑实验测量误差,二者速率存在差异的主要原因是_______ 。
| 编号 | 温度℃ | 反应物 | 催化剂 |
| 甲 | 25 | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
| 乙 | 25 | 试管中加入3mL5%H2O2溶液 | 1mL0.1mol/LFeCl3溶液 |
| 丙 | 40 | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
(2)实验甲和实验乙的实验目的是
(3)这种控制其他条件不变,只改变单一条件的方法叫做
(4)实验过程中该同学对实验乙中产生的气体进行收集,并在2 min内6个时间点对注射器内气体进行读数,记录数据如下表。
(在反应环境相同时,可直接用体积变化量与反应时间的比值表示反应速率)
| 时间/s | 20 | 40 | 60 | 80 | 90 | 120 | |
| 气体体积/mL | 实验乙 | 15.0 | 29.5 | 43.5 | 56.5 | 69.5 | 81.5 |
您最近一年使用:0次
【推荐3】硫酸是重要的化工原料,工业上以黄铁矿(主要成分是 )为原料,采用接触法生产硫酸,流程简单示意图如下:
)为原料,采用接触法生产硫酸,流程简单示意图如下:

(1)焙烧时 全部转化为
全部转化为 和一种具有刺激性气味的气体X,反应的化学方程式为
和一种具有刺激性气味的气体X,反应的化学方程式为___________ 。
(2)一定温度下,发生反应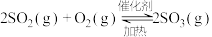 ,在2L密闭容器内,500℃,测得
,在2L密闭容器内,500℃,测得 随时间的变化如下表:
随时间的变化如下表:
①反应达到平衡时, 的转化率是
的转化率是___________ 。
②用 表示0~2s内该反应的平均速率
表示0~2s内该反应的平均速率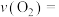
___________ 。
③说明反应已达到平衡状态的是___________ (填标号)。
A.容器内气体压强保持不变
B.
C.容器内气体的浓度
D.容器内气体密度保持不变
(3)硫酸工业中可合成 ,下表列出了不同温度、压强下
,下表列出了不同温度、压强下 的平衡转化率:
的平衡转化率:
已知工业合成 选定的温度为450℃,选定的压强为常压;请阐述选择常压而不是高压的原因:
选定的温度为450℃,选定的压强为常压;请阐述选择常压而不是高压的原因:___________ 。
(4)硫酸工业生产中 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为98.3%,适宜温度为
所用硫酸的适宜浓度为98.3%,适宜温度为___________ ,而工业生产中一般采用60℃的可能原因是___________ 。

 )为原料,采用接触法生产硫酸,流程简单示意图如下:
)为原料,采用接触法生产硫酸,流程简单示意图如下:
(1)焙烧时
 全部转化为
全部转化为 和一种具有刺激性气味的气体X,反应的化学方程式为
和一种具有刺激性气味的气体X,反应的化学方程式为(2)一定温度下,发生反应
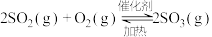 ,在2L密闭容器内,500℃,测得
,在2L密闭容器内,500℃,测得 随时间的变化如下表:
随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
 (mol) (mol) | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
 的转化率是
的转化率是②用
 表示0~2s内该反应的平均速率
表示0~2s内该反应的平均速率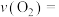
③说明反应已达到平衡状态的是
A.容器内气体压强保持不变
B.

C.容器内气体的浓度

D.容器内气体密度保持不变
(3)硫酸工业中可合成
 ,下表列出了不同温度、压强下
,下表列出了不同温度、压强下 的平衡转化率:
的平衡转化率:| 温度/℃ |  的平衡转化率% 的平衡转化率% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
 选定的温度为450℃,选定的压强为常压;请阐述选择常压而不是高压的原因:
选定的温度为450℃,选定的压强为常压;请阐述选择常压而不是高压的原因:(4)硫酸工业生产中
 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为98.3%,适宜温度为
所用硫酸的适宜浓度为98.3%,适宜温度为
您最近一年使用:0次



