根据实验室测定硫酸铜结晶(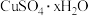 )水含量的实验,填写下列空白:
)水含量的实验,填写下列空白:
实验步骤为:①研磨;②准确称取10.990g已经研碎的硫酸铜晶体;③加热;④冷却;⑤称量;⑥重复③至⑤的操作,直至……;⑦根据实验数据计算硫酸铜晶体里结晶水的含量。回答相关问题:
(1)步骤②需要的实验仪器是___________ ,④需要使用干燥器,使用此仪器的目的是___________ ,步骤⑥操作为重复③至⑤的操作的目的是___________
(2)步骤③所用的大部分仪器如下,在空格中填入仪器的名称:
灼烧时将瓷坩埚置于___________ 上(用所给仪器的编号填入,下同),取用坩埚应使用___________ ,灼烧后的坩埚应放在___________ 上,不能直接放在桌面上
实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
某学生实验后得到以下数据:
(3)若无需再进行第三次称量,则a的数值范围应为___________ (区间表示)
(4)若加热后坩埚与固体总质量为18.620g,计算x的实测值___________ (保留二位小数),相对误差为___________
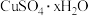 )水含量的实验,填写下列空白:
)水含量的实验,填写下列空白:实验步骤为:①研磨;②准确称取10.990g已经研碎的硫酸铜晶体;③加热;④冷却;⑤称量;⑥重复③至⑤的操作,直至……;⑦根据实验数据计算硫酸铜晶体里结晶水的含量。回答相关问题:
(1)步骤②需要的实验仪器是
(2)步骤③所用的大部分仪器如下,在空格中填入仪器的名称:
灼烧时将瓷坩埚置于
实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
某学生实验后得到以下数据:
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
| 第一次称量 | 第二次称量 | ||
| 11.710g | 22.700g | 18.621g | a |
(4)若加热后坩埚与固体总质量为18.620g,计算x的实测值
更新时间:2022-02-20 23:17:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】溴苯( )是一种化工原料。实验室可用苯和液溴反应制得,有关物质的物理性质如下表,回答下列问题。
)是一种化工原料。实验室可用苯和液溴反应制得,有关物质的物理性质如下表,回答下列问题。
(1)某小组拟选用如图两套装置制取溴苯。
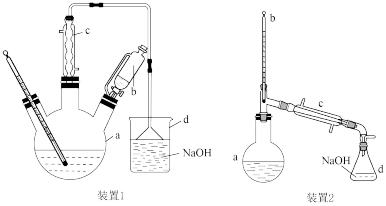
①装置1中仪器b的名称是_______ 。
②若用装置2中的直形冷凝管c代替装置1中的球形冷凝管c,不足之处是_______ 。
(2)反应完的混合物中含苯、液溴、溴苯、铁屑,将混合物转移至烧杯中,经过下列步骤分离提纯:
步骤①:向烧杯中加入10 mL水,然后过滤除去未反应的铁屑。
步骤②:滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_______ (用化学方程式表示)。
步骤③:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
步骤④:_______ 。
(3)由溴苯的同系物一溴甲苯(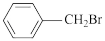 )可制备苯甲醇(
)可制备苯甲醇( ),在一定条件下高铁酸盐(FeO
),在一定条件下高铁酸盐(FeO )可将苯甲醇氧化为苯甲醛(
)可将苯甲醇氧化为苯甲醛(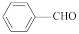 )
)
①写出一溴甲苯制备苯甲醇的化学方程式_______ 。
②控制适当温度,向碱性次氯酸盐溶液中加入Fe(NO3)3,搅拌,生成高铁酸盐,其反应的离子方程式是_______ 。
③当反应溶液pH=11.5,反应4分钟时,温度对苯甲醇氧化反应影响的实验数据如下表:
温度对苯甲醇氧化反应的影响
分析表中数据,N的数值应该为_______ (填选项)。
A.72.3 B.45.5 C.26.8
随着温度的升高,苯甲醛产率逐渐降低的主要原因是_______ 。
 )是一种化工原料。实验室可用苯和液溴反应制得,有关物质的物理性质如下表,回答下列问题。
)是一种化工原料。实验室可用苯和液溴反应制得,有关物质的物理性质如下表,回答下列问题。| 苯 | 液溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

①装置1中仪器b的名称是
②若用装置2中的直形冷凝管c代替装置1中的球形冷凝管c,不足之处是
(2)反应完的混合物中含苯、液溴、溴苯、铁屑,将混合物转移至烧杯中,经过下列步骤分离提纯:
步骤①:向烧杯中加入10 mL水,然后过滤除去未反应的铁屑。
步骤②:滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是
步骤③:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
步骤④:
(3)由溴苯的同系物一溴甲苯(
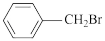 )可制备苯甲醇(
)可制备苯甲醇( ),在一定条件下高铁酸盐(FeO
),在一定条件下高铁酸盐(FeO )可将苯甲醇氧化为苯甲醛(
)可将苯甲醇氧化为苯甲醛(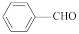 )
)①写出一溴甲苯制备苯甲醇的化学方程式
②控制适当温度,向碱性次氯酸盐溶液中加入Fe(NO3)3,搅拌,生成高铁酸盐,其反应的离子方程式是
③当反应溶液pH=11.5,反应4分钟时,温度对苯甲醇氧化反应影响的实验数据如下表:
温度对苯甲醇氧化反应的影响
| T/℃ | 苯甲醇转化率/% | 苯甲醛 | |
| 选择性/% | 产率/% | ||
| 18 | 62.0 | 82.3 | 51.0 |
| 28 | 68.5 | 67.9 | 46.5 |
| 38 | 86.8 | N | 39.5 |
| 48 | 96.3 | 29.8 | 28.7 |
A.72.3 B.45.5 C.26.8
随着温度的升高,苯甲醛产率逐渐降低的主要原因是
您最近一年使用:0次
【推荐2】某小组探究乙醛与银氨溶液反应产生银镜的条件。
已知: 。
。
(1)向银氨溶液中滴加乙醛,振荡后将试管放在热水浴中加热,试管内壁产生银镜。写出反应的化学方程式_______ 。
(2)文献记载:碱性条件有利于银镜产生。小组设计实验验证该说法。
①对比实验_______ 和_______ ,证实了文献的说法。
②实验Ⅱ未产生银镜,结合以下机理简要分析原因_______ 。
 CH3COO-+Ag
CH3COO-+Ag
(3)文献还记载:在强碱条件下,加热银氨溶液可能析出银镜。小组进一步实验如下。
实验Ⅳ:向银氨溶液中加入NaOH溶液至pH=14,得到棕黑色沉淀,振荡后将试管放在热水浴中温热,有气泡产生,试管内壁产生银镜。
①实验Ⅳ中,将Ag元素还原的离子可能是_______ 。
②经检验棕黑色沉淀Y中含有Ag单质,请设计实验方案验证:_______ 。
已知:
 。
。(1)向银氨溶液中滴加乙醛,振荡后将试管放在热水浴中加热,试管内壁产生银镜。写出反应的化学方程式
(2)文献记载:碱性条件有利于银镜产生。小组设计实验验证该说法。
| 序号 | 实验 | 试剂 | 混合液pH | 现象 |
| Ⅰ |  | NaOH | 10 | 常温产生银镜 |
| Ⅱ | 浓氨水 | 10 | 加热无银镜 | |
| Ⅲ | 无 | 8 | 加热才能产生银镜 |
②实验Ⅱ未产生银镜,结合以下机理简要分析原因
 CH3COO-+Ag
CH3COO-+Ag(3)文献还记载:在强碱条件下,加热银氨溶液可能析出银镜。小组进一步实验如下。
实验Ⅳ:向银氨溶液中加入NaOH溶液至pH=14,得到棕黑色沉淀,振荡后将试管放在热水浴中温热,有气泡产生,试管内壁产生银镜。
①实验Ⅳ中,将Ag元素还原的离子可能是
②经检验棕黑色沉淀Y中含有Ag单质,请设计实验方案验证:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)如何用实验证明绿矾中的铁是二价铁而不是三价铁_______ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。

①仪器B的名称是________ 。
②将下列实验操作步骤正确排序_______ (填标号);重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.打开K1和K2,缓缓通入N2 c.关闭K1和K2
d.熄灭酒精灯 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=_______ (列式表示)。若实验时按a、b次序操作,则使x_______ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
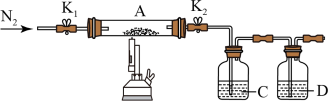
①C中的溶液为BaCl2,其作用是______ 。D溶液为______ ,D中可观察到的现象为_______ 。
②写出硫酸亚铁高温分解反应的化学方程式________ 。
③有同学认为该实验装置存在一定缺陷,请你谈谈完善该试验装置的措施____ 。
(1)如何用实验证明绿矾中的铁是二价铁而不是三价铁
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.打开K1和K2,缓缓通入N2 c.关闭K1和K2
d.熄灭酒精灯 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C中的溶液为BaCl2,其作用是
②写出硫酸亚铁高温分解反应的化学方程式
③有同学认为该实验装置存在一定缺陷,请你谈谈完善该试验装置的措施
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氮化硅(Si3N4)是一种重要的结构陶瓷材料,硬度大。某兴趣小组设计下列方案制备少量氮化硅。
i.制备流程: 。
。
ii. 的制备反应:
的制备反应: (放热反应,己烷作溶剂),制备装置如图所示。
(放热反应,己烷作溶剂),制备装置如图所示。

已知:氨气在高温下易分解: 。
。
回答下列问题:
(1)仪器M的名称为_______ 。
(2)装置A中产生氨气的总化学方程式为_______ 。
(3)液体石蜡鼓泡瓶的作用是_______ 。电磁搅拌器上水槽中的X是固液混合体,则X是_______ 。
(4)下列装置可用于吸收氨气的是_______ (填序号)。

(5)采用热重分析法测定 热分解生成
热分解生成 的质量。
的质量。

① 在
在 下分解生成
下分解生成 的化学方程式是
的化学方程式是_______ 。
②将样品加热到 时,完全反应后,样品失重1.7
时,完全反应后,样品失重1.7 ,则生成
,则生成 的质量是
的质量是_______  。
。
i.制备流程:
 。
。ii.
 的制备反应:
的制备反应: (放热反应,己烷作溶剂),制备装置如图所示。
(放热反应,己烷作溶剂),制备装置如图所示。
已知:氨气在高温下易分解:
 。
。回答下列问题:
(1)仪器M的名称为
(2)装置A中产生氨气的总化学方程式为
(3)液体石蜡鼓泡瓶的作用是
(4)下列装置可用于吸收氨气的是

(5)采用热重分析法测定
 热分解生成
热分解生成 的质量。
的质量。
①
 在
在 下分解生成
下分解生成 的化学方程式是
的化学方程式是②将样品加热到
 时,完全反应后,样品失重1.7
时,完全反应后,样品失重1.7 ,则生成
,则生成 的质量是
的质量是 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】连二亚硫酸钠 又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
Ⅰ.查阅材料
i.连二亚硫酸钠 是一种白色粉末,易溶于水,难溶于乙醇。
是一种白色粉末,易溶于水,难溶于乙醇。
ii.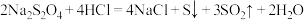
iii.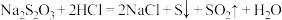
II.制备方法
 ℃时将甲酸钠和纯碱加入乙醇水溶液中,通入
℃时将甲酸钠和纯碱加入乙醇水溶液中,通入 进行反应,完成其反应方程式:
进行反应,完成其反应方程式:_____ 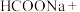
______ 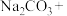
______ = ______ 
______ 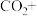
____ ,冷却至40℃~45℃,过滤,用 ______ 洗涤,干燥制得 ;
;
III. 的性质
的性质
(1) 溶液在空气中易被氧化,课题小组测定
溶液在空气中易被氧化,课题小组测定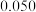

 溶液在空气中pH变化如图:
溶液在空气中pH变化如图: 段主要生成
段主要生成 ,根据pH变化图,
,根据pH变化图, 的电离平衡
的电离平衡 ______ 水解平衡 填“
填“ ”或“
”或“ ”
” ,课题小组推测
,课题小组推测 溶液在空气中易被氧化,
溶液在空气中易被氧化, 发生离子反应方程式为
发生离子反应方程式为 ______ 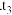 时溶液中主要阴离子符号是
时溶液中主要阴离子符号是 ______ 。
(2)隔绝空气加热 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和气体为
和气体为 ______  填化学式
填化学式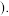 请你设计实验验证产物有
请你设计实验验证产物有 存在,完成下表中内容.
存在,完成下表中内容. 供选择的试剂:稀盐酸、稀硝酸、
供选择的试剂:稀盐酸、稀硝酸、 溶液、
溶液、 溶液
溶液
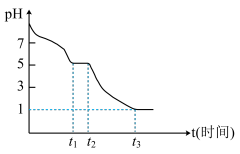
 又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。Ⅰ.查阅材料
i.连二亚硫酸钠
 是一种白色粉末,易溶于水,难溶于乙醇。
是一种白色粉末,易溶于水,难溶于乙醇。ii.
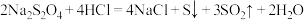
iii.
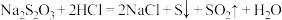
II.制备方法
 ℃时将甲酸钠和纯碱加入乙醇水溶液中,通入
℃时将甲酸钠和纯碱加入乙醇水溶液中,通入 进行反应,完成其反应方程式:
进行反应,完成其反应方程式: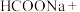
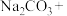

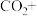
 ;
;III.
 的性质
的性质(1)
 溶液在空气中易被氧化,课题小组测定
溶液在空气中易被氧化,课题小组测定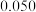

 溶液在空气中pH变化如图:
溶液在空气中pH变化如图: 段主要生成
段主要生成 ,根据pH变化图,
,根据pH变化图, 的电离平衡
的电离平衡  填“
填“ ”或“
”或“ ”
” ,课题小组推测
,课题小组推测 溶液在空气中易被氧化,
溶液在空气中易被氧化, 发生离子反应方程式为
发生离子反应方程式为 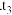 时溶液中主要阴离子符号是
时溶液中主要阴离子符号是 (2)隔绝空气加热
 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和气体为
和气体为  填化学式
填化学式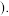 请你设计实验验证产物有
请你设计实验验证产物有 存在,完成下表中内容.
存在,完成下表中内容. 供选择的试剂:稀盐酸、稀硝酸、
供选择的试剂:稀盐酸、稀硝酸、 溶液、
溶液、 溶液
溶液
实验步骤 不要求写出具体操作过程 不要求写出具体操作过程 | 预期的实验现象和结论 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
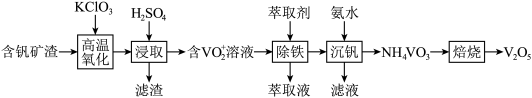
【推荐3】五氧化二钒在冶金、化工等领域有重要应用。实验室以含钒矿渣(主要成分为FeO·V2O3、V2O5,含少量SiO2杂质)为原料制备V2O5的主要流程如下:
已知:①钒有多种价态,其中+5价最稳定
②
回答下列问题:
(1)“高温氧化”过程中消耗1molKClO3转移6mol电子,该反应的化学方程式为___________ 。滤渣的主要成分为___________ 。
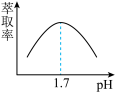
(2)“除铁”时,萃取剂(HA)萃取Fe3+的原理为: 的萃取率与pH的关系如下图所示。pH<1.7时,萃取率上升的原因是
的萃取率与pH的关系如下图所示。pH<1.7时,萃取率上升的原因是___________ 。
(3)“沉钒”过程中主要反应的离子方程式为___________ 。
(4)研究表明“焙烧”过程分为三步,每一步产生NH3和H2O(g)的物质的量之比分别为2∶1、3∶1、x。取117gNH4VO3固体进行热重分析,剩余固体质量与温度的关系如图所示。图中m=___________ ;分解过程最后一步产生的NH3和H2O(g)的物质的量之比x=___________ 。


已知:①钒有多种价态,其中+5价最稳定
②

回答下列问题:
(1)“高温氧化”过程中消耗1molKClO3转移6mol电子,该反应的化学方程式为
(2)“除铁”时,萃取剂(HA)萃取Fe3+的原理为:
 的萃取率与pH的关系如下图所示。pH<1.7时,萃取率上升的原因是
的萃取率与pH的关系如下图所示。pH<1.7时,萃取率上升的原因是
(3)“沉钒”过程中主要反应的离子方程式为
(4)研究表明“焙烧”过程分为三步,每一步产生NH3和H2O(g)的物质的量之比分别为2∶1、3∶1、x。取117gNH4VO3固体进行热重分析,剩余固体质量与温度的关系如图所示。图中m=

您最近一年使用:0次



