已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。
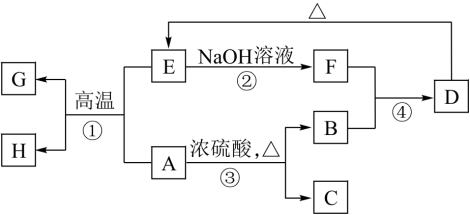
(1)H的名称是___________ 。
(2)写出E的一种用途是___________ ,其与氢氧化钠溶液反应的离子方程式为___________ 。
(3)反应③的化学方程式是___________ 。
(4)反应④的离子方程式是___________ 。

(1)H的名称是
(2)写出E的一种用途是
(3)反应③的化学方程式是
(4)反应④的离子方程式是
更新时间:2022-03-22 22:26:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某无色透明的溶液中可能大量含有以下离子中的几种: 、
、 、
、 、
、 、
、 、
、 、
、 、
、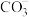 、
、 、
、 ,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:
,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:
①取少量溶液于试管中,滴入石蕊试液,溶液变红;
②取少量溶液做焰色试验,透过蓝色钴玻璃片观察,焰色为紫色;
③取少量溶液于试管中,滴入硝酸钡溶液,产生白色沉淀;
④取少量溶液于试管中,滴入过量氢氧化钠溶液,产生白色沉淀;
(1)由步骤①可以判断溶液中存在的离子为___________ (填离子符号,下同),由步骤②可以判断溶液中存在的离子为___________ 。
(2)写出步骤③发生反应的离子方程式___________ ;写出步骤④产生白色沉淀的离子方程式___________ ;
(3)综合以上实验分析,该溶液中一定存在的阴离子是___________ (填离子符号)。
(4)取一定量的原溶液,逐滴滴入 溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈
溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈___________ 性(填“酸”、“中”、“碱”),此时溶液中还大量存在的阳离子为___________ (填离子符号)。
(5)取一定量的原溶液,加入铜片,观察到铜片溶解,同时产生气泡(经测定该气体为NO),溶液最终变为蓝色。写出该反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、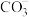 、
、 、
、 ,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:
,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:①取少量溶液于试管中,滴入石蕊试液,溶液变红;
②取少量溶液做焰色试验,透过蓝色钴玻璃片观察,焰色为紫色;
③取少量溶液于试管中,滴入硝酸钡溶液,产生白色沉淀;
④取少量溶液于试管中,滴入过量氢氧化钠溶液,产生白色沉淀;
(1)由步骤①可以判断溶液中存在的离子为
(2)写出步骤③发生反应的离子方程式
(3)综合以上实验分析,该溶液中一定存在的阴离子是
(4)取一定量的原溶液,逐滴滴入
 溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈
溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈(5)取一定量的原溶液,加入铜片,观察到铜片溶解,同时产生气泡(经测定该气体为NO),溶液最终变为蓝色。写出该反应的离子方程式
您最近一年使用:0次
【推荐2】用于灭活新冠病毒的二氧化氯稳定性较差(纯 易分解爆炸),故用
易分解爆炸),故用 和NaOH混合溶液将其吸收转化为
和NaOH混合溶液将其吸收转化为 保存。现利用如下装置(夹持装置略去)及试剂制备
保存。现利用如下装置(夹持装置略去)及试剂制备 。
。
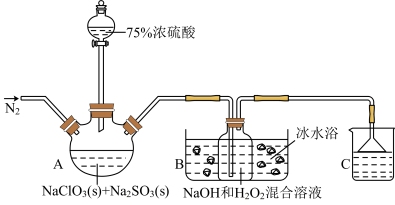
已知:① 熔点―59℃、沸点11℃,在碱性环境中发生反应:
熔点―59℃、沸点11℃,在碱性环境中发生反应: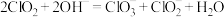 ;
;
②温度高于60℃时, 分解成
分解成 和NaCl。
和NaCl。
回答下列问题:
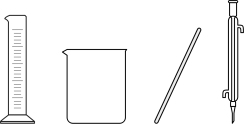
(1)配制75%浓硫酸,下列仪器中不需要的是_______ (填仪器名称)。
(2)A为 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为_______ 。
(3)实验过程中持续通入 的作用是
的作用是_______ 。
(4)装置B中 和NaOH需按照一定比例混合配成溶液与
和NaOH需按照一定比例混合配成溶液与 反应制取
反应制取 ,
, 作
作_______ (填“氧化剂”或“还原剂”);此装置需要采用冰水浴,可能的原因为_______ (任写一点)。
(5)装置C烧杯中的试剂是_______ 。
(6)某同学认为实验过程中会产生 ,推测产品中可能含
,推测产品中可能含 杂质,请设计简单实验证明
杂质,请设计简单实验证明_______ 。
(7)某研究性学习小组用制取的 作漂白剂。0.5mol
作漂白剂。0.5mol 的氧化能力(得电子数)相当于
的氧化能力(得电子数)相当于_______ g  的氧化能力。
的氧化能力。
 易分解爆炸),故用
易分解爆炸),故用 和NaOH混合溶液将其吸收转化为
和NaOH混合溶液将其吸收转化为 保存。现利用如下装置(夹持装置略去)及试剂制备
保存。现利用如下装置(夹持装置略去)及试剂制备 。
。
已知:①
 熔点―59℃、沸点11℃,在碱性环境中发生反应:
熔点―59℃、沸点11℃,在碱性环境中发生反应: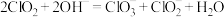 ;
;②温度高于60℃时,
 分解成
分解成 和NaCl。
和NaCl。回答下列问题:
(1)配制75%浓硫酸,下列仪器中不需要的是

(2)A为
 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为(3)实验过程中持续通入
 的作用是
的作用是(4)装置B中
 和NaOH需按照一定比例混合配成溶液与
和NaOH需按照一定比例混合配成溶液与 反应制取
反应制取 ,
, 作
作(5)装置C烧杯中的试剂是
(6)某同学认为实验过程中会产生
 ,推测产品中可能含
,推测产品中可能含 杂质,请设计简单实验证明
杂质,请设计简单实验证明(7)某研究性学习小组用制取的
 作漂白剂。0.5mol
作漂白剂。0.5mol 的氧化能力(得电子数)相当于
的氧化能力(得电子数)相当于 的氧化能力。
的氧化能力。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫代硫酸钠又名大苏打,为氰化物的解毒剂。工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
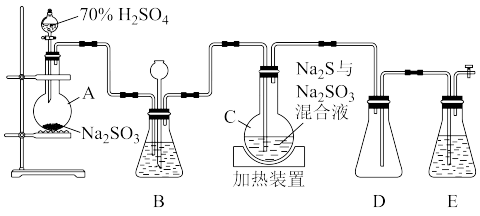
烧瓶C中发生反应如下:
①Na2S(a)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
②2H2S(aq)+SO2(g)= 3S(s)+2H2O(l)快 (II)
③S(s)+Na2SO3(aq)=Na2S2O3(aq)慢 (III)
回答下列问题:
(1)装置A中发生反应的离子方程式为_______ 。
(2)装置D的作用是_______ 。
(3)结合反应原理,装置C中反应已经完成的实验现象是_______ 。
(4)装置B有多重作用,其一可以用于整套装置气密性检查,请写出操作及现象:_______ ;其二可以用于观察SO2的生成速率,其中的液体最好选择_______ 。
(5)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_______ 。

烧瓶C中发生反应如下:
①Na2S(a)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
②2H2S(aq)+SO2(g)= 3S(s)+2H2O(l)快 (II)
③S(s)+Na2SO3(aq)=Na2S2O3(aq)慢 (III)
回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)装置D的作用是
(3)结合反应原理,装置C中反应已经完成的实验现象是
(4)装置B有多重作用,其一可以用于整套装置气密性检查,请写出操作及现象:
(5)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图所示转化关系中,A、B均为单质,F为酸性氧化物,C为日常生活中最常见的无色无味液体,D、E、G、H均为含A元素的化合物,H常用作膨松剂(其他与题目无关的生成物均已略去)。
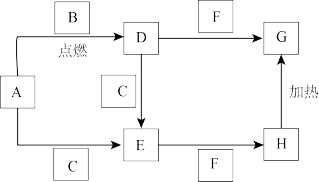
回答下列问题:
(1)A在空气中久置易变质,最终生成_______ (填化学式)。
(2)C+D→E的离子方程式为_______ ;将3.9g D溶于C配成500mL溶液,所得溶液中溶质的物质的量浓度为_______ mol/L。
(3)H→G的化学方程式为_______ 。
(4)E与F反应可以生成H,也可以生成G,生成H的离子方程式为_______ ;除去H溶液中混有的G的试剂是_______ (填化学式)。

回答下列问题:
(1)A在空气中久置易变质,最终生成
(2)C+D→E的离子方程式为
(3)H→G的化学方程式为
(4)E与F反应可以生成H,也可以生成G,生成H的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
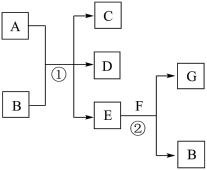
(1)G、A的化学式分别为_______ 、_______ 。
(2)写出反应①的化学方程式:______ 。
(3)写出反应②的化学方程式:_______ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是_______ 。请写出A与水反应的化学方程式:_______ 。
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是________ (用化学方程式表示)。

(1)G、A的化学式分别为
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】多晶硅是制作光伏电池的关键材料,以下是工业上由石英砂制备多晶硅的简易流程。
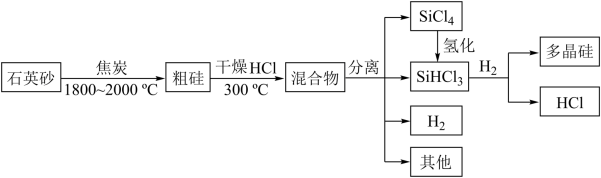
(1)请写出由石英砂制备粗硅的主要方程式___ 。
(2)经研究发现SiO2生成Si的反应机理不是一步完成的,反应机理如下:
反应1:SiO2(s)+C(s) SiO(g)+CO(g)
SiO(g)+CO(g)
反应2:SiO(g)+2C(s) SiC(s)+CO(g)
SiC(s)+CO(g)
反应3:2SiO2(s)+SiC(s) 3SiO(g)+CO(g)
3SiO(g)+CO(g)
反应4:SiO(g)+SiC(s) 2Si(l)+CO(g)
2Si(l)+CO(g)
反应5:SiO2(s)+Si(l) 2SiO(g)
2SiO(g)
如图曲线表示5个反应的平衡pSiO/pCO与温度变化关系图。
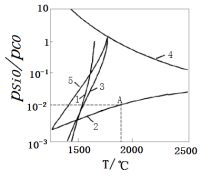
结合图象判断反应2的△H___ 0(填“>”、“<”或“=”),请说明理由___ 。
(3)工业上以硅粉和氯化氢气体为原料生产SiHCl3时伴随发生的反应有:
Si(s)+4HCl(g)=SiCl4(g)+2H2(g)∆H=-241kJ•mol-1
SiHCl3(g)+HCl(g)=SiCl4(g)+H2(g)∆H=-31kJ•mol-1
请书写以硅粉和氯化氢气体生产SiHCl3的热化学反应方程式___ 。
(4)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl3(g)+HCl(g)∆H1>0
SiHCl3(g)+HCl(g)∆H1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)∆H2<0
4SiHCl3(g)∆H2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g) 3SiHCl3(g)∆H3
3SiHCl3(g)∆H3
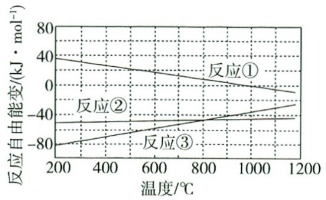
已知体系自由能变∆G=∆H-T∆S,∆G<0时反应自发进行。三个氢化反应的∆G与温度的关系如图所示,可知:反应①能自发进行的最低温度是___ ;相同温度下,反应②比反应①的∆G小,主要原因是___ 。

(1)请写出由石英砂制备粗硅的主要方程式
(2)经研究发现SiO2生成Si的反应机理不是一步完成的,反应机理如下:
反应1:SiO2(s)+C(s)
 SiO(g)+CO(g)
SiO(g)+CO(g)反应2:SiO(g)+2C(s)
 SiC(s)+CO(g)
SiC(s)+CO(g)反应3:2SiO2(s)+SiC(s)
 3SiO(g)+CO(g)
3SiO(g)+CO(g)反应4:SiO(g)+SiC(s)
 2Si(l)+CO(g)
2Si(l)+CO(g)反应5:SiO2(s)+Si(l)
 2SiO(g)
2SiO(g)如图曲线表示5个反应的平衡pSiO/pCO与温度变化关系图。

结合图象判断反应2的△H
(3)工业上以硅粉和氯化氢气体为原料生产SiHCl3时伴随发生的反应有:
Si(s)+4HCl(g)=SiCl4(g)+2H2(g)∆H=-241kJ•mol-1
SiHCl3(g)+HCl(g)=SiCl4(g)+H2(g)∆H=-31kJ•mol-1
请书写以硅粉和氯化氢气体生产SiHCl3的热化学反应方程式
(4)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)
 SiHCl3(g)+HCl(g)∆H1>0
SiHCl3(g)+HCl(g)∆H1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g)∆H2<0
4SiHCl3(g)∆H2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)
 3SiHCl3(g)∆H3
3SiHCl3(g)∆H3已知体系自由能变∆G=∆H-T∆S,∆G<0时反应自发进行。三个氢化反应的∆G与温度的关系如图所示,可知:反应①能自发进行的最低温度是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氮化硅高温陶瓷材料是现代重要的结构陶瓷,因其有硬度大、熔点高、化学性质稳定等特点而受到广泛关注。工业上普遍用下列流程进行生产:

(1)SiO2和C反应除了得到粗硅外,还有可能得到一种硬度也很大的物质SiC,是生成粗硅还是生成该物质主要是由___ 决定的。
(2)反应①的条件是隔绝空气和____ 。
(3)写出制粗硅的反应的化学方程式____ 。
(4)写出硅与氢氧化钠溶液的离子方程式____ 。
(5)现在是用四氯化硅、氮气、氢气在稀有气体保护下加强热,得到纯度较高的氮化硅,其反应方程式为___ 。

(1)SiO2和C反应除了得到粗硅外,还有可能得到一种硬度也很大的物质SiC,是生成粗硅还是生成该物质主要是由
(2)反应①的条件是隔绝空气和
(3)写出制粗硅的反应的化学方程式
(4)写出硅与氢氧化钠溶液的离子方程式
(5)现在是用四氯化硅、氮气、氢气在稀有气体保护下加强热,得到纯度较高的氮化硅,其反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】2017年1月4日,谷歌公司宣布:以60胜0负1平的战绩横扫众多围棋高手的神秘棋手“Master”乃是其人工智能产品AlpbaGo的升级版,人工智能再次成为热门话题。其中,高纯度硅是一种重要的基础材料。以下是工业上制取纯硅的一种方法:
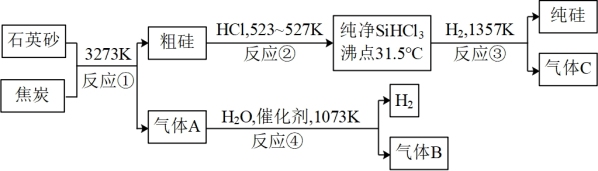
请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有_______ (填反应代号)。
(2)反应①的化学方程式:_______ ;反应③的化学方程式_______ 。
(3)下列有关硅材料的说法正确的是_______ 。
A.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
B.金刚砂是一种新型陶瓷材料
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D. 能做光导纤维的原因是因为自身具有良好的导电性
能做光导纤维的原因是因为自身具有良好的导电性
E.建筑用的水泥和实验室使用的陶瓷坩埚都属于硅酸盐材料
(4)已知硅的最简单氢化物甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水,已知室温条件下,1g甲硅烷自燃放出热量为44.6kJ。则其热化学方程式是_______ ;
(5)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是_______ (填字母)。
A.高温结构陶瓷B.生物陶瓷C.导电陶瓷。

请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有
(2)反应①的化学方程式:
(3)下列有关硅材料的说法正确的是
A.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
B.金刚砂是一种新型陶瓷材料
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.
 能做光导纤维的原因是因为自身具有良好的导电性
能做光导纤维的原因是因为自身具有良好的导电性E.建筑用的水泥和实验室使用的陶瓷坩埚都属于硅酸盐材料
(4)已知硅的最简单氢化物甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水,已知室温条件下,1g甲硅烷自燃放出热量为44.6kJ。则其热化学方程式是
(5)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是
A.高温结构陶瓷B.生物陶瓷C.导电陶瓷。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】太阳能光伏产业蓬勃发展,推动了高纯硅的生产和应用。工业上以硅石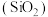 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
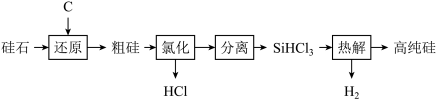
已知: 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。
(1)Si在元素周期表中的位置是_______ 。
(2)“还原”需在高温条件下进行,该反应的化学方程式是_______ 。
(3)“氯化”时的还原产物是_______ (填化学式)。
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是_______ 。
(5)该流程中能循环利用的物质是_______ (填两种)。
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。

①氢氟酸不能用玻璃试剂瓶保存的原因是_______ 。
②酸性条件下,羟胺与 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为_______ 。
③高纯硅样品中铁的质量为_______ 。
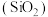 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
已知:
 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。(1)Si在元素周期表中的位置是
(2)“还原”需在高温条件下进行,该反应的化学方程式是
(3)“氯化”时的还原产物是
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是
(5)该流程中能循环利用的物质是
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺
 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。
①氢氟酸不能用玻璃试剂瓶保存的原因是
②酸性条件下,羟胺与
 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为③高纯硅样品中铁的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组设计了如下装置对焦炭还原二氧化硅的气体产物的成分进行探究。

已知:PdCl2溶液可用于检验CO,反应的化学方程式为CO + PdCl2 + H2O = CO2 + 2HCl + Pd(产生黑色金属钯粉末,使溶液变浑浊)。
(1)实验时要通入足够长时间的N2,其原因是________________________ 。
(2)装置B的作用是____________________________ 。
(3)装置C、D中所盛试剂分别为___ 、___ ,若装置C、D中溶液均变浑浊,且经检测两气体产物的物质的量相等,则该反应的化学方程式为____________________________ 。
(4)该装置的缺点是____________________________ 。
(5)设计实验证明碳酸的酸性比硅酸的强:____________________________ 。

已知:PdCl2溶液可用于检验CO,反应的化学方程式为CO + PdCl2 + H2O = CO2 + 2HCl + Pd(产生黑色金属钯粉末,使溶液变浑浊)。
(1)实验时要通入足够长时间的N2,其原因是
(2)装置B的作用是
(3)装置C、D中所盛试剂分别为
(4)该装置的缺点是
(5)设计实验证明碳酸的酸性比硅酸的强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。二氧化硅又称硅石,是制备硅及其化合物的重要原料,部分转化过程如图所示。回答下面问题:_______ (填字母)。
A.碳元素和硅元素都位于周期表的IVA族,非金属性较强的是碳元素
B.自然界中存在天然游离的硅单质
C.玻璃、水泥、陶瓷都是传统的硅酸盐产品
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.硅元素在金属与非金属的分界线处,因此具弱导电性,一般可用作半导体材料
(2)光导纤维是一种良好的通讯材料,其成分是_______ (填化学式,下同),高纯硅是制造半导体芯片的基础原材料,由SiO2制备高纯度硅的工业流程如上图所示,可以循环使用的物质为_______ 和_______ ,写出第①步的化学方程式_______ 。
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学反应方程式为_______ 。
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
①根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式_______ 。
②根据以上描述,推测氮化硅可能有哪些用途:_______ (填字母)。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具

A.碳元素和硅元素都位于周期表的IVA族,非金属性较强的是碳元素
B.自然界中存在天然游离的硅单质
C.玻璃、水泥、陶瓷都是传统的硅酸盐产品
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.硅元素在金属与非金属的分界线处,因此具弱导电性,一般可用作半导体材料
(2)光导纤维是一种良好的通讯材料,其成分是
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学反应方程式为
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
①根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式
②根据以上描述,推测氮化硅可能有哪些用途:
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
您最近一年使用:0次




