下列说法正确的是
A.甲醛(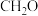 )分子中 )分子中 键和 键和 键的个数比为2∶1 键的个数比为2∶1 |
B. 易溶于苯、 易溶于苯、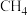 难溶于水,都可用“相似相溶”原理解释 难溶于水,都可用“相似相溶”原理解释 |
| C.键长越长,往往键能越大,共价键越稳定 |
| D.只含非极性键的分子一定是非极性分子,只含极性键的分子一定是极性分子 |
更新时间:2022/03/30 22:13:31
|
相似题推荐
单选题-单题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
A.键角: | B.酸性: |
| C.沸点:邻羟基苯甲醛>对羟基苯甲醛 | D.水中溶解度:乙醇>正戊醇 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实不能用键能的大小来解释的是
| A.N元素的电负性较大,但N2的化学性质很稳定 |
| B.稀有气体一般难发生反应 |
| C.HF、HCl、HBr、HI的稳定性逐渐减弱 |
| D.O2比N2更容易与H2反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】二茂铁是由环戊二烯阴离子( ,平面结构)与
,平面结构)与 形成的分子,其结构如下图所示。下列说法正确的是
形成的分子,其结构如下图所示。下列说法正确的是

 ,平面结构)与
,平面结构)与 形成的分子,其结构如下图所示。下列说法正确的是
形成的分子,其结构如下图所示。下列说法正确的是
A.铁元素位于 区 区 |
B.二茂铁中 与环戊二烯阴离子之间为离子键 与环戊二烯阴离子之间为离子键 |
| C.二茂铁易溶于苯、乙醚等有机溶剂 |
D.环戊二烯阴离子中碳原子的杂化方式有 和 和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中正确的是
A.ClO 的空间结构为平面三角形 的空间结构为平面三角形 |
| B.CS2为直线形的非极性分子,形成分子晶体 |
| C.氯化硼(BCl3)的熔点为-107℃,氯化硼液态时能导电而固态时不导电 |
D.SiF4和SO 的中心原子均为sp3杂化,二者均呈正四面体形 的中心原子均为sp3杂化,二者均呈正四面体形 |
您最近一年使用:0次
【推荐3】五种前四周期的元素X、Y、Z、Q、T。已知X元素基态原子的M层有6种运动状态不同的电子;Y原子的价电子构型为3d84s2,基态Z原子的L层p能级有一个空轨道;Q原子的L电子层的p能级只有一对成对电子;基态T原子的M电子层上p轨道半充满。下列说法错误的是
| A.Y、Q及氢三种元素形成的某化合物,能用于制作可充电电池的电极材料 |
| B.若X、T、Z的最高价的氧化物对应的水化物分别为u、v、w,则酸性为:u>v>w。理由是含氧酸酸性与非羟基氧原子数有关 |
| C.X、Y、T三种元素第一电离能的大小次序是:X>T>Y |
| D.化合物ZQ2、ZX2均是由极性键构成的非极性分子 |
您最近一年使用:0次



