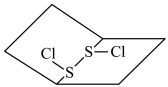
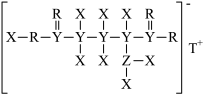
下列叙述中正确的是
A.ClO 的空间结构为平面三角形 的空间结构为平面三角形 |
| B.CS2为直线形的非极性分子,形成分子晶体 |
| C.氯化硼(BCl3)的熔点为-107℃,氯化硼液态时能导电而固态时不导电 |
D.SiF4和SO 的中心原子均为sp3杂化,二者均呈正四面体形 的中心原子均为sp3杂化,二者均呈正四面体形 |
更新时间:2024-01-16 19:48:16
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】从微粒结构角度分析,下列说法正确的是
A.三氧化硫有单分子气体和三聚分子固体( )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
B. 中 中 原子采用 原子采用 杂化, 杂化, 离子的空间构型为平面正方形 离子的空间构型为平面正方形 |
C.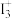 的空间结构为V形,中心原子的杂化方式为 的空间结构为V形,中心原子的杂化方式为 |
D. 配合物 配合物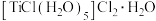 和足量硝酸银溶液反应,能产生 和足量硝酸银溶液反应,能产生 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列分子和离子的中心原子的价层电子对几何构型为四面体而分子或离子的空间构型为V形的是( )
| A.NH4+ | B.PH3 | C.H3O+ | D.H2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.在SCl2中,中心原子S采取sp杂化轨道成键 |
| B.凡是中心原子采取sp3杂化的分子,其立体构型都是正四面体形 |
| C.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现有四种元素基态原子的电子排布式如下,则下列有关比较中不正确的是
① ②
② ③
③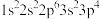 ④
④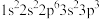
①
 ②
② ③
③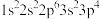 ④
④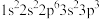
| A.电负性:①>②>④ |
| B.第一电离能:①>②>③>④ |
| C.原子半径:④>②>① |
D.②、③的简单氢化物,中心原子均为 杂化,且均为极性分子 杂化,且均为极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某溴丁烷与乙醇反应的能量转化如图(“ ”表示过渡态)。下列说法错误的是
”表示过渡态)。下列说法错误的是

 ”表示过渡态)。下列说法错误的是
”表示过渡态)。下列说法错误的是
| A.总反应为取代反应 |
| B.该反应过程中C原子杂化方式有变化 |
| C.反应过程中(CH3)3C+是中间产物 |
| D.决定该过程正反应快慢的步骤与逆反应快慢的步骤互为可逆反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的五种短周期非金属元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。

A. 的键角大于 的键角大于 的键角 的键角 | B.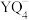 的VSEPR模型为正四面体形 的VSEPR模型为正四面体形 |
C.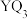 是极性分子, 是极性分子, 是非极性分子 是非极性分子 | D.M2的键能小于Q2的键能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中错误的是
| A.SO2、SO3都是极性分子 |
B.在 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.CO可以和很多金属形成配合物,如Ni(CO)2,Ni与CO之间的键型为配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上可用 处理水体中的氨氮(NH3、NH
处理水体中的氨氮(NH3、NH )生成
)生成 。下列说法正确的是
。下列说法正确的是
 处理水体中的氨氮(NH3、NH
处理水体中的氨氮(NH3、NH )生成
)生成 。下列说法正确的是
。下列说法正确的是A.原子半径: |
B.电负性: |
C. 属于分子晶体 属于分子晶体 |
D.第一电离能: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是
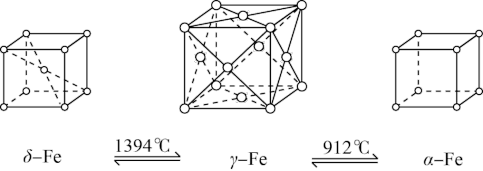

| A.δFe晶体中与每个铁原子等距离且最近的铁原子有8个 |
| B.αFe晶体中与每个铁原子等距离且最近的铁原子有6个 |
| C.若δFe晶胞边长为a cm,αFe晶胞边长为b cm,则两种晶体密度比为2b3∶a3 |
| D.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型相同 |
您最近一年使用:0次

 和
和 的空间结构不同,所以中心S原子杂化方式也不同
的空间结构不同,所以中心S原子杂化方式也不同