下列实验操作正确的是
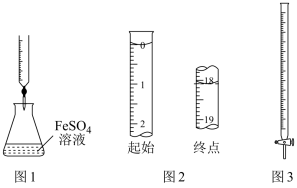

| A.用图1装置进行KMnO4溶液滴定未知浓度的FeSO4溶液实验 |
| B.如图2所示,记录滴定终点读数为19.90 mL |
| C.图3用盐酸标准溶液滴定未知浓度的NaOH,达到滴定终点时发现滴定管尖嘴部分有悬滴,会使测定结果偏小 |
| D.利用“Ag++SCN-=AgSCN↓”原理,可用标准KSCN溶液测AgNO3溶液浓度:Fe(NO3)3为指示剂,滴定终点的现象为溶液变为血红色 |
更新时间:2022-04-14 16:08:55
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验操作规范且能达到目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 取 酸性高锰酸钾溶液 酸性高锰酸钾溶液 | 在规格为 的酸式滴定管中装入酸性高锰酸钾溶液,调整初始读数为 的酸式滴定管中装入酸性高锰酸钾溶液,调整初始读数为 ,将剩余溶液放入锥形瓶中 ,将剩余溶液放入锥形瓶中 |
| B | 制备氢氧化铁胶体 | 将饱和硫酸铁溶液加入沸水中并煮沸至液体呈红褐色 |
| C | 测定次氯酸钠溶液的 | 用玻璃棒蘸取待测液,点在干燥的 试纸上 试纸上 |
| D | 配制氯化亚铁溶液 | 将氯化亚铁固体溶于蒸馏水中,并加入少量盐酸和还原铁粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项实验基本操作中,正确的是
| A.在做中和滴定实验时用蒸馏水清洗锥形瓶后,直接开始滴定实验 |
| B.为了加快锌和硫酸反应的速率,可将稀硫酸改为浓硫酸 |
| C.为了加快过滤速度,用玻璃棒搅拌漏斗中的液体 |
| D.蒸干AlCl3溶液制无水AlCl3固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图示与对应的叙述相符的是
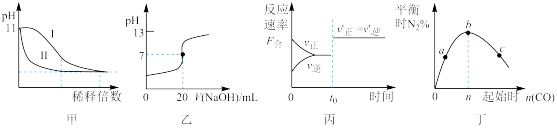

| A.图甲表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水 |
| B.图乙表示常温下,0.1000mol∙L-1NaOH 溶液滴定20.00mL0.1000mol∙L-1醋酸溶液的滴定曲线 |
C.图丙表示某可逆反应的反应速率随时间的变化,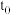 时刻改变的条件一定是使用了催化剂 时刻改变的条件一定是使用了催化剂 |
D.图丁表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列装置图或曲线图与对应的叙述不相符的是
 |  |  |  |
| 图1 | 图2 | 图3 | 图4 |
| A.图1:用0.1mol/L NaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| B.图2:酸性KMnO4溶液颜色会逐渐变浅乃至褪去 |
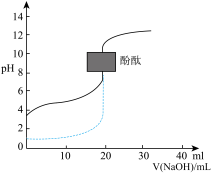
C.图3:用0.1mol/L CH3COOH溶液漓定20mL0.1mo/L NaOH溶液的滴定曲线,当pH=7时: |
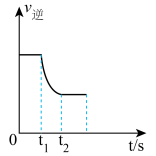
D.图4:表示 的v逆随时间变化曲线,由图知t1时刻可能减小了N2的浓度 的v逆随时间变化曲线,由图知t1时刻可能减小了N2的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
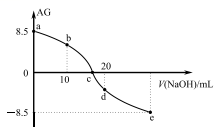
【推荐3】化学上常用AG表示溶液中的lg 。25℃时,用0.100 mol/L 的NaOH溶液滴定20.00 mL 0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100 mol/L 的NaOH溶液滴定20.00 mL 0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
 。25℃时,用0.100 mol/L 的NaOH溶液滴定20.00 mL 0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100 mol/L 的NaOH溶液滴定20.00 mL 0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
A.随着NaOH溶液的加入, 增大 增大 |
| B.25 ℃时,HNO2的电离常数Ka≈1.0×10-4.5 |
C.b点溶液中存在2c(H+)-2c(OH-)=c( )-c(HNO2) )-c(HNO2) |
| D.a、b、c、d、e五点的溶液中,水的电离程度最大的点是d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用标准盐酸溶液滴定未知浓度的NaOH溶液(酚酞作指示剂),下列操作中可能使所测NaOH溶液的浓度数值偏低的有:(1)酸式滴定管未用标准溶液润洗(2)锥形瓶用待测溶液润洗(3)锥形瓶洗净后还留有蒸馏水(4)放出碱液的滴定管开始有气泡,放出液体后气泡消失(5)酸式滴定管滴定前有气泡,滴定终点时气泡消失(6)部分酸液滴出锥形瓶外(7)酸式滴定管滴定前读数正确,滴定后俯视读数(8)酸式滴定管滴定前读数正确,滴定后仰视读数
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法中正确的是
A. 水解: 水解: +H2O +H2O  +H3O+ +H3O+ |
| B.中和滴定时眼睛必须注意锥形瓶内溶液颜色的变化 |
| C.电解水生成H2和O2的实验中,可加入少量盐酸或硫酸增强导电性 |
| D.用等浓度(0.5 mol•L﹣1)等体积(50 mL)的NaOH溶液与盐酸混合测定中和热 |
您最近一年使用:0次

 有毒,不能用作食品添加剂
有毒,不能用作食品添加剂

