镁-次氯酸钠电池在可移动电子设备电源等方面应用前景广阔,该电池的总反应为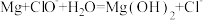 ,其工作原理如图所示。请回答下列问题。
,其工作原理如图所示。请回答下列问题。
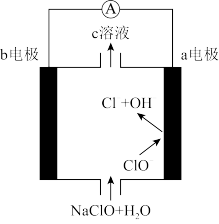
(1)该电池的负极是_______ (填“a”或“b”)电极,该电池工作时导线中电流流向为_______ (填“a→b”或“b→a”)。
(2)a电极的电极反应式为_______ 。
(3)c溶液中的溶质为_______ (填化学式)。
(4)当电路中通过0.2mol电子时,溶液中产生 的物质的量为
的物质的量为_______ 。
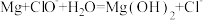 ,其工作原理如图所示。请回答下列问题。
,其工作原理如图所示。请回答下列问题。
(1)该电池的负极是
(2)a电极的电极反应式为
(3)c溶液中的溶质为
(4)当电路中通过0.2mol电子时,溶液中产生
 的物质的量为
的物质的量为
更新时间:2022/04/23 20:45:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某学生进行下图所示的锌铜原电池的实验:
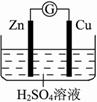
(1)从理论上讲,预期看到的现象是__________________________________ 。
(2)实验过程中,观察到锌极上有少量气泡逸出,铜极上有大量气泡逸出。试解释:
_________________________________________________________________

(1)从理论上讲,预期看到的现象是
(2)实验过程中,观察到锌极上有少量气泡逸出,铜极上有大量气泡逸出。试解释:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学为了探究原电池产生电流的过程,设计了如图实验。
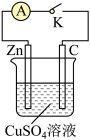
(1)打开K,观察到的现象为________________ 。
(2)关闭K,观察到的现象是_________ 。此电池的负极的电极反应式为_____ 。
(3)关闭K,溶液中阳离子向_______ (填“Zn”或“C”)极移动,外电路中,电子流动方向是________ 。

(1)打开K,观察到的现象为
(2)关闭K,观察到的现象是
(3)关闭K,溶液中阳离子向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】将A、B两个电极,分别用接线柱平行地固定在一块塑料板上,与电流表连结,插入盛有溶液C的小烧杯中。试回答下列问题:
(1)若A、B分别为铜和铝C为浓 ,原电池的负极为
,原电池的负极为_______ (填“铝”或“铜”)极,铝片上的电极反应式为:_______ 。
(2)若A、B分别为镁和铝,C为氢氧化钠溶液,原电池的负极为_______ (填“铝”或“镁”)极铝片上的电极反应式为:_______ 。
(3)若A、B分别为碳和铝,C为氯化钠溶液,原电池正极上的电极反应式为:_______ 。
(1)若A、B分别为铜和铝C为浓
 ,原电池的负极为
,原电池的负极为(2)若A、B分别为镁和铝,C为氢氧化钠溶液,原电池的负极为
(3)若A、B分别为碳和铝,C为氯化钠溶液,原电池正极上的电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NH3和O2可以形成碱性燃料电池,结构如图所示。
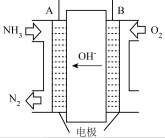
(1)电极A是_______ (填“正极”或“负极”),其电极反应式为_______ 。
(2)若反应生成28 gN2,则该燃料电池理论上消耗的O2的体积(在标准状况下)为_______ L。
(3)若用该电池电解精炼铜,通氧气一端的电极应接_______ (填“纯铜”或“粗铜”)。若用CuSO4溶液做电解液电解精练铜,则电解一段时间后CuSO4溶液的浓度_______ (填增大、变小、不变)。

(1)电极A是
(2)若反应生成28 gN2,则该燃料电池理论上消耗的O2的体积(在标准状况下)为
(3)若用该电池电解精炼铜,通氧气一端的电极应接
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图1、图2。
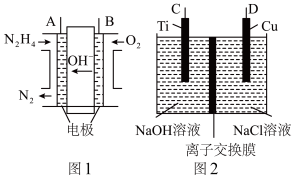
(1)①肼燃料电池中A极发生的电极反应为___________ 。
②上述装置中D电极应连接肼燃料电池的___________ 极(填“A”或“B”),该电解池的阳极反应式为___________ 。
③当反应生成14.4gCu2O时,停止电解,至少需要肼___________ mol,通过离子交换膜的阴离子的物质的量为___________ mol。(离子交换膜只允许OH-通过)
(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2也可制备纳米级Cu2O,同时放出N2,该反应的化学方程式为___________ 。
(3)发射火箭时以液态肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。已知:①2H2O2(1)=2H2O(l)+O2(g) △H=-196kJmol-1;②H2O(l)=H2O(g) △H=43.98kJmol-1;③肼的燃烧热为-622.08kJmol-1。写出上述反应的热化学方程式___________ 。

(1)①肼燃料电池中A极发生的电极反应为
②上述装置中D电极应连接肼燃料电池的
③当反应生成14.4gCu2O时,停止电解,至少需要肼
(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2也可制备纳米级Cu2O,同时放出N2,该反应的化学方程式为
(3)发射火箭时以液态肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。已知:①2H2O2(1)=2H2O(l)+O2(g) △H=-196kJmol-1;②H2O(l)=H2O(g) △H=43.98kJmol-1;③肼的燃烧热为-622.08kJmol-1。写出上述反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】图中甲池的总反应式为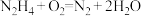 。
。

(1)甲池中负极上的电极反应式为_____________________ 。
(2)乙池中石墨电极上电极反应式为_________________________________ 。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的_______________ 。
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_________________ g。
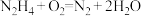 。
。
(1)甲池中负极上的电极反应式为
(2)乙池中石墨电极上电极反应式为
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示。请回答下列问题:
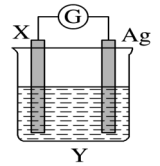
(1)电解质溶液Y是_______ 。
(2)银电极为电池的_______ 极,发生的电极反应式为_______ ;
(3)外电路中的电子_______ (填“流出”或“流入”)Ag电极。
(4)当有1.6g铜溶解时,银棒增重_______ g。

(1)电解质溶液Y是
(2)银电极为电池的
(3)外电路中的电子
(4)当有1.6g铜溶解时,银棒增重
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极的电极反应方程式为:___________ 。当被腐蚀的铜的质量为12.8 g时,则电路中转移电子的数目为___________ 。
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___________ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的正极反应方程式是:___________ 。
②电池工作一段时间后硫酸溶液的浓度___________ (填“增大”“减小”或“不变”)。
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的正极反应方程式是:
②电池工作一段时间后硫酸溶液的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢能是发展中的新能源,它的利用包括氢的制备和储存。回答下列问题:
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
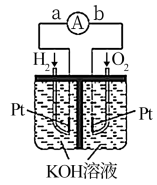
①在导线中电子流动方向为_______ (用a、b表示)
②正极反应式为_______ 。
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应: 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是_______ 。
a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为_______ mol。
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为
②正极反应式为
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:
 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2
 2LiH
2LiH Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近一年使用:0次



