能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题。回答下列问题:
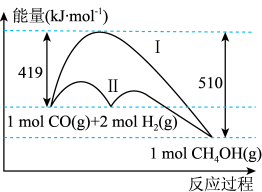
(1)工业上用CO生产燃料甲醇,一定条件下发生反应: ,反应过程中的能量变化情况如图所示。曲线
,反应过程中的能量变化情况如图所示。曲线_______ (选填“Ⅰ”或“Ⅱ”)表示使用催化剂的反应过程。计算当反应生成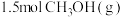 时,能量变化值是
时,能量变化值是_______ kJ。
(2)用 表示阿伏加德罗常数,在
表示阿伏加德罗常数,在 (气态)完全燃烧生成
(气态)完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有 个电子转移时,放出650kJ的热量。其燃烧热的热化学方程式为
个电子转移时,放出650kJ的热量。其燃烧热的热化学方程式为_______ 。
(3)已知拆开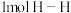 键、
键、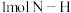 键、
键、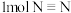 键分别需要的能量是436kJ、391kJ、946kJ,则
键分别需要的能量是436kJ、391kJ、946kJ,则 与
与 反应生成
反应生成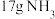 需放出的热量为
需放出的热量为_______ kJ。
(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳的排放。有一种用 生产甲醇燃料的方法:
生产甲醇燃料的方法:
已知:①

②

③

④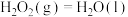

则表示 燃烧生成
燃烧生成 气体和液态水的反应热
气体和液态水的反应热 为
为_______  (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
(5)已知乙醇的燃烧热为 。已知单位质量的燃料完全燃烧时所放出的热量称为该燃料的热值,则乙醇的热值是
。已知单位质量的燃料完全燃烧时所放出的热量称为该燃料的热值,则乙醇的热值是_______  。(取小数点后一位)
。(取小数点后一位)
(1)工业上用CO生产燃料甲醇,一定条件下发生反应:
 ,反应过程中的能量变化情况如图所示。曲线
,反应过程中的能量变化情况如图所示。曲线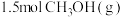 时,能量变化值是
时,能量变化值是
(2)用
 表示阿伏加德罗常数,在
表示阿伏加德罗常数,在 (气态)完全燃烧生成
(气态)完全燃烧生成 和液态水的反应中,每有
和液态水的反应中,每有 个电子转移时,放出650kJ的热量。其燃烧热的热化学方程式为
个电子转移时,放出650kJ的热量。其燃烧热的热化学方程式为(3)已知拆开
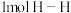 键、
键、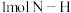 键、
键、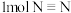 键分别需要的能量是436kJ、391kJ、946kJ,则
键分别需要的能量是436kJ、391kJ、946kJ,则 与
与 反应生成
反应生成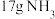 需放出的热量为
需放出的热量为(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳的排放。有一种用
 生产甲醇燃料的方法:
生产甲醇燃料的方法:已知:①


②


③


④
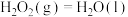

则表示
 燃烧生成
燃烧生成 气体和液态水的反应热
气体和液态水的反应热 为
为 (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。(5)已知乙醇的燃烧热为
 。已知单位质量的燃料完全燃烧时所放出的热量称为该燃料的热值,则乙醇的热值是
。已知单位质量的燃料完全燃烧时所放出的热量称为该燃料的热值,则乙醇的热值是 。(取小数点后一位)
。(取小数点后一位)
更新时间:2022-04-22 11:53:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知下列热化学方程式:①H2(g)+ O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+
O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+ O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+
O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+  O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
(1)上述反应中属于放热反应的是_______ 。(填序号)
(2)H2的燃烧热为___ ;C的燃烧热为____ 。
(3)燃烧4g H2生成液态水,放出的热量为_______ 。
(4)根据盖斯定律可知CO的燃烧热为_____ ;其热化学方程式为_____ 。
(5)比较下列各组热化学方程式中△H的大小:
①C(s)+O2(g)=CO2(g)△H1 C(s)+ O2(g)=CO(g) △H2 △H1
O2(g)=CO(g) △H2 △H1 ____ △H2
②S(s)+O2(g)=SO2(g)△H3 S(g)+O2(g)=SO2(g) △H4 △H3__ △H4
 O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+
O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+ O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+
O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+  O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧4g H2生成液态水,放出的热量为
(4)根据盖斯定律可知CO的燃烧热为
(5)比较下列各组热化学方程式中△H的大小:
①C(s)+O2(g)=CO2(g)△H1 C(s)+
 O2(g)=CO(g) △H2 △H1
O2(g)=CO(g) △H2 △H1 ②S(s)+O2(g)=SO2(g)△H3 S(g)+O2(g)=SO2(g) △H4 △H3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应的过程,既有物质的转化过程,也是化学能与热等其他形式能量的转化过程。
Ⅰ.已知某反应 过程中的能量变化如图所示,回答问题。
过程中的能量变化如图所示,回答问题。
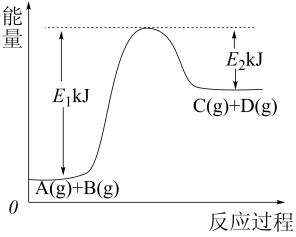
(1)该反应是___________ (填“吸热”或“放热”)反应,该反应的 =
=___________ kJ/mol(用含E1、E2的代数式表示)。
(2)1mol气体A和1mol气体B具有的总能量___________ (填“>”“<”或“=”)1mol气体C和1mol气体D具有的总能量。
Ⅱ.发射卫星时可用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,两者反应生成氮气和气态水。
已知: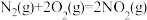
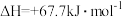

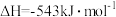
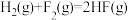
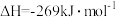
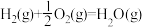
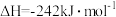
(3)N2H4 (g)和NO2(g)反应的热化学方程式为___________ ;
(4)有人认为若用氟单质代替二氧化氮作为氧化剂,则反应释放能量更多,N2H4 (g)和F2(g)反应的热化学方程式为___________ 。
Ⅲ.有机物通常能发生燃烧,对应的反应往往都有重要用途。
(5)在25℃、101k Pa条件下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程为___________ 。
(6)用NA表示阿伏加德罗常数的值,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。则该反应的热化学方程式为___________ 。
Ⅰ.已知某反应
 过程中的能量变化如图所示,回答问题。
过程中的能量变化如图所示,回答问题。
(1)该反应是
 =
=(2)1mol气体A和1mol气体B具有的总能量
Ⅱ.发射卫星时可用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,两者反应生成氮气和气态水。
已知:
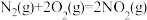
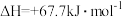

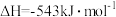
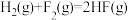
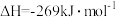
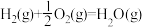
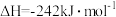
(3)N2H4 (g)和NO2(g)反应的热化学方程式为
(4)有人认为若用氟单质代替二氧化氮作为氧化剂,则反应释放能量更多,N2H4 (g)和F2(g)反应的热化学方程式为
Ⅲ.有机物通常能发生燃烧,对应的反应往往都有重要用途。
(5)在25℃、101k Pa条件下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程为
(6)用NA表示阿伏加德罗常数的值,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请按照要求完成下列填空。
(1)在配制 的氯化钠溶液过程中,以下可能导致所配溶液浓度偏低的是
的氯化钠溶液过程中,以下可能导致所配溶液浓度偏低的是
(2)请写出实验室制乙炔的反应方程式___________ 制取的乙炔常含有硫化氢等杂质,用___________ 溶液除去。
(3)葡萄酒中通常要加 作为抗氧化剂和保鲜剂,为测定
作为抗氧化剂和保鲜剂,为测定 的含量通常用酸性高锰酸钾滴定的方法,请写出该反应原理的离子方程式:
的含量通常用酸性高锰酸钾滴定的方法,请写出该反应原理的离子方程式:___________
(4)漂白剂和洁厕灵(含盐酸)同时使用会使人中毒是什么原因呢?请用离子方程式解释:___________
(5)25℃,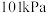 时,32g甲烷在足量的氧气中完全燃烧放出
时,32g甲烷在足量的氧气中完全燃烧放出 的热量,请写出甲烷燃烧热的热化学方程式:
的热量,请写出甲烷燃烧热的热化学方程式:___________
(1)在配制
 的氯化钠溶液过程中,以下可能导致所配溶液浓度偏低的是
的氯化钠溶液过程中,以下可能导致所配溶液浓度偏低的是| A.氯化钠固体不纯 | B.定容时仰视读数 |
| C.装瓶时有少量溶液洒出 | D.称量时砝码端忘垫质量相同的纸片 |
(3)葡萄酒中通常要加
 作为抗氧化剂和保鲜剂,为测定
作为抗氧化剂和保鲜剂,为测定 的含量通常用酸性高锰酸钾滴定的方法,请写出该反应原理的离子方程式:
的含量通常用酸性高锰酸钾滴定的方法,请写出该反应原理的离子方程式:(4)漂白剂和洁厕灵(含盐酸)同时使用会使人中毒是什么原因呢?请用离子方程式解释:
(5)25℃,
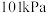 时,32g甲烷在足量的氧气中完全燃烧放出
时,32g甲烷在足量的氧气中完全燃烧放出 的热量,请写出甲烷燃烧热的热化学方程式:
的热量,请写出甲烷燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.利用CO2合成淀粉是实现碳中和的有效途径,其成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:已知:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H
CH3OH(g)+H2O(g) ∆H
②CO(g)+2H2(g) CH3OH(g) ∆H=-99kJ∙mol-1
CH3OH(g) ∆H=-99kJ∙mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) ∆H=+41kJ∙mol-1
CO(g)+H2O(g) ∆H=+41kJ∙mol-1
(1)反应①中∆H =_______ ;该反应的自发条件是_______ (填“高温自发”“低温自发”或“任何温度下都自发”)。
(2)对于反应①CO2(g)+3H2(g) CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),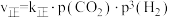 ,
,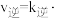
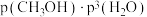 。其中
。其中 、
、 分别为正逆反应速率常数,p为气体分压,(分压=物质的量分数×总压)。
分别为正逆反应速率常数,p为气体分压,(分压=物质的量分数×总压)。
①升高温度,
_______ (填“变大”“变小”或“不变”)。
在540K下,按初始投料比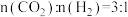 、
、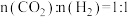 、
、 ,得到不同压强条件下CO2的平衡转化率关系图:
,得到不同压强条件下CO2的平衡转化率关系图:

②比较a、b、c各曲线所表示的投料比大小顺序为_______ (用字母表示)。
③计算540K下压强平衡常数Kp=_______ (MPa)-2(用分压代替浓度)。
Ⅱ.若以 (g)为燃料设计原电池,其反应原理如图所示。请回答下列问题:
(g)为燃料设计原电池,其反应原理如图所示。请回答下列问题:

(3)该电池中电极a是_______ 极(填“正”或“负”)。
(4)该电池的b极反应式为_______ 。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H
CH3OH(g)+H2O(g) ∆H②CO(g)+2H2(g)
 CH3OH(g) ∆H=-99kJ∙mol-1
CH3OH(g) ∆H=-99kJ∙mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H=+41kJ∙mol-1
CO(g)+H2O(g) ∆H=+41kJ∙mol-1(1)反应①中∆H =
(2)对于反应①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),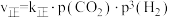 ,
,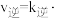
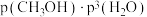 。其中
。其中 、
、 分别为正逆反应速率常数,p为气体分压,(分压=物质的量分数×总压)。
分别为正逆反应速率常数,p为气体分压,(分压=物质的量分数×总压)。①升高温度,

在540K下,按初始投料比
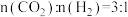 、
、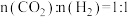 、
、 ,得到不同压强条件下CO2的平衡转化率关系图:
,得到不同压强条件下CO2的平衡转化率关系图:
②比较a、b、c各曲线所表示的投料比大小顺序为
③计算540K下压强平衡常数Kp=
Ⅱ.若以
 (g)为燃料设计原电池,其反应原理如图所示。请回答下列问题:
(g)为燃料设计原电池,其反应原理如图所示。请回答下列问题:
(3)该电池中电极a是
(4)该电池的b极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】甲烷是一种重要的化工原料,常用于制H2和CO。
(1)CH4和H2O(g) 在一定条件下可制得H2和CO,反应原理如下:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH1=-165 kJ·mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41 kJ·mol-1
③CH4(g)+H2O(g) =CO(g)+3H2(g) ΔH3
反应③的ΔH3=_______ 。
(2)甲烷裂解制氢的反应为CH4(g)=C(s)+2H2(g) ΔH=+75 kJ·mol-1,Ni和活性炭均可作该反应催化剂。CH4在催化剂孔道表面反应,若孔道堵塞会导致催化剂失活。
①Ni催化剂可用NiC2O4·2H2O晶体在氩气环境中受热分解制备,该反应方程式为_______ 。
②向反应系统中通入水蒸气可有效减少催化剂失活,其原因是_______ 。
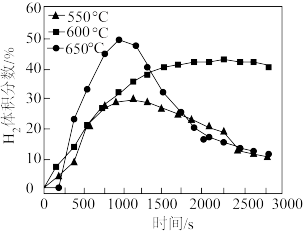
③使用Ni催化剂,且其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如图所示。使用催化剂的最佳温度为_______ 。
④650℃条件下,1 000 s后,氢气的体积分数快速下降的原因为_______ 。
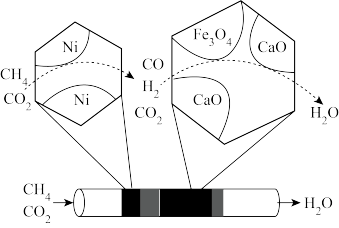
(3)甲烷、二氧化碳重整制CO经历过程I、Ⅱ。过程I如图所示,可描述为_______ ;过程Ⅱ保持温度不变,再通入惰性气体,CaCO3分解产生CO2,Fe 将CO2还原得到CO和Fe3O4。
(1)CH4和H2O(g) 在一定条件下可制得H2和CO,反应原理如下:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH1=-165 kJ·mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41 kJ·mol-1
③CH4(g)+H2O(g) =CO(g)+3H2(g) ΔH3
反应③的ΔH3=
(2)甲烷裂解制氢的反应为CH4(g)=C(s)+2H2(g) ΔH=+75 kJ·mol-1,Ni和活性炭均可作该反应催化剂。CH4在催化剂孔道表面反应,若孔道堵塞会导致催化剂失活。
①Ni催化剂可用NiC2O4·2H2O晶体在氩气环境中受热分解制备,该反应方程式为
②向反应系统中通入水蒸气可有效减少催化剂失活,其原因是
③使用Ni催化剂,且其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如图所示。使用催化剂的最佳温度为
④650℃条件下,1 000 s后,氢气的体积分数快速下降的原因为

(3)甲烷、二氧化碳重整制CO经历过程I、Ⅱ。过程I如图所示,可描述为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列填空:
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为_______ 。
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,表示氢气燃烧热的热化学方程式为_______ 。
(3)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该反应的热化学方程式:_______ 。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(5)已知:H2O(g)=H2O(l) ∆H=-44 kJ/mol;
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ∆H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:_______ 。
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,表示氢气燃烧热的热化学方程式为
(3)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该反应的热化学方程式:
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式
(5)已知:H2O(g)=H2O(l) ∆H=-44 kJ/mol;
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ∆H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成 P4O6,空气充足时生成 P4O10。
(1)已知 298K 时白磷、红磷完全燃烧的热化学方程式分别为
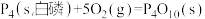 △H1 =-2983.2kJ/mol
△H1 =-2983.2kJ/mol
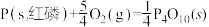 △H2 =-738.5kJ/mol
△H2 =-738.5kJ/mol
则该温度下白磷转化为红磷的热化学方程式为________________________ .
(2)已知 298K 时白磷不完全燃烧的热化学方程式为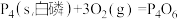 △H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为
△H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为________________ ,反应过程中放出的热为_________________
(3)已知白磷和 PCl3 的分子结构如图所示,现提供以下化学键的键能(KJ/mol):P-P:198, Cl-Cl:243, P-Cl :331 .
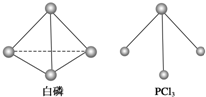
则反应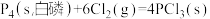 的反应热 △H2 =
的反应热 △H2 =__________ .
(1)已知 298K 时白磷、红磷完全燃烧的热化学方程式分别为
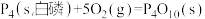 △H1 =-2983.2kJ/mol
△H1 =-2983.2kJ/mol 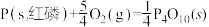 △H2 =-738.5kJ/mol
△H2 =-738.5kJ/mol 则该温度下白磷转化为红磷的热化学方程式为
(2)已知 298K 时白磷不完全燃烧的热化学方程式为
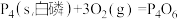 △H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为
△H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为(3)已知白磷和 PCl3 的分子结构如图所示,现提供以下化学键的键能(KJ/mol):P-P:198, Cl-Cl:243, P-Cl :331 .

则反应
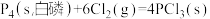 的反应热 △H2 =
的反应热 △H2 =
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】H2SO4溶液和KOH溶液反应时有热量放出,已知反应物的总能量为E1,生成物的总能量为E2。试回答下列问题:
(1)用离子方程式表示中和反应的实质_______________ 。
(2)判断E1和E2的大小关系:E1___ E2。
(3)已知H+(aq)+OH−(aq)=H2O(l) ΔH=−57.3 kJ/mol,计算下列中和反应中放出的热量。
①用20 g NaOH配成稀溶液与足量稀盐酸反应,能放出___ kJ的热量。
②用0.1 mol Ba(OH)2配成稀溶液跟足量稀硝酸反应,能放出___ kJ的热量。
(1)用离子方程式表示中和反应的实质
(2)判断E1和E2的大小关系:E1
(3)已知H+(aq)+OH−(aq)=H2O(l) ΔH=−57.3 kJ/mol,计算下列中和反应中放出的热量。
①用20 g NaOH配成稀溶液与足量稀盐酸反应,能放出
②用0.1 mol Ba(OH)2配成稀溶液跟足量稀硝酸反应,能放出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
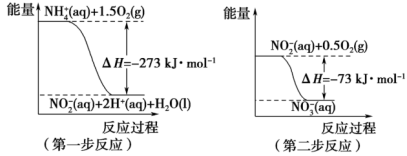
①第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
②1mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(2)已知:
① △H=-566kJ·mol-1
△H=-566kJ·mol-1
②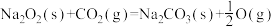 △H=-226 kJ·mol-1
△H=-226 kJ·mol-1
则CO(g)与Na2O2(s)反应放出509kJ热量时,消耗CO的物质的量为_______ 。
(3)已知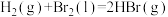 △H=-72kJ·mol-1,蒸发1ml Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:
△H=-72kJ·mol-1,蒸发1ml Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=_______ 。
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)已知:
①
 △H=-566kJ·mol-1
△H=-566kJ·mol-1②
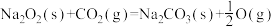 △H=-226 kJ·mol-1
△H=-226 kJ·mol-1则CO(g)与Na2O2(s)反应放出509kJ热量时,消耗CO的物质的量为
(3)已知
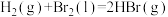 △H=-72kJ·mol-1,蒸发1ml Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:
△H=-72kJ·mol-1,蒸发1ml Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | a |
则表中a=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时电极反应式为负极:C6Li-xe-=C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)正极:Li1-xMO2+xLi++xe-=LiMO2(LiMO2表示含锂的过渡金属氧化物)。
(1)锂电池放电时电池的反应式为_______ 。
(2)假设放电过程中消耗负极材料5.6 g,转移的电子数目为_______ (NA为阿伏加德罗常数值)。
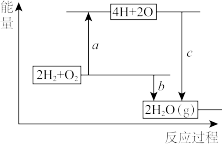
(3)已知破坏1 mol H-H键、1 mol O═O键、1mol H-O键时分别需要吸收436 kJ、498 kJ、465 kJ的能量。图表示H2、O2转化为水的反应过程能量变化,则b=_______ 。
(4)某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了如下平行实验:
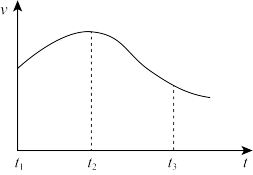
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示。
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
①试分析实验①中t1~t2速率增大的主要原因是_______ 。t2~t3速率减小的主要原因是_______ 。
②实验②放出氢气的量减少的原因是_______ 。
③某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?_______ (填“正确”或“不正确”)。请选择下列相应的a或b作答_______ 。
a.若不正确,请说明原因。
b.若正确则写出实验③中原电池的正极电极反应式。
(1)锂电池放电时电池的反应式为
(2)假设放电过程中消耗负极材料5.6 g,转移的电子数目为
(3)已知破坏1 mol H-H键、1 mol O═O键、1mol H-O键时分别需要吸收436 kJ、498 kJ、465 kJ的能量。图表示H2、O2转化为水的反应过程能量变化,则b=

(4)某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了如下平行实验:

实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示。
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
①试分析实验①中t1~t2速率增大的主要原因是
②实验②放出氢气的量减少的原因是
③某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?
a.若不正确,请说明原因。
b.若正确则写出实验③中原电池的正极电极反应式。
您最近一年使用:0次
【推荐2】回答下列问题:
(1)拆开lmolH—H键、lmolN—H键、lmolN≡N键分别需要的能量是akJ、bkJ、ckJ,则由氢气和氮气生成1molNH3(g)的反应热为___ 。
(2)在一定条件下,氢气和丙烷燃烧的化学方程式为:
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220kJ/mol
5mol氢气和丙烷的混合气完全燃烧时放热3847kJ,则氢气和甲烷的体积比为___ 。
(3)已知在一定温度下的可逆反应N2O4(g) 2NO2(g)ΔH>0中,v正=k正c(N2O4),v逆=k逆c2(NO2)(速率常数k正、k逆只是温度函数)。若该温度下的平衡常数K=10,则k正=
2NO2(g)ΔH>0中,v正=k正c(N2O4),v逆=k逆c2(NO2)(速率常数k正、k逆只是温度函数)。若该温度下的平衡常数K=10,则k正=___ k逆。升高温度,k正增大的倍数___ (填“大于”“小于”或“等于”)k逆增大的倍数。
(4)用一个离子反应方程式证明ClO-比CO 结合质子的能力弱:
结合质子的能力弱:___ 。
(5)KSCN为离子化合物,各原子均满足8电子稳定结构,KSCN的电子式为:___ 。
(6)溴乙烷的官能团名称:___ 。
(1)拆开lmolH—H键、lmolN—H键、lmolN≡N键分别需要的能量是akJ、bkJ、ckJ,则由氢气和氮气生成1molNH3(g)的反应热为
(2)在一定条件下,氢气和丙烷燃烧的化学方程式为:
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220kJ/mol
5mol氢气和丙烷的混合气完全燃烧时放热3847kJ,则氢气和甲烷的体积比为
(3)已知在一定温度下的可逆反应N2O4(g)
 2NO2(g)ΔH>0中,v正=k正c(N2O4),v逆=k逆c2(NO2)(速率常数k正、k逆只是温度函数)。若该温度下的平衡常数K=10,则k正=
2NO2(g)ΔH>0中,v正=k正c(N2O4),v逆=k逆c2(NO2)(速率常数k正、k逆只是温度函数)。若该温度下的平衡常数K=10,则k正=(4)用一个离子反应方程式证明ClO-比CO
 结合质子的能力弱:
结合质子的能力弱:(5)KSCN为离子化合物,各原子均满足8电子稳定结构,KSCN的电子式为:
(6)溴乙烷的官能团名称:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】肼( )是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
)是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
(1)已知:
①g表示物质的状态为气态。
②298K时,1mol物质的相对能量如图所示:
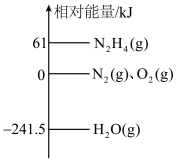
1mol (g)与足量
(g)与足量 (g)完全反应生成
(g)完全反应生成 (g)和
(g)和 (g)
(g)___________ (填吸收或释放)的能量为___________ kJ。
(2)298K时,1mol气态分子中的化学键断裂形成气态原子吸收的能量如下表所示:
a=___________  。
。
(3)根据 (g)与
(g)与 (g)的反应设计肼燃料电池,其工作原理如图所示。
(g)的反应设计肼燃料电池,其工作原理如图所示。
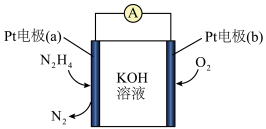
①下列说法正确的是___________ (填序号)。
A.电池工作时,将热能转化为电能 B.Pt电极a的电势低于Pt电极b
C.离子导体中, 向Pt电极b移动 D.电池工作时,KOH的物质的量不变
向Pt电极b移动 D.电池工作时,KOH的物质的量不变
②写出Pt电极a上的电极反应式___________ 。
 )是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
)是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:(1)已知:
①g表示物质的状态为气态。
②298K时,1mol物质的相对能量如图所示:

1mol
 (g)与足量
(g)与足量 (g)完全反应生成
(g)完全反应生成 (g)和
(g)和 (g)
(g)(2)298K时,1mol气态分子中的化学键断裂形成气态原子吸收的能量如下表所示:
 (g) (g) |  (g) (g) |  (g) (g) |  (g) (g) |
1757 | a  | 946 | 926 |
 。
。(3)根据
 (g)与
(g)与 (g)的反应设计肼燃料电池,其工作原理如图所示。
(g)的反应设计肼燃料电池,其工作原理如图所示。
①下列说法正确的是
A.电池工作时,将热能转化为电能 B.Pt电极a的电势低于Pt电极b
C.离子导体中,
 向Pt电极b移动 D.电池工作时,KOH的物质的量不变
向Pt电极b移动 D.电池工作时,KOH的物质的量不变②写出Pt电极a上的电极反应式
您最近一年使用:0次



