甲烷和乙烯是常见的两种有机化合物,在生产生活中有广泛的应用。
Ⅰ.以甲烷等碳氢化合物为燃料的新型燃料电池,成本大大低于以氢气为燃料的传统燃料电池。一种以甲烷为燃料的电池装置示意图如图。
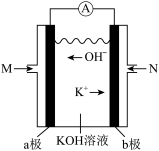
(1)N口通入的气体是_______ (填化学式)。
(2)外电路中电流的方向是由_______ 极到_______ 极(填“a”或“b”)。
(3)a极为_______ 极(填“正”或“负”),其电极方程式为_______ 。
(4)电路中每转移0.8mol电子,标准状况下消耗O2的体积是_______ L。
Ⅱ.石油裂解可得到重要的化工原料乙烯(CH2=CH2),有关乙烯的部分转化关系如图:
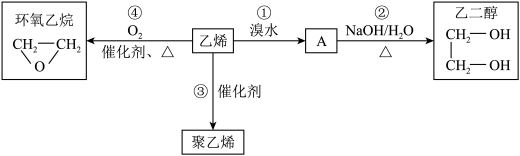
回答下列问题:
(5)写出A的结构简式:_______ 。
(6)②的反应类型为_______ 。
(7)反应③的化学方程式为_______ 。
(8)已知反应④的原子利用率为100%,其化学方程式为_______ 。
Ⅰ.以甲烷等碳氢化合物为燃料的新型燃料电池,成本大大低于以氢气为燃料的传统燃料电池。一种以甲烷为燃料的电池装置示意图如图。

(1)N口通入的气体是
(2)外电路中电流的方向是由
(3)a极为
(4)电路中每转移0.8mol电子,标准状况下消耗O2的体积是
Ⅱ.石油裂解可得到重要的化工原料乙烯(CH2=CH2),有关乙烯的部分转化关系如图:

回答下列问题:
(5)写出A的结构简式:
(6)②的反应类型为
(7)反应③的化学方程式为
(8)已知反应④的原子利用率为100%,其化学方程式为
更新时间:2022-05-03 11:21:34
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产生活提供能量。
Ⅰ.如图是某同学设计的一个简易的原电池装置,请回答下列问题。
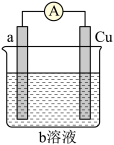
(1)若a电极材料为碳、b溶液为 溶液则正极的电极反应式为
溶液则正极的电极反应式为_______ ,当有3.2g的负极材料溶解时,导线中转移的电子的数目为_______ 。
(2)若a电极材料为铁、b溶液为稀硫酸,电流表的指针也会偏转,则电子的流向为_______ →_______ (填电极材料,下同),溶液中的 向
向_______ 极移动。
Ⅱ.水是生命之源,也是化学反应中的主角。
断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子,所吸收的能量称为A-B键的键能。列出了一些共价键的键能如表:
关于 的反应,请回答下列问题:
的反应,请回答下列问题:
(3)若有1mol 生成,需要
生成,需要_______ (填“吸收”或“放出”)热量_______ kJ;该反应的能量变化可用图_______ 表示(填“甲”或“乙”)

Ⅲ.天然气(主要成分 )和氧应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。
)和氧应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。
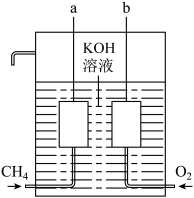
(4)b电极的电极反应式是_______ 。
Ⅰ.如图是某同学设计的一个简易的原电池装置,请回答下列问题。

(1)若a电极材料为碳、b溶液为
 溶液则正极的电极反应式为
溶液则正极的电极反应式为(2)若a电极材料为铁、b溶液为稀硫酸,电流表的指针也会偏转,则电子的流向为
 向
向Ⅱ.水是生命之源,也是化学反应中的主角。
断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子,所吸收的能量称为A-B键的键能。列出了一些共价键的键能如表:
| 共价键 | H-H | O=O | O-H |
| 键能 | 436kJ/mol | 498kJ/mol | 463kJ/mol |
关于
 的反应,请回答下列问题:
的反应,请回答下列问题:(3)若有1mol
 生成,需要
生成,需要
Ⅲ.天然气(主要成分
 )和氧应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。
)和氧应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。
(4)b电极的电极反应式是
您最近一年使用:0次
【推荐2】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g) 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。
已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol−1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol−1
C(s)+ O2(g)=CO(g)ΔH=-111kJ·mol−1
O2(g)=CO(g)ΔH=-111kJ·mol−1
该催化重整反应的ΔH=________ kJ·mol−1。有利于提高CH4平衡转化率的条件是____ (填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为___________________________ 。
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是________ ,负极反应式是_____________________________ 。
(3)正极现象是_______________________________________________ 。
(4)放电时OH-向_____________ (填“正极”或“负极”)移动。
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)
 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol−1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol−1
C(s)+
 O2(g)=CO(g)ΔH=-111kJ·mol−1
O2(g)=CO(g)ΔH=-111kJ·mol−1该催化重整反应的ΔH=
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是
(3)正极现象是
(4)放电时OH-向
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】填空。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O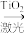 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为_______ 能;分解海水的反应属于_____ 反应(填“放热”或“吸热”)
(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式_______ 。
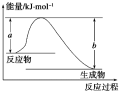
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=_______ kJ∙mol−1,x=________ 。
(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O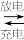 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为_____ 。
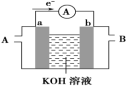
(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为______ 。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
| A.氢气分子内每个氢原子都达到稳定结构 |
| B.氢气分子的能量比两个氢原子的能量低 |
| C.1molH2离解成2molH要放出437.6kJ热量 |
| D.氢原子比氢气分子稳定 |
 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=

(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】观察图示,回答问题:
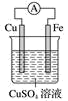
(1)负极是_______ ,电极反应式为_______ 。
(2)正极是_______ ,电极反应式为_______ 。
(3)电池总反应的离子方程式为_______ 。

(1)负极是
(2)正极是
(3)电池总反应的离子方程式为
您最近一年使用:0次
【推荐2】一定温度下,在2L的恒容密闭容器中充入1 mol CO和2mol H2,发生反应:CO(g)+2H2(g) CH3OH(g),
CH3OH(g),
测得CO(g)和CH3OH(g)的物质的量随时间变化如图1所示,反应过程中的能量变化如图2所示。___________ mol/(L·min)。
(2)改变下列条件对反应速率无影响的是___________ (填标号)。
(3)下列描述中能说明上述反应达到平衡状态的是___________(填标号)。
(4)平衡时H2的转化率为___________ ,平衡时压强与起始时压强之比为___________ 。
(5)已知断开1 mol CO(g)和2 mol H2(g)中的化学键需要吸收的能量为1944 kJ,则断开1 mol CH3OH(g)中的化学键所需要吸收___________ kJ的能量。
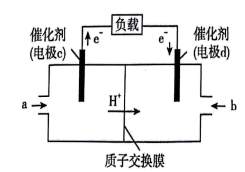
(6)CH3OH和O2形成的燃料电池的结构如下图所示。则电极c的反应式为___________ ,若转移2 mol电子,则消耗的O2在标准状况下的体积为___________ L。
 CH3OH(g),
CH3OH(g),测得CO(g)和CH3OH(g)的物质的量随时间变化如图1所示,反应过程中的能量变化如图2所示。
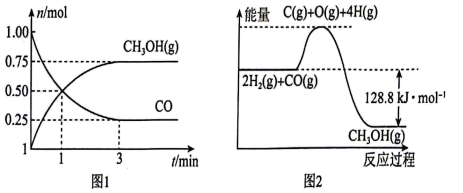
(2)改变下列条件对反应速率无影响的是___________ (填标号)。
| A.升高温度 | B.加入合适的催化剂 |
| C.保持压强不变,充入氩气 | D.保持体积不变,充入氩气 |
| A.混合气体的密度不随时间的变化而变化 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内消耗2 mol H2的同时生成1 mol CH3OH |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
(5)已知断开1 mol CO(g)和2 mol H2(g)中的化学键需要吸收的能量为1944 kJ,则断开1 mol CH3OH(g)中的化学键所需要吸收
(6)CH3OH和O2形成的燃料电池的结构如下图所示。则电极c的反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】I.回答下列问题:
(1)实验室用 固体配制240mL0.100mol∙L-1的
固体配制240mL0.100mol∙L-1的 溶液,需要的仪器有
溶液,需要的仪器有___________ 、胶头滴管、烧杯、玻璃棒、天平。
(2)下列配制的溶液浓度偏高的是___________ ;
A.称量 时,称量时间较长 B.配制前,容量瓶中有少量蒸馏水
时,称量时间较长 B.配制前,容量瓶中有少量蒸馏水
C.配制时, 未冷却直接定容 D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
未冷却直接定容 D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线 F.加蒸馏水时不慎加过了刻度线
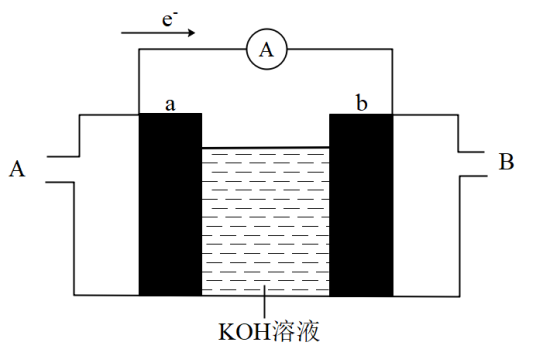
(3)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为___________
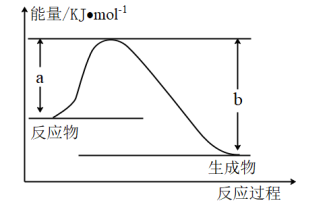
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+ O2(g)=H2O(g) 放出241.8 kJ能量,则b=
O2(g)=H2O(g) 放出241.8 kJ能量,则b=___________ kJ∙mol−1,x=___________
(5)铅蓄电池是可充电电池,放电时电池总反应为: PbO2+Pb+4H++2SO =2PbSO4+2H2O 则正极的电极反应式
=2PbSO4+2H2O 则正极的电极反应式___________ ;若负极质量增加48 g,则外电路通过电子数目是___________ 。
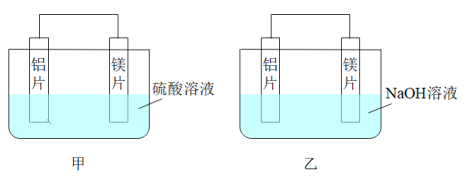
II.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。
(6)写出甲中正极的电极反应式:___________
(7)写出乙中负极的电极反应式:___________
(1)实验室用
 固体配制240mL0.100mol∙L-1的
固体配制240mL0.100mol∙L-1的 溶液,需要的仪器有
溶液,需要的仪器有(2)下列配制的溶液浓度偏高的是
A.称量
 时,称量时间较长 B.配制前,容量瓶中有少量蒸馏水
时,称量时间较长 B.配制前,容量瓶中有少量蒸馏水C.配制时,
 未冷却直接定容 D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
未冷却直接定容 D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面E.定容时俯视刻度线 F.加蒸馏水时不慎加过了刻度线
(3)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为

(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+
 O2(g)=H2O(g) 放出241.8 kJ能量,则b=
O2(g)=H2O(g) 放出241.8 kJ能量,则b=
(5)铅蓄电池是可充电电池,放电时电池总反应为: PbO2+Pb+4H++2SO
 =2PbSO4+2H2O 则正极的电极反应式
=2PbSO4+2H2O 则正极的电极反应式II.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(6)写出甲中正极的电极反应式:
(7)写出乙中负极的电极反应式:
您最近一年使用:0次
【推荐1】石油裂解气是一种复杂的混合气体,主要含有乙烯、丙烯、E等不饱和烃,以石油裂解气为原料可以生产很多化工产品,其中生成部分产品的流程图如图所示。已知D为有香味的液体。请回答下列问题:

(1)A的名称为__________ ,写出乙烯与水反应生成A的化学方程式:__________ 。
(2)B、D中所含官能团的名称分别为______ 、_______ 。 的反应类型为
的反应类型为______ 。
(3)____ (填“能”或“不能”)用一种试剂鉴别出A、C两种物质,若能请写出简要的步骤:________ (若不能,此空不填)。
(4)写出由丙烯生成聚丙烯的化学方程式:______ 。
(5)合成 的单体E的结构简式为
的单体E的结构简式为________ ,若E与HCl按物质的量之比为1∶1发生加成反应,写出可能生成的一种产物的结构简式:__________ 。

(1)A的名称为
(2)B、D中所含官能团的名称分别为
 的反应类型为
的反应类型为(3)
(4)写出由丙烯生成聚丙烯的化学方程式:
(5)合成
 的单体E的结构简式为
的单体E的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知A的产量通常用来衡量一个国家的石油化工水平,D的结构可用图Ⅱ模型表示。现以A为主要原料合成F和高分子化合物E,其合成路线如图Ⅰ。

(1)E的结构简式为_________________ 。
(2)反应①的化学方程式是____ 。
(3)在实验室,我们可通过反应②,利用如图Ⅲ装置来制取F。
a.反应②的化学方程式是___________________ ,反应类型是__________ 。
b.试管乙中所盛的试剂的作用是___________________________ 。
c.该装置中的一个明显的错误是____________________________ 。

(1)E的结构简式为
(2)反应①的化学方程式是
(3)在实验室,我们可通过反应②,利用如图Ⅲ装置来制取F。
a.反应②的化学方程式是
b.试管乙中所盛的试剂的作用是
c.该装置中的一个明显的错误是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】已知A的产量通常用来衡量一个国家的石油化工发展水平,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高分子化合物E,其合成路线如图所示。
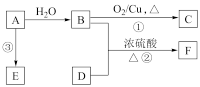
(1)A的结构式为_______ ,B中决定其性质的重要官能团的名称为_______ 。
(2)写出下列反应的化学方程式并判断反应类型。
①_______ ,反应类型:_______ 。
②_______ ,反应类型:_______ 。
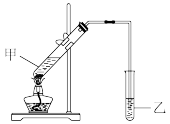
(3)在实验室里我们可以用如图所示的装置来制取F,浓硫酸作用为_______ ,乙中所盛的试剂为_______ ,该溶液的主要作用是_______ ;该装置图中有一个明显的错误是_______ 。

(1)A的结构式为
(2)写出下列反应的化学方程式并判断反应类型。
①
②
(3)在实验室里我们可以用如图所示的装置来制取F,浓硫酸作用为

您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐1】化合物E是一种药物中间体,合成路线如下图所示。
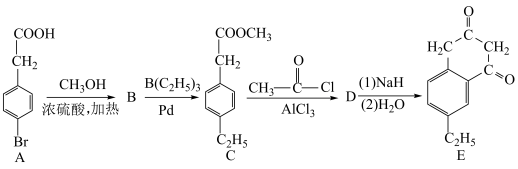
已知: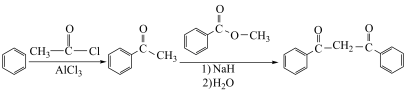
回答下列问题:
(1)A中含氧官能团的名称为___________ 。
(2)写出A→B的反应方程式___________ 。
(3)下列说法正确的是___________。
(4)D的结构简式是___________ 。
(5)已知
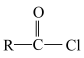 ,请设计由乙烯为原料合成
,请设计由乙烯为原料合成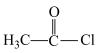 的路线(用流程图表示,无机试剂任选,流程图示例如图:
的路线(用流程图表示,无机试剂任选,流程图示例如图: )。
)。_________

已知:

回答下列问题:
(1)A中含氧官能团的名称为
(2)写出A→B的反应方程式
(3)下列说法正确的是___________。
| A.化合物C的分子式是C11H14O2 |
| B.化合物B和D均能与NaOH溶液反应 |
| C.D→E的反应类型为加成反应 |
| D.化合物E中所有原子共平面 |
(4)D的结构简式是
(5)已知

 ,请设计由乙烯为原料合成
,请设计由乙烯为原料合成 的路线(用流程图表示,无机试剂任选,流程图示例如图:
的路线(用流程图表示,无机试剂任选,流程图示例如图: )。
)。
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】碳原子不仅能与氢、氧、氮、氯等元素原子形成化学键,且碳原子之间还能相互结合,并连接形成直链、支链以及各种环状化合物。
根据下列几种烃的结构式,回答下列问题:
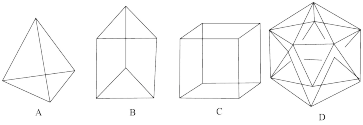
(1)结构D显然是不可能合成的,原因是__________ ;在结构A的每两个碳原子之间插入一个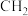 原子团,可以形成金刚烷的结构,则金刚烷的分子式是
原子团,可以形成金刚烷的结构,则金刚烷的分子式是_______________ 。
(2)B的一种同分异构是最简单的芳香烃,能证明该芳香烃中的化学键不是单键和双键交替排列的事实是_________ (填字母)。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
C的一种同分异构体E是一种重要的化工原料,在一定条件下可以发生如下反应:

已知苯环侧链上的烃基在一定条件下能被氧化成羧基。
(3)下列关于有机化合物E的说法正确的是______ (填字母)。
a.属于芳香烃 b.属于苯的同系物
c.苯环上有烷基 d.侧链中含碳碳双键
(4)有机化合物E的结构简式为____________ 。
(5)请写出E→F反应的化学方程式为__________________ ,反应类型为____________ 。
(6)H具有优良的绝热、绝缘性能,可用作包装材料和建筑材料,在工业上以E为原料生产。请写出相关化学反应方程式________________________ 。
根据下列几种烃的结构式,回答下列问题:

(1)结构D显然是不可能合成的,原因是
 原子团,可以形成金刚烷的结构,则金刚烷的分子式是
原子团,可以形成金刚烷的结构,则金刚烷的分子式是(2)B的一种同分异构是最简单的芳香烃,能证明该芳香烃中的化学键不是单键和双键交替排列的事实是
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
C的一种同分异构体E是一种重要的化工原料,在一定条件下可以发生如下反应:

已知苯环侧链上的烃基在一定条件下能被氧化成羧基。
(3)下列关于有机化合物E的说法正确的是
a.属于芳香烃 b.属于苯的同系物
c.苯环上有烷基 d.侧链中含碳碳双键
(4)有机化合物E的结构简式为
(5)请写出E→F反应的化学方程式为
(6)H具有优良的绝热、绝缘性能,可用作包装材料和建筑材料,在工业上以E为原料生产。请写出相关化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】已知 为最简单的烯烃,
为最简单的烯烃, 为环状结构。以
为环状结构。以 和
和 为原料制造隐形眼镜的功能聚合材料
为原料制造隐形眼镜的功能聚合材料 ,其合成路线如下:
,其合成路线如下:
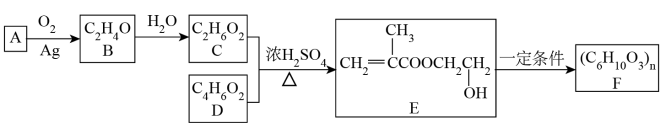
请回答:
(1)A的结构简式为_______ 。
(2) 的反应类型是
的反应类型是_______ 。
(3)请写出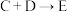 反应的化学方程式
反应的化学方程式_______ 。
(4)下列说法正确的是_______。
 为最简单的烯烃,
为最简单的烯烃, 为环状结构。以
为环状结构。以 和
和 为原料制造隐形眼镜的功能聚合材料
为原料制造隐形眼镜的功能聚合材料 ,其合成路线如下:
,其合成路线如下:
请回答:
(1)A的结构简式为
(2)
 的反应类型是
的反应类型是(3)请写出
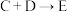 反应的化学方程式
反应的化学方程式(4)下列说法正确的是_______。
A.有机物 能使酸性高锰酸钾溶液褪色 能使酸性高锰酸钾溶液褪色 |
B.有机物 、 、 的官能团种类相同 的官能团种类相同 |
C.仅用 无法鉴别有机物 无法鉴别有机物 和 和 |
D.材料 属于高分子化合物,具有亲水性 属于高分子化合物,具有亲水性 |
您最近一年使用:0次



