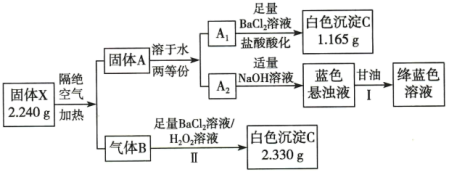
某研究性学习小组利用下列有关装置制备 ,并对
,并对 的性质进行探究(装置的气密性已检查)。已知:
的性质进行探究(装置的气密性已检查)。已知: 溶液显酸性。
溶液显酸性。

Ⅰ.探究 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是_______ 。
(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是_______ ,装置C中反应的离子方程式是_______ 。
(3)装置D中NaOH全部转化为 的标志为
的标志为_______ 。
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是_______ (用化学反应方程式表示)。
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是_______ ,其作用是_______ ,通过_______ 现象即可证明亚硫酸的酸性强于次氯酸。
 ,并对
,并对 的性质进行探究(装置的气密性已检查)。已知:
的性质进行探究(装置的气密性已检查)。已知: 溶液显酸性。
溶液显酸性。
Ⅰ.探究
 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间
 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是
(3)装置D中NaOH全部转化为
 的标志为
的标志为Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是
更新时间:2022-05-05 19:29:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.兴趣小组1组同学利用下图所示装置(夹持装置已略去)探究 的性质,并制取一种常用食品抗氧化剂焦亚硫酸钠(
的性质,并制取一种常用食品抗氧化剂焦亚硫酸钠( )。(实验前已除去装置中的空气)
)。(实验前已除去装置中的空气)
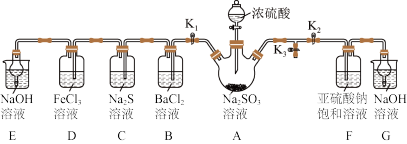
(1)A中盛放 固体的仪器的名称为
固体的仪器的名称为_______ ,其中发生反应的化学方程式为_______ 。
(2)关闭 、
、 ,打开
,打开 。
。
①装置B中的现象是_______ 。
②装置C中出现淡黄色浑浊,说明 具有
具有_______ 性。
③装置D中发生反应的离子方程式为_______ 。
④装置E和G中NaOH溶液的作用是_______ 。
(3)关闭 、
、 ,打开
,打开 。一段时间后F中有
。一段时间后F中有 晶体析出,装置F中发生反应的化学方程式
晶体析出,装置F中发生反应的化学方程式_______ 。 晶体久置空气中易被氧化,检验其在空气中已被氧化的操作和现象:取少量
晶体久置空气中易被氧化,检验其在空气中已被氧化的操作和现象:取少量 晶体于试管中,加适量水溶解,
晶体于试管中,加适量水溶解,_______ 。
II.兴趣小组2组同学用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
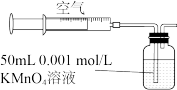
(4)当注入标准状况下200mL空气时,酸性 溶液恰好褪色,停止实验。该空气中
溶液恰好褪色,停止实验。该空气中 的体积分数为
的体积分数为_______ 。
 的性质,并制取一种常用食品抗氧化剂焦亚硫酸钠(
的性质,并制取一种常用食品抗氧化剂焦亚硫酸钠( )。(实验前已除去装置中的空气)
)。(实验前已除去装置中的空气)
(1)A中盛放
 固体的仪器的名称为
固体的仪器的名称为(2)关闭
 、
、 ,打开
,打开 。
。①装置B中的现象是
②装置C中出现淡黄色浑浊,说明
 具有
具有③装置D中发生反应的离子方程式为
④装置E和G中NaOH溶液的作用是
(3)关闭
 、
、 ,打开
,打开 。一段时间后F中有
。一段时间后F中有 晶体析出,装置F中发生反应的化学方程式
晶体析出,装置F中发生反应的化学方程式 晶体久置空气中易被氧化,检验其在空气中已被氧化的操作和现象:取少量
晶体久置空气中易被氧化,检验其在空气中已被氧化的操作和现象:取少量 晶体于试管中,加适量水溶解,
晶体于试管中,加适量水溶解,II.兴趣小组2组同学用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
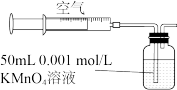
(4)当注入标准状况下200mL空气时,酸性
 溶液恰好褪色,停止实验。该空气中
溶液恰好褪色,停止实验。该空气中 的体积分数为
的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为验证 和NaOH能发生化学反应,某实验小组的同学设计了如图所示的实验装置。
和NaOH能发生化学反应,某实验小组的同学设计了如图所示的实验装置。
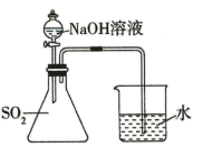
(1)预测实验现象:___________ ;产生该实验现象的原因可能是___________ 。
(2)某同学质疑由上述实验设计得出的结论,该同学质疑的依据是___________ 。
(3)在原实验的基础上,请你设计实验,证明在上述实验装置的锥形瓶中, 和NaOH肯定发生了化学反应:
和NaOH肯定发生了化学反应:___________ 。
(4)写出 与过量NaOH溶液反应的离子方程式:
与过量NaOH溶液反应的离子方程式:___________ 。
 和NaOH能发生化学反应,某实验小组的同学设计了如图所示的实验装置。
和NaOH能发生化学反应,某实验小组的同学设计了如图所示的实验装置。
(1)预测实验现象:
(2)某同学质疑由上述实验设计得出的结论,该同学质疑的依据是
(3)在原实验的基础上,请你设计实验,证明在上述实验装置的锥形瓶中,
 和NaOH肯定发生了化学反应:
和NaOH肯定发生了化学反应:(4)写出
 与过量NaOH溶液反应的离子方程式:
与过量NaOH溶液反应的离子方程式:
您最近一年使用:0次
【推荐3】回答下列问题:
(1)用下图装置制备纯净的SO2发生装置中反应的化学方程式为___________ ,装置的连接顺序为:a→___________ (按气流方向,用小写字母表示)。
+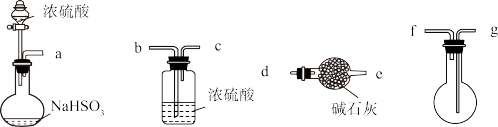
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉 - KI 溶液、新制H2S溶液。
(3)工业上利用硫酸厂烧渣(主要成分为Fe2O3,还含有少量FeS、SiO2等)制备绿矾的流程如下(其中所加试剂均过量):
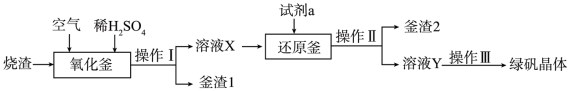
已知“釜渣 I ”中存在淡黄色固体颗粒,则“釜渣 1”主要成分为___________ ,生成该淡黄色固体反应的离子方程式为___________ 。“试剂 a”是一种单质,其名称为___________ ,其作用是 ___________ 。
(1)用下图装置制备纯净的SO2发生装置中反应的化学方程式为
+
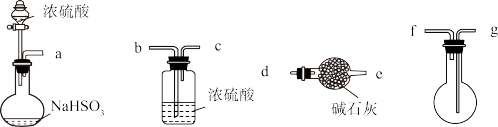
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉 - KI 溶液、新制H2S溶液。

| 操作步骤 | 实验现象 | 解释原因 |
| 用注射器将新制H2S溶液注入充满SO2的烧瓶中 | 产生淡黄色浑浊 | +4价S具有 |
| 用注射器将 | +4价S具有还原性,反应的离子方程式为 |

已知“釜渣 I ”中存在淡黄色固体颗粒,则“釜渣 1”主要成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究性学习小组学生用图中所示装置(部分夹持装置略)探究NO与Na2O2反应的情况,提出假设并进行相关实验。
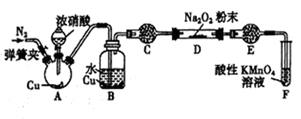
该研究性学习小组同学认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO4-反应生成NO3-和Mn2+。
(1)在反应前,打开弹簧夹,通入一段时间N2,目的是__________________________ 。
(2)A 中反应的氧化剂与还原剂的物质的量之比为______________ 。
(3)B 中观察到的主要现象是____________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生
(4)C、E 中所盛装的试剂不能是________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
(5)F 中反应的离子方程式是_________________________________________ 。
(6)充分反应后,检验D装置中产物的方法是:_____________________________ ,则产物是NaNO2。

该研究性学习小组同学认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO4-反应生成NO3-和Mn2+。
(1)在反应前,打开弹簧夹,通入一段时间N2,目的是
(2)A 中反应的氧化剂与还原剂的物质的量之比为
(3)B 中观察到的主要现象是
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生
(4)C、E 中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
(5)F 中反应的离子方程式是
(6)充分反应后,检验D装置中产物的方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
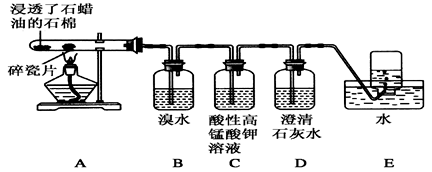
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34 C8H18+甲,甲
C8H18+甲,甲 4乙,则甲的分子式为
4乙,则甲的分子式为________ ,乙的结构简式为____________________________________ 。
(2)B装置中的实验现象可能是________ ,写出反应的化学方程式:__________ ,其反应类型是________ 。
(3)C装置中可观察到的现象是____________ ,反应类型是________ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_____ (填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________ 。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________ (选填字母,下同);除去甲烷中乙烯的方法是________ 。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是_________________ 。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34
 C8H18+甲,甲
C8H18+甲,甲 4乙,则甲的分子式为
4乙,则甲的分子式为(2)B装置中的实验现象可能是
(3)C装置中可观察到的现象是
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过上述实验探究,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是
您最近一年使用:0次