硫及其化合物在生产中应用广泛。
(1)古文献《新修本草》关于绿矾 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
①实验室检验绿矾变质的试剂是___________ (填化学式,下同)溶液。
②“青矾厂气”中一定含有___________ ,赤色固体可能是___________ 。
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。
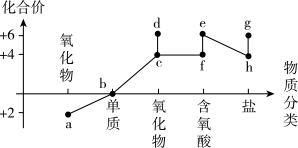
①下列物质能与d反应,但不属于氧化还原反应的是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
②f的钠盐长期放置容易变质,原因为___________ (用化学方程式表示)。
③为确认工业废气中含有c和d,将其通入依次以下装置。
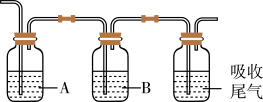
A、B中供选择的试剂有:a.品红 b. c.
c. d.
d. e.浓硫酸
e.浓硫酸
B中溶液为___________ (填标号),可观察到A中的现象为___________ 。
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即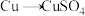 。
。
方案乙: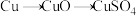 。
。
①方案甲中,铜和浓硫酸发生反应的化学方程式是___________ 。该反应体现了浓硫酸的___________ 。
②这两种方案,你认为哪一种方案更合理?___________ 。理由是___________ 。
(1)古文献《新修本草》关于绿矾
 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。①实验室检验绿矾变质的试剂是
②“青矾厂气”中一定含有
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。

①下列物质能与d反应,但不属于氧化还原反应的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液②f的钠盐长期放置容易变质,原因为
③为确认工业废气中含有c和d,将其通入依次以下装置。

A、B中供选择的试剂有:a.品红 b.
 c.
c. d.
d. e.浓硫酸
e.浓硫酸B中溶液为
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
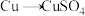 。
。方案乙:
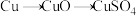 。
。①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
更新时间:2022/05/06 16:01:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】焦亚硫酸钠(Na2S2O5)广泛用于化工、医药工业、食品工业等,为白色结晶粉末,水溶液呈酸性,易被氧化。回答下列问题:
(1)实验室制备少量Na2S2O5的实验装置如图:
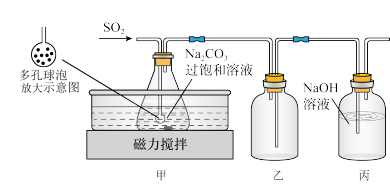
①装置甲中的反应先生成NaHSO3,NaHSO3再发生分解生成Na2S2O5。生成NaHSO3的离子方程式为__ ;通SO2气体的导管末端是带许多小孔的玻璃球泡,其主要作用是__ ;水浴加热温度为40℃左右,若反应温度过高可能会生成Na2SO3和Na2SO4等杂质。检验溶液中是否含 离子的方法是
离子的方法是___ 。
②装置乙的作用是__ 。
(2)Na2S2O5是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。
①为检验某白葡萄酒中是否含有Na2S2O5能否用酸性KMnO4溶液检验?作出判断并说明理由___ 。
②向一定质量的高筋面粉中分别添加不同比例的焦亚硫酸钠,加入适量NaCl、水、和面、熟化、揉搓、拉伸至面筋柔顺,用模具压制成2mm×60mm的面团条,用专用仪器进行拉伸试验及检测,焦亚硫酸钠的添加比例对二硫。键(—S—S—)含量、游离巯基(—SH)含量和拉伸距离的影响如图所示。
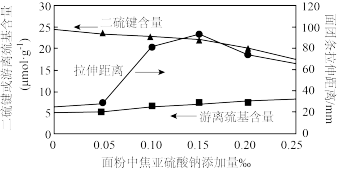
已知:二硫键是维持面筋蛋白弹性的重要结构,其含量过高或过低都会影响面团的延伸性。分析图象可知,拉面中添加焦亚硫酸钠,其在反应中表现出的性质是___ ;当添加量___ (填标号)时,面团延伸性较好。
A.0~0.05‰ B.0.05‰~0.10‰ C.0.1‰~0.15‰ D.0.20‰~0.25‰
(3)根据我国相关规定,焦亚硫酸钠在拉面中的最大使用量为0.05g·kg-1(以二氧化硫残留量计)。若每1kg面粉中添加0.1gNa2S2O3(添加量为0.1‰),可制得约1.5kg拉面,则理论上拉面中二氧化硫最大残留量约为__ g·kg-1(不考虑二氧化硫的反应和挥发)。
(1)实验室制备少量Na2S2O5的实验装置如图:

①装置甲中的反应先生成NaHSO3,NaHSO3再发生分解生成Na2S2O5。生成NaHSO3的离子方程式为
 离子的方法是
离子的方法是②装置乙的作用是
(2)Na2S2O5是常用的食品添加剂,常用于葡萄酒、果脯、拉面等食品中。
①为检验某白葡萄酒中是否含有Na2S2O5能否用酸性KMnO4溶液检验?作出判断并说明理由
②向一定质量的高筋面粉中分别添加不同比例的焦亚硫酸钠,加入适量NaCl、水、和面、熟化、揉搓、拉伸至面筋柔顺,用模具压制成2mm×60mm的面团条,用专用仪器进行拉伸试验及检测,焦亚硫酸钠的添加比例对二硫。键(—S—S—)含量、游离巯基(—SH)含量和拉伸距离的影响如图所示。

已知:二硫键是维持面筋蛋白弹性的重要结构,其含量过高或过低都会影响面团的延伸性。分析图象可知,拉面中添加焦亚硫酸钠,其在反应中表现出的性质是
A.0~0.05‰ B.0.05‰~0.10‰ C.0.1‰~0.15‰ D.0.20‰~0.25‰
(3)根据我国相关规定,焦亚硫酸钠在拉面中的最大使用量为0.05g·kg-1(以二氧化硫残留量计)。若每1kg面粉中添加0.1gNa2S2O3(添加量为0.1‰),可制得约1.5kg拉面,则理论上拉面中二氧化硫最大残留量约为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)习近平在纳扎尔巴耶夫大学回答学生问题时指出:“我们既要绿水青山,也要金山银山。宁要绿水青山,不要金山银山,而且绿水青山就是金山银山。”改善空气质量、保护水土资源是实现美丽中国的基础。
①下列气体的排放会导致酸雨形成的是_______ (填字母,下同)。
a.CH4 b.CO c.SO2d.NO
②下列处理废水的方法属于中和法的是_______
a.用熟石灰处理废水中的酸. b.用臭氧处理废水中的氰化物
c.用铁粉回收废水中的铜 d.用FeSO4处理废水中的Cr2O
③下列做法会造成土壤重金属污染的是_______
a.作物秸秆露天焚烧 b.废干电池就地填埋.
c.废旧塑料随意丢弃 d.推广使用无铅汽油
(2)材料的发展与应用促进了人类社会的进步
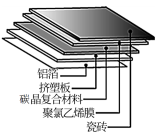
①碳晶地暖环保、节能、安全,其构造如图所示。其中属于高分子材料的是挤塑板和__________ ;属于金属材料的是______ ;属于硅酸盐材料的是______ ;
②吸附材料具有多孔、表面积大的特点。活性炭吸附NO2的过程中,会伴有C与NO2的反应.产物为两种常见无毒气体。写出该反应的化学方程式:______ ;
③LiMn2O4是锂离子电池的一种正极材料,可通过MnO2与Li2CO3煅烧制备,同时还生成CO2和一种单质。写出该反应的化学方程式:______ 。
①下列气体的排放会导致酸雨形成的是
a.CH4 b.CO c.SO2d.NO
②下列处理废水的方法属于中和法的是
a.用熟石灰处理废水中的酸. b.用臭氧处理废水中的氰化物
c.用铁粉回收废水中的铜 d.用FeSO4处理废水中的Cr2O

③下列做法会造成土壤重金属污染的是
a.作物秸秆露天焚烧 b.废干电池就地填埋.
c.废旧塑料随意丢弃 d.推广使用无铅汽油
(2)材料的发展与应用促进了人类社会的进步

①碳晶地暖环保、节能、安全,其构造如图所示。其中属于高分子材料的是挤塑板和
②吸附材料具有多孔、表面积大的特点。活性炭吸附NO2的过程中,会伴有C与NO2的反应.产物为两种常见无毒气体。写出该反应的化学方程式:
③LiMn2O4是锂离子电池的一种正极材料,可通过MnO2与Li2CO3煅烧制备,同时还生成CO2和一种单质。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】《化学与生活》,根据要求完成下列填空
(1)近年来,全国多个省市出现雾霾天气,进入冬季后,雾霾尤为严重。防治污染,改善生态环境已成为全民共识。
①空气污染指数API表明了空气的质量。空气污染指数主要是根据空气中______ 、NO2和可吸入颗粒物等污染物的浓度计算出来的数值。
②下列行为可能会导致雾霾现象加重的是_______ (选填字母)。
a.燃煤脱硫 b.静电除尘 c.燃放鞭炮
③氨气与氮氧化物(NOx)在一定条件下反应可生成对空气无污染的物质,则该反应的化学方程式为______________ 。
(2)合理选择饮食,正确使用药物,可以促进身心健康。
①糖类是生命活动的基础能源,油脂、蛋白质也能为人体提供能量。等质量的上述物质中,提供能量最多的是________ (选填字母)。
a.糖类 b.油脂 c.蛋白质
②人体牙龈出血、患坏血病主要是缺乏__________ (选填字母)。
a.维生素A b.维生素B c.维生素C
③合理食用加碘盐是防止缺碘性疾病的有效方法之一。在人体必需元素中,碘属于
________ (选填“常量”或“微量”)元素。
④复方氢氧化铝可治疗胃酸过多,氢氧化铝与胃酸(HCl)反应的离子方程式为:_____ 。
(3)材料的不断发展可以促进社会进步。
①碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
化学式中a、b、c、d的代数关系式为____________________ 。
②聚乙烯塑料可用于食品的包装袋,其结构简式为____________ 。
③橡胶是制造轮胎的重要原料,天然橡胶通过______ 处理,使其转化为体型结构,从而增大橡胶的强度。
④体育场馆的建设需要大量的钢筋、水泥、玻璃等建筑材料。

生产水泥、玻璃共同的原料是_______ (填名称)。钢筋主要是Fe和______ (填化学符号)的合金。钢梁结构露置在潮湿的空气中易发生电化学腐蚀,写出发生电化学腐蚀时负极的电极反应式____________ 。
(1)近年来,全国多个省市出现雾霾天气,进入冬季后,雾霾尤为严重。防治污染,改善生态环境已成为全民共识。
①空气污染指数API表明了空气的质量。空气污染指数主要是根据空气中
②下列行为可能会导致雾霾现象加重的是
a.燃煤脱硫 b.静电除尘 c.燃放鞭炮
③氨气与氮氧化物(NOx)在一定条件下反应可生成对空气无污染的物质,则该反应的化学方程式为
(2)合理选择饮食,正确使用药物,可以促进身心健康。
①糖类是生命活动的基础能源,油脂、蛋白质也能为人体提供能量。等质量的上述物质中,提供能量最多的是
a.糖类 b.油脂 c.蛋白质
②人体牙龈出血、患坏血病主要是缺乏
a.维生素A b.维生素B c.维生素C
③合理食用加碘盐是防止缺碘性疾病的有效方法之一。在人体必需元素中,碘属于
④复方氢氧化铝可治疗胃酸过多,氢氧化铝与胃酸(HCl)反应的离子方程式为:
(3)材料的不断发展可以促进社会进步。
①碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
化学式中a、b、c、d的代数关系式为
②聚乙烯塑料可用于食品的包装袋,其结构简式为
③橡胶是制造轮胎的重要原料,天然橡胶通过
④体育场馆的建设需要大量的钢筋、水泥、玻璃等建筑材料。

生产水泥、玻璃共同的原料是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:
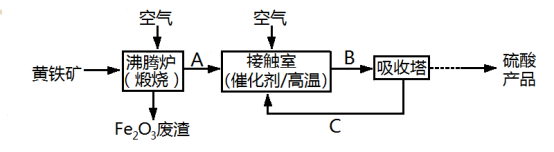
回答下列问题:
(1)在接触室中发生的反应是2SO2+O2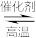 2SO3,该反应属于
2SO3,该反应属于_______ (填字母)
a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式_______ 。
(3)写出沸腾炉中发生反应的化学方程式:_______
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是_______ 。
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:_______ 。

回答下列问题:
(1)在接触室中发生的反应是2SO2+O2
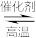 2SO3,该反应属于
2SO3,该反应属于a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)写出Cu和浓硫酸反应的化学方程式
(3)写出沸腾炉中发生反应的化学方程式:
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是
(5)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的还原性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)写出正丁烷的结构简式:_______ ;
(2)胆矾晶体遇浓硫酸变白,体现了浓硫酸的_______ 性;
(3)写出铁和氯化铁溶液反应的离子方程式_______ ;
(4)根据所学的知识,试解释 比
比 热稳定性强的原因
热稳定性强的原因_______ 。
(1)写出正丁烷的结构简式:
(2)胆矾晶体遇浓硫酸变白,体现了浓硫酸的
(3)写出铁和氯化铁溶液反应的离子方程式
(4)根据所学的知识,试解释
 比
比 热稳定性强的原因
热稳定性强的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列八种物质:①铜 ②SO2的水溶液 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥红褐色的氢氧化铁胶体 ⑦HCl ⑧新制氯水
(1)上述物质中属于电解质的有___________ 。(填序号)
(2)向⑧中滴加紫色石蕊溶液,看到的现象是___________ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为___________ 。
(4)写出①与浓硫酸反应的化学方程式___________ 。
(5)配平⑦的浓溶液与高锰酸钾发生反应的化学方程式为:______ ____KMnO4+_______HCl(浓)=____ __ MnCl2+_______KCl+_____Cl2↑+____H2O,该反应中的氧化剂与还原剂的物质的量之比___________
(6)②与⑧都能使品红溶液褪色,而将二种气体等物质的量混合后通入品红溶液,品红不褪色,试离子方程式解释其原因___________ 。
(1)上述物质中属于电解质的有
(2)向⑧中滴加紫色石蕊溶液,看到的现象是
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(4)写出①与浓硫酸反应的化学方程式
(5)配平⑦的浓溶液与高锰酸钾发生反应的化学方程式为:
(6)②与⑧都能使品红溶液褪色,而将二种气体等物质的量混合后通入品红溶液,品红不褪色,试离子方程式解释其原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______ 。
(2)向Ba(OH)2溶液中加入稀硫酸,现象:_______ ,离子方程式:_______ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关反应的离子方程式为_______ 。
③通过以上叙述可知溶液中肯定不存在的离子是_______ ,可能存在的离子是_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向Ba(OH)2溶液中加入稀硫酸,现象:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是_________ ,理由是_________ 。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子是________ ,有关的离子方程式为_____________ 。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是_________ ,有关反应的离子方程式为__________________ 。
(4)原溶液中可能大量存在的阴离子是下列A~D中的(填序号)_________。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子是
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)原溶液中可能大量存在的阴离子是下列A~D中的(填序号)_________。
| A.Cl- | B. | C. | D.OH- |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、NH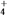 、Cl-、CO
、Cl-、CO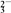 和SO
和SO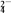 。现每次取10.00 mL进行实验:
。现每次取10.00 mL进行实验:
②第二份加入足量NaOH后加热,收集到气体0.672 L (标准状况下);
③第三份加足量BaCl2溶液后得干燥沉淀6.63 g,沉淀经足量盐酸洗涤,干燥后剩4.66 g。
请回答:
(1) c(CO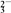 )=
)=
(3) 根据以上实验:
①不能判断哪些离子是否存在
②若存在这些离子,如何进行检验?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】胶体是一种重要的分散系。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈________ 色,即可制得Fe(OH)3胶体。
(2)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到_______ 烧杯(填甲”或“乙”)中的液体产生丁达尔效应。
(3)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中逐渐滴加稀盐酸至过量,在此过程中可以观察到的现象是______________________________________________________________ 。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈
(2)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(3)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中逐渐滴加稀盐酸至过量,在此过程中可以观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的离子方程式为__________ ,反应后得到的FeCl3溶液呈_______ 色。
用此溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,可以观察到有红褐色沉淀生成,反应的离子方程式为_________ ,此反应属于__________ 反应。
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈___ 色,即可制得Fe(OH)3胶体。化学方程式为____________
(4)取另一小烧杯也加入20mL蒸馏水后,向烧杯中加入1mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置在暗处:分别用激光笔照射杯中的液体,可以看到____ 烧杯中的液体会产生丁达尔效应。
(5)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,此过程发生的化学方程式为________
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的离子方程式为
用此溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,可以观察到有红褐色沉淀生成,反应的离子方程式为
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈
(4)取另一小烧杯也加入20mL蒸馏水后,向烧杯中加入1mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置在暗处:分别用激光笔照射杯中的液体,可以看到
(5)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,此过程发生的化学方程式为
您最近一年使用:0次




