下表是元素周期表的一部分,根据表中给出10种元素,按要求作答。
(1)光导纤维的主要成分是_______ (填化学式)。
(2)形成化合物种类最多的元素_______ (填元素符号)。
(3)③、⑧、⑨的氢化物稳定性最强的是_______ (填化学式)。
(4)元素④、⑥的最高价氧化物对应的水化物之间可以相互反应,写出该反应的离子方程式___ 。
(5)元素②和⑤形成的化合物中含有_______ (填“离子键”或“共价键”)
(6)画出⑩的原子结构示意图_______ 。
(7)高温下,⑥单质与氧化铁反应的化学方程式为_______ ,该反应可用于_______ (填用途)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)形成化合物种类最多的元素
(3)③、⑧、⑨的氢化物稳定性最强的是
(4)元素④、⑥的最高价氧化物对应的水化物之间可以相互反应,写出该反应的离子方程式
(5)元素②和⑤形成的化合物中含有
(6)画出⑩的原子结构示意图
(7)高温下,⑥单质与氧化铁反应的化学方程式为
更新时间:2022-05-20 18:44:02
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语 回答下列问题:
(1)⑧元素氢化物的电子式是_____________ 。
(2)②、③、⑤元素的原子半径由大到小的顺序为____________________ 。
(3)②、④、⑦元素的气态氢化物稳定性由强到弱的顺序是_________________________ 。
(4)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生离子反应,则该反应的离子方程式为_____________________________________________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)⑧元素氢化物的电子式是
(2)②、③、⑤元素的原子半径由大到小的顺序为
(3)②、④、⑦元素的气态氢化物稳定性由强到弱的顺序是
(4)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生离子反应,则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表列出了①~⑨九种元素在周期表中的位置。
回答下列问题:
(1)①~⑨九种元素中,化学性质最不活泼的是___________ (填元素符号)。
(2)元素⑦在周期表中的位置是___________ 。
(3)元素②和③中原子半径较大的是___________ (填元素符号)。
(4)元素③和④中气态氢化物稳定性较强的是___________ (填化学式)。
(5)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是___________ (填化学式),X和Y反应的离子方程式为___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)①~⑨九种元素中,化学性质最不活泼的是
(2)元素⑦在周期表中的位置是
(3)元素②和③中原子半径较大的是
(4)元素③和④中气态氢化物稳定性较强的是
(5)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】2021年10月16日,神舟十三号载人飞船与“天和”核心舱成功径向交会对接。化学助力我国航天事业发展,借助元素周期表可以认识各种材料的组成、结构和性质。a~h8种元素在元素周期表中的位置如下:
(1)液态a单质和液态d单质可用作火箭推进剂,二者反应的化学方程式为___________ 。常温下,与a单质更容易反应的是___________ (填“c”或“d”或“e”)单质。
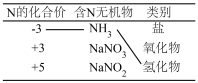
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。_________
(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为___________ ;h最高价氧化物对应的水化物的稀溶液,与f的最高价氧化物反应的离子方程式为___________ 。
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为___________ ;b和g组成的化合物可作为新型陶瓷材料,其化学式为___________ 。上述g的两种化合物含有的化学键类型均为___________ 。
| 周期 | ⅠA | 0 | |||||||
| 1 | a | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | e | |||||
| 3 | f | g | h | ||||||
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。

(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,⑦的元素符号____ ,原子半径最大的是____ ,S2-结构示意图为____ 。
(2)元素的最高价氧化物对应的水化物中酸性最强的___ ,碱性最强的是____ ,呈两性的氢氧化物是____ 。
(3)按要求写出下列两种物质的电子式:①的氢化物_____ ;③的最高价氧化物对应的水化物____ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的
(3)按要求写出下列两种物质的电子式:①的氢化物
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D、E、F六种短周期主族元素,其原子半径和主要化合价信息如表所示:
请回答下列问题:
(1)D元素在元素周期表中的位置是_______ ,化合物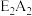 含有的化学键类型是
含有的化学键类型是_______ 。
(2)上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (用化学式表示)。
(3)A和D的简单氢化物中沸点高的是_______ (填化学式),原因是_______ 。
(4)化合物FC溶于强碱生成氨气,写出FC与NaOH溶液反应的化学方程式_______ 。
(5)由A和E两种元素组成的一种化合物加入到硫酸亚铁溶液中,立即产生红褐色沉淀,但无气体产生,试写出该反应的离子方程式_______ 。
| A | B | C | D | E | F | |
| 原子半径/(nm) | 0.074 | 0.099 | 0.075 | 0.102 | 0.186 | 0.143 |
| 最高或最低化合价 | +7 | +5 | +6 | +1 | +3 | |
| -2 | -1 | -3 | -2 |
(1)D元素在元素周期表中的位置是
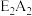 含有的化学键类型是
含有的化学键类型是(2)上述元素的最高价氧化物对应的水化物中,酸性最强的是
(3)A和D的简单氢化物中沸点高的是
(4)化合物FC溶于强碱生成氨气,写出FC与NaOH溶液反应的化学方程式
(5)由A和E两种元素组成的一种化合物加入到硫酸亚铁溶液中,立即产生红褐色沉淀,但无气体产生,试写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】Ⅰ.已知有下列物质:①HNO3;②硫单质;③NaOH;④液氦;⑤Na2O2;⑥H2O2;⑦CCl4;⑧NH4Cl;⑨KBr;⑩O2,分别将正确的序号填入相应的位置。
(1)以上物质中只含有离子键的是___________ ;
(2)只含有共价键的是___________ ;
(3)既含有离子键又含有极性共价键的是___________ ;其电子式分别为___________ 、___________ ;
(4)含有非极性共价键的化合物是___________ ;
(5)不含化学键的是___________ 。
Ⅱ.下表为元素周期表的一部分。
请回答下列问题:
(6)⑦⑧⑨三种元素最高价氧化物对应的水化物中酸性最强的是___________ (填化学式)。
(7)③⑥⑨三种元素的简单离子半径由大到小排序为___________ (填离子符号);
(8)元素④和⑥最高价氧化物对应的水化物反应的离子方程式为___________ ;
(9)从原子结构的角度分析④与⑤的金属性强弱:___________ 。
(10)②、⑦的气态氢化物中较稳定的是___________ (填化学式),判断依据是___________
(1)以上物质中只含有离子键的是
(2)只含有共价键的是
(3)既含有离子键又含有极性共价键的是
(4)含有非极性共价键的化合物是
(5)不含化学键的是
Ⅱ.下表为元素周期表的一部分。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥIA | ⅦA | 0 | |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(6)⑦⑧⑨三种元素最高价氧化物对应的水化物中酸性最强的是
(7)③⑥⑨三种元素的简单离子半径由大到小排序为
(8)元素④和⑥最高价氧化物对应的水化物反应的离子方程式为
(9)从原子结构的角度分析④与⑤的金属性强弱:
(10)②、⑦的气态氢化物中较稳定的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素①~⑩在周期表中的位置如表所示:
回答下列问题:
(1)最外层电子数为2的元素有_______ (填元素符号);⑨的简单离子结构示意图为_______ 。
(2)①与④两种元素形成相对分子质量为42的链状化合物的结构简式为_______ ;①、⑤、⑥三种元素形成的一种常见盐的化学式为_______ ,该盐中含有的化学键有_______ 。
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈_______ 色。⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为_______ 。
(4)用电子式表示⑧与⑩形成的化合物的形成过程_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)最外层电子数为2的元素有
(2)①与④两种元素形成相对分子质量为42的链状化合物的结构简式为
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈
(4)用电子式表示⑧与⑩形成的化合物的形成过程
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(2)A、B、F三种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是_______ 。
(4)元素A与C形成的电子总数为22的分子的结构式为_______ 。
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为_______ ,其所含的化学键有_______ (填化学键类型)。
(6)C的简单氢化物在通常状况下,加热到100℃时由液态变为气态,加热到2000℃时发生分解反应,请从物质的构成微粒及相互作用的角度解释这两种变化过程中所需温度差异的原因_______ 。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)A、B、F三种元素的原子半径由大到小的顺序是
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为
(6)C的简单氢化物在通常状况下,加热到100℃时由液态变为气态,加热到2000℃时发生分解反应,请从物质的构成微粒及相互作用的角度解释这两种变化过程中所需温度差异的原因
您最近一年使用:0次



