实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如图实验。请完成下列填空:
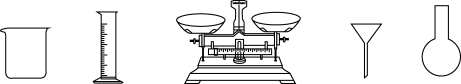
(1)由NaOH固体配制0.10mol/LNaOH标准溶液,需要的仪器有药匙、玻璃棒、容量瓶、____ (从图中选择,写出名称)。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如表:
滴定达到终点的标志是____ 。根据上述数据,可计算出该盐酸的浓度约为____ (保留两位有效数字)。
(3)用NaOH标准溶液滴定未知浓度的盐酸时,下列各操作中无误差的是____ (填序号)。
(1)由NaOH固体配制0.10mol/LNaOH标准溶液,需要的仪器有药匙、玻璃棒、容量瓶、

(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如表:
| 实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 22.04 | 20.00 |
| 3 | 0.10 | 22.00 | 20.00 |
(3)用NaOH标准溶液滴定未知浓度的盐酸时,下列各操作中无误差的是
| A.用蒸馏水洗净碱式滴定管后,注入NaOH标准溶液进行滴定 |
| B.用蒸馏水洗涤锥形瓶后,再用待测盐酸润洗,而后装入一定体积的盐酸溶液进行滴定 |
| C.用酸式滴定管量取10.00mL稀盐酸放入用蒸馏水洗涤后的锥形瓶中,再加入适量蒸馏水和几滴酚酞后进行滴定 |
| D.滴定完毕读数后发现滴定管尖嘴还残余1滴液体 |
更新时间:2022-05-20 16:25:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】孔雀石主要含Cu2(OH)2CO3,以及少量Fe、Si的化合物,可以用孔雀石为原料制备胆矾( CuSO4·5H2O),步骤如下:

回答下列问题:
(1)试剂①是一种常见的酸,其化学式为______ 。过滤所需要的玻璃仪器有烧杯、__________ 。
(2)实验室检验 Fe3+的常用方法是_____________________________________ 。
(3)若溶液A中的金属离子有Cu2+、Fe2+ 、Fe3+,上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+,从而形成溶液 B,则试剂②能否使用氯水?(填“能”或“不能”,若填“不能”,请解释原因)。_________________
(4)由溶液C获得胆矾,需要经过_______ 、_____ 、过滤等操作。
(5)取25.00mL溶液A,用1.000×10-2mol/L的 KMnO4标准溶液滴定。反应离子方程式为:5Fe2++ MnO4-+8H+=5Fe3+ Mn2+ +4H2O,若消耗标准溶液 20.00mL,则溶液A 中Fe2+的浓度为_________ mol/L。

回答下列问题:
(1)试剂①是一种常见的酸,其化学式为
(2)实验室检验 Fe3+的常用方法是
(3)若溶液A中的金属离子有Cu2+、Fe2+ 、Fe3+,上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+,从而形成溶液 B,则试剂②能否使用氯水?(填“能”或“不能”,若填“不能”,请解释原因)。
(4)由溶液C获得胆矾,需要经过
(5)取25.00mL溶液A,用1.000×10-2mol/L的 KMnO4标准溶液滴定。反应离子方程式为:5Fe2++ MnO4-+8H+=5Fe3+ Mn2+ +4H2O,若消耗标准溶液 20.00mL,则溶液A 中Fe2+的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下:
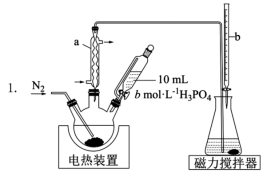
①三颈烧瓶中加入 香菇样品和
香菇样品和 水;锥形瓶中加入
水;锥形瓶中加入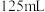 水、
水、 淀粉溶液,并预加
淀粉溶液,并预加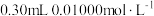 的碘标准溶液,搅拌。
的碘标准溶液,搅拌。
②以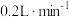 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了
流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了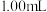 碘标准溶液。
碘标准溶液。
做空白实验,消耗了 碘标准溶液。
碘标准溶液。
用适量 替代香菇样品,重复上述步骤,测得
替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
的平均回收率为95%。
已知: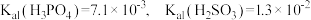
回答下列问题:
(1)装置图中仪器a、b的名称分别为___________ 、___________ 。
(2)三颈烧瓶适宜的规格为___________ (填标号)。
A. B.
B. C.
C.
(3)滴定管在使用前需要___________ 、洗涤、润洗:滴定终点时溶液的颜色为___________ ;滴定反应的离子方程式为___________ 。
(4)若先加磷酸再通氮气,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
(5)该样品中亚硫酸盐含量为___________ 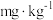 (以
(以 计,结果保留三位有效数字)。
计,结果保留三位有效数字)。

①三颈烧瓶中加入
 香菇样品和
香菇样品和 水;锥形瓶中加入
水;锥形瓶中加入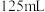 水、
水、 淀粉溶液,并预加
淀粉溶液,并预加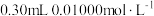 的碘标准溶液,搅拌。
的碘标准溶液,搅拌。②以
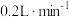 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了
流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了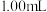 碘标准溶液。
碘标准溶液。做空白实验,消耗了
 碘标准溶液。
碘标准溶液。用适量
 替代香菇样品,重复上述步骤,测得
替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
的平均回收率为95%。已知:
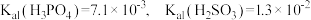
回答下列问题:
(1)装置图中仪器a、b的名称分别为
(2)三颈烧瓶适宜的规格为
A.
 B.
B. C.
C.
(3)滴定管在使用前需要
(4)若先加磷酸再通氮气,会使测定结果
(5)该样品中亚硫酸盐含量为
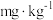 (以
(以 计,结果保留三位有效数字)。
计,结果保留三位有效数字)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度,将水样与 碱性悬浊液(含有
碱性悬浊液(含有 )混合,反应生成
)混合,反应生成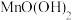 ,实现氧的固定。
,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,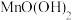 被
被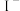 还原为
还原为 ,在暗处静置
,在暗处静置 ,然后用标准
,然后用标准 溶液滴定,生成的
溶液滴定,生成的 反应为:
反应为: 。
。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_______ 。
(2)“氧的固定”中发生反应的化学方程式为_______ 。
(3)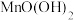 被
被 还原为
还原为 的离子反应方程式
的离子反应方程式_______ 。
(4)取 水样经固氧、酸化后,用
水样经固氧、酸化后,用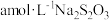 溶液滴定,以淀粉溶液作指示剂,终点现象为
溶液滴定,以淀粉溶液作指示剂,终点现象为_______ .若消耗 溶液的体积为
溶液的体积为 ,则水样中溶解氧的含量为
,则水样中溶解氧的含量为_______  。
。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏_______ (填“高”或“低”)。
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度,将水样与
 碱性悬浊液(含有
碱性悬浊液(含有 )混合,反应生成
)混合,反应生成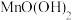 ,实现氧的固定。
,实现氧的固定。Ⅱ.酸化、滴定
将固氧后的水样酸化,
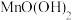 被
被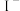 还原为
还原为 ,在暗处静置
,在暗处静置 ,然后用标准
,然后用标准 溶液滴定,生成的
溶液滴定,生成的 反应为:
反应为: 。
。回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是
(2)“氧的固定”中发生反应的化学方程式为
(3)
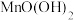 被
被 还原为
还原为 的离子反应方程式
的离子反应方程式(4)取
 水样经固氧、酸化后,用
水样经固氧、酸化后,用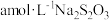 溶液滴定,以淀粉溶液作指示剂,终点现象为
溶液滴定,以淀粉溶液作指示剂,终点现象为 溶液的体积为
溶液的体积为 ,则水样中溶解氧的含量为
,则水样中溶解氧的含量为 。
。(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室用硫酸铜晶体(CuSO4•5H2O)配制1.00mol•L-1的CuSO4溶液100mL,回答下列问题:
(1)本实验需硫酸铜晶体的质量为____ g(保留3位有效数字)
(2)应选用_____ mL的容量瓶。
(3)某同学将称量好的硫酸铜晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯内壁和玻璃棒2~3次,洗涤液也转移至容量瓶中,然后加蒸馏水至液面距离容量瓶的刻度线1~2cm时,用胶头滴管加蒸馏水至刻度线,最后将溶液转移到试剂瓶中。指出上述操作中的3个错误。
①___ ;
②___ ;
③___ 。
(4)配制上述溶液时,造成所配溶液浓度偏小的原因可能是____ (填标号)。
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线
B.向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤后未晾干
C.定容时俯视刻度线
D.洗涤液移入容量瓶中时,洒出一部分
(1)本实验需硫酸铜晶体的质量为
(2)应选用
(3)某同学将称量好的硫酸铜晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯内壁和玻璃棒2~3次,洗涤液也转移至容量瓶中,然后加蒸馏水至液面距离容量瓶的刻度线1~2cm时,用胶头滴管加蒸馏水至刻度线,最后将溶液转移到试剂瓶中。指出上述操作中的3个错误。
①
②
③
(4)配制上述溶液时,造成所配溶液浓度偏小的原因可能是
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线
B.向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤后未晾干
C.定容时俯视刻度线
D.洗涤液移入容量瓶中时,洒出一部分
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验需要80mL1.00 mol/L Na2CO3溶液,现用碳酸钠晶体(Na2CO3·10H2O)进行配制,回答下列问题:
(1)所需主要仪器为:药匙、托盘天平、烧杯、___________ 、___________ 和胶头滴管。
(2)本实验须用托盘天平称量碳酸钠晶体(Na2CO3•10H2O)___________ g。
(3)试分析下列操作,对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”):
①若定容时仰视读数,会导致所配溶液浓度___________ 。
②若摇匀后发现液面低于刻度线再加水,会导致所配溶液浓度___________ 。
(1)所需主要仪器为:药匙、托盘天平、烧杯、
(2)本实验须用托盘天平称量碳酸钠晶体(Na2CO3•10H2O)
(3)试分析下列操作,对所配溶液的浓度有何影响(填“偏高”“偏低”或“无影响”):
①若定容时仰视读数,会导致所配溶液浓度
②若摇匀后发现液面低于刻度线再加水,会导致所配溶液浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学生计划用12 mol·L-1的浓盐酸配制0.10 mol·L-1的稀盐酸450 mL。回答下列问题:
(1)量取浓盐酸的体积为________ mL,应选用的量筒规格为________ 。
(2)配制时应选用的容量瓶规格为__________ 。
(3)配制时(除容量瓶外)还需选用的仪器主要有______ 、________ 、________ 、________ 和试剂瓶。
(4)定容时应用什么仪器?_________________________________________ 。
如何观察刻度线?________________________________________________ 。
定容时超过刻度线,如何操作?________________________________________________ 。
(1)量取浓盐酸的体积为
(2)配制时应选用的容量瓶规格为
(3)配制时(除容量瓶外)还需选用的仪器主要有
(4)定容时应用什么仪器?
如何观察刻度线?
定容时超过刻度线,如何操作?
您最近一年使用:0次



