下面是我们熟悉的物质:①O2 ②NaBr ③H2SO4 ④Na2CO3 ⑤NH4Cl ⑥NaHSO4 ⑦Ne ⑧Na2O2 ⑨NaOH ⑩CO2。
(1)这些物质中,只含有共价键的是_______ ;只含有离子键的是_______ ;不存在化学键的是_______ (填物质序号)。
(2)属于共价化合物的是_______ (填物质序号)。
(3)CO2固体气化破坏了_______ 。
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)CO2固体气化破坏了
更新时间:2022-06-05 19:41:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】非金属元素在化工生产中扮演着重要角色。其中硅是无机非金属材料的重要组成元素;在众多的化工原料和产品中,都能见到氮元素的踪迹。
I.回答下列问题:
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是______ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:_______ 。
②熔化烧碱应选用的坩埚为______ (填字母)。
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
II.某化学小组模拟工业生产制取HNO3,设计了如图所示装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置E中主要反应的化学方程式为_______ 。
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式______ 。
(5)装置C中浓硫酸的主要作用是______ 。
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:
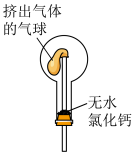
①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是______ 。由此,该同学得出结论:不能用CaCl2代替碱石灰。
I.回答下列问题:
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:
②熔化烧碱应选用的坩埚为
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
II.某化学小组模拟工业生产制取HNO3,设计了如图所示装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置E中主要反应的化学方程式为
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式
(5)装置C中浓硫酸的主要作用是
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:

①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氯化碳,有下列反应:2Na[Al(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O。
(1)上述五种物质中沸点最低物质的结构式为______ ,由上述物质中的两种元素按原子个数比1:1形成的离子化合物的电子式为______ (写一例)。
(2)请将Na、Al、O的原子半径和简单离子的半径分别按由小到大的顺序排列:______ (用元素符号表示),______ (用离子符号表示)。
(3)①在上述混合物的组成元素中,与铝元素同周期的另一元素的原子共有______ 种不同能级的电子,该元素的最高价氧化物对应水合物与铝单质反应的离子反应方程式为______ 。
②已知AlN的熔点2200℃,AlCl3的熔点194℃,二者常温下均为固体,其熔点差异较大的原因是______ 。
(4)NaHCO3溶液中各含碳微粒按浓度由大到小的顺序排列______ 。
(1)上述五种物质中沸点最低物质的结构式为
(2)请将Na、Al、O的原子半径和简单离子的半径分别按由小到大的顺序排列:
(3)①在上述混合物的组成元素中,与铝元素同周期的另一元素的原子共有
②已知AlN的熔点2200℃,AlCl3的熔点194℃,二者常温下均为固体,其熔点差异较大的原因是
(4)NaHCO3溶液中各含碳微粒按浓度由大到小的顺序排列
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.厨房中有下列用品:①食盐②小苏打③纯碱④食醋(主要成分为醋酸)。
(1)主要成分属于酸的是_______ (填序号);
(2)水溶液呈碱性的是_______ (填序号);
(3)食盐在水中的电离方程式是_______ 。
(4)纯碱中含有少量NaCl。检验此混合物中的 、
、 的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
向第一支试管中加入稀盐酸,可观察到产生无色气泡,说明溶液中存在_______ 离子,该反应的离子方程式为_______ 。
向第二支试管中先加入足量稀硝酸,再加入_______ 溶液,可观察到白色沉淀,说明溶液中存在 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
Ⅱ. 和
和 热稳定性对比实验如下图所示。
热稳定性对比实验如下图所示。
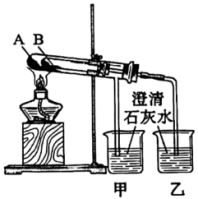
(5)物质A是_______ (填化学式)。
(6)能够证明 的热稳定性强于
的热稳定性强于 的证据是
的证据是_______ 。
(7)试管中发生反应的化学方程式是_______ 。烧杯中发生反应的离子方程式是_______ 。
(1)主要成分属于酸的是
(2)水溶液呈碱性的是
(3)食盐在水中的电离方程式是
(4)纯碱中含有少量NaCl。检验此混合物中的
 、
、 的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,说明溶液中存在
向第二支试管中先加入足量稀硝酸,再加入
 ,该反应的离子方程式为
,该反应的离子方程式为Ⅱ.
 和
和 热稳定性对比实验如下图所示。
热稳定性对比实验如下图所示。
(5)物质A是
(6)能够证明
 的热稳定性强于
的热稳定性强于 的证据是
的证据是(7)试管中发生反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是________ 。
①两种原子构成的共价化合物分子中的化学键都是极性键
②含有非极性键的化合物一定是共价化合物
③难失去电子的原子,易形成阴离子
④单质分子中不存在化学键,化合物的分子中才存在化学键
⑤非金属元素原子组成的化合物不可能是离子化合物
⑥共价化合物中不可能含有离子键
⑦在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子,原子核与原子核之间的排斥作用
⑧离子化合物中可能含共价键
⑨两种非金属原子间不可能形成离子键
⑩标准状况下,2.24 L CCl4含有的共价键数为0.4NA
⑪碳酸亚乙烯酯(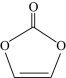 )分子中只有极性键
)分子中只有极性键
⑫硫化钠的电子式: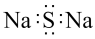
①两种原子构成的共价化合物分子中的化学键都是极性键
②含有非极性键的化合物一定是共价化合物
③难失去电子的原子,易形成阴离子
④单质分子中不存在化学键,化合物的分子中才存在化学键
⑤非金属元素原子组成的化合物不可能是离子化合物
⑥共价化合物中不可能含有离子键
⑦在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子,原子核与原子核之间的排斥作用
⑧离子化合物中可能含共价键
⑨两种非金属原子间不可能形成离子键
⑩标准状况下,2.24 L CCl4含有的共价键数为0.4NA
⑪碳酸亚乙烯酯(
 )分子中只有极性键
)分子中只有极性键⑫硫化钠的电子式:
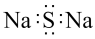
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)由表中①、④两种元素的原子按1∶1组成的常见液态化合物的电子式_______ 。
(2)②、③、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:_____ 。将⑧形成的单质充入①、④、⑤形成的化合物的水溶液中,写出反应的离子方程式_____ 。
(4)断开1 mol 由①元素原子形成的单质中的共价单键、1 mol由③①形成的化合物中的共价单键 、1 mol 元素③形成的单质中的共价叁键分别需要吸收的能量为436 kJ、391 kJ、946 kJ。求:1 mol 元素③形成的单质完全反应生成由③①形成的化合物需放出_______ kJ。

(1)由表中①、④两种元素的原子按1∶1组成的常见液态化合物的电子式
(2)②、③、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:
(4)断开1 mol 由①元素原子形成的单质中的共价单键、1 mol由③①形成的化合物中的共价单键 、1 mol 元素③形成的单质中的共价叁键分别需要吸收的能量为436 kJ、391 kJ、946 kJ。求:1 mol 元素③形成的单质完全反应生成由③①形成的化合物需放出
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学与人类生活、生产密切相关.请根据题意回答下列问题:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。光导纤维的主要成分是__ (填化学式)。下列物质属于硅酸盐产品的是__ (填标号)。
A.生活中的陶瓷餐具
B.商场售卖的水晶项链
C.实验室的石英坩埚
D.建造桥梁的水泥
(2)在氮气和含氮化合物中:常用作保护气的物质是__ (填化学式);常用作制冷剂的是__ (填化学式),其原因是__ 。氮元素的最高价氧化物对应的水化物与氮元素的最简单氢化物反应生成的产物为__ (填化学式),该化合物所含化学键类型为__ 。
(3)通过海水晾晒可得粗盐,粗盐中除含有NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。
①可通过化学沉淀法除去粗盐中的杂质离子(Mg2+、Ca2+、SO ),需要使用的除杂试剂有Na2CO3溶液、BaCl2溶液、NaOH溶液。加入试剂的顺序是
),需要使用的除杂试剂有Na2CO3溶液、BaCl2溶液、NaOH溶液。加入试剂的顺序是__ 、NaOH溶液、__ 。
②沉淀完全后,过滤,所得滤液中的阴离子有__ (填离子符号),需要加入__ (填试剂名称)调节至中性。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。光导纤维的主要成分是
A.生活中的陶瓷餐具
B.商场售卖的水晶项链
C.实验室的石英坩埚
D.建造桥梁的水泥
(2)在氮气和含氮化合物中:常用作保护气的物质是
(3)通过海水晾晒可得粗盐,粗盐中除含有NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。
①可通过化学沉淀法除去粗盐中的杂质离子(Mg2+、Ca2+、SO
 ),需要使用的除杂试剂有Na2CO3溶液、BaCl2溶液、NaOH溶液。加入试剂的顺序是
),需要使用的除杂试剂有Na2CO3溶液、BaCl2溶液、NaOH溶液。加入试剂的顺序是②沉淀完全后,过滤,所得滤液中的阴离子有
您最近一年使用:0次



