下列实验对应的离子方程式不正确 的是
A.将少量 通入 通入 溶液: 溶液: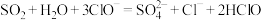 |
B. 溶液中 溶液中 的电离: 的电离: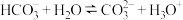 |
C.将碳酸氢钙溶液与过量的氨水混合: |
D.电解精炼铜的阴极反应式: |
21-22高二下·浙江·阶段练习 查看更多[2]
更新时间:2022-05-27 11:11:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】以重晶石( )为原料,可按如下工艺生产立德粉(
)为原料,可按如下工艺生产立德粉( ):
):

下列说法不正确的是
 )为原料,可按如下工艺生产立德粉(
)为原料,可按如下工艺生产立德粉( ):
):
下列说法不正确的是
A.在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为 |
B.回转炉尾气中含有有毒气体,生产上可通过水蒸气变换将其转化为 和一种清洁能源气体,该反应的化学方程式为 和一种清洁能源气体,该反应的化学方程式为 |
C.在潮湿空气中长期放置的“还原料”会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的 |
D.沉淀器中发生的离子反应方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】能正确表示下列反应的离子方程式为
A.向 溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl- 溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
B.向碳酸钠溶液中通入少量CO2:CO + CO2+H2O=2HCO + CO2+H2O=2HCO |
C.NH4HCO3溶于少量的浓KOH溶液中:NH +HCO +HCO +2OH﹣=CO +2OH﹣=CO +NH3↑+2 H2O +NH3↑+2 H2O |
D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO 沉淀完全:2Al3++3SO 沉淀完全:2Al3++3SO +3Ba2++6OH﹣=2 Al(OH)3↓+3BaSO4↓ +3Ba2++6OH﹣=2 Al(OH)3↓+3BaSO4↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列解释事实的方程式不正确的是
A.向AgCl悬浊液中加入Na2S溶液: |
B.硫酸亚铁溶液中加入过氧化氢溶液: |
C.向NaHCO3溶液中加入NaOH溶液: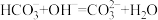 |
D.硫酸铜溶液中加入氢氧化钡溶液: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列指定反应的离子方程式正确的是
| A.向0.1mol/LNaHA溶液(pH=1)加入NaOH溶液:HA﹣+OH﹣→A2﹣+H2O |
B.像Ca(HCO3)2溶液中加入足量NaOH溶液:Ca2++2HCO +2OH﹣=CaCO3↓+CO +2OH﹣=CaCO3↓+CO +2H2O +2H2O |
C.Na2S2O3溶液与硝酸溶液混合:S2O +2H+→S↓+SO2↑+H2O +2H+→S↓+SO2↑+H2O |
| D.溴化亚铁溶液中通入足量氯气:2Fe2++2Br﹣+2Cl2→2Fe3++Br2+4Cl﹣ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2和NO2是主要大气污染物,利用如图装置可同时吸收SO2和NO。已知电解池的阴极室中溶液的pH保持在4~7之间。下列说法正确的是


| A.电极a为直流电源的正极 |
| B.电解过程中,阳极区电解液的pH增大 |
C.阴极反应式为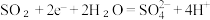 |
D.吸收NO的离子方程式为2NO+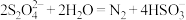 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知氧化性Fe3+>I2。向含a mol FeI2的溶液中通入b mol Cl2,充分反应。下列说法不正确的是
| A.离子的还原性强弱:I->Fe2+>Cl- |
B.当a≥b时,发生的离子反应为2I-+Cl2 I2+2Cl- I2+2Cl- |
| C.当a=2b时,反应后的离子浓度之比:c(Fe2+)∶c(I-)∶c(Cl-)=1∶2∶1 |
D.当3a≤2b时,发生的离子反应为2Fe2++4I-+3Cl2 2Fe3++2I2+6Cl- 2Fe3++2I2+6Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】三氧化二镍(Ni2O3)可用于制造高能电池元件。电解法制备过程如 下:用NaOH 溶液将NiCl2溶液的pH调至7.5,加入适量硫酸钠固体 后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍(可简单写成Ni2+)氧化为Ni3+,再将Ni3+经一系列反应后转化为Ni2O3.电解装置如图所示。下列说法不正确的是( )


| A.加入适量硫酸钠的作用是增加离子浓度,增强溶液的导电能力 |
| B.电解过程中阳极附近溶液的pH降低 |
| C.电解过程中,溶液中的Cl-经阳离子交换膜向阳极移动 |
| D.ClO-氧化Ni2+的离子方程式为:ClO-+H2O+2Ni2+=Cl-+2Ni3++2OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.向CH3COOH溶液中加入少量醋酸钠固体,CH3COOH的电离程度增大 |
| B.电解精炼铜时,阳极质量减少3.2 g,反应过程中一定转移6.02×1022个电子 |
| C.室温下,向0.1 mol·L-1NH4Cl溶液中加水,促进水解,溶液的pH变小 |
| D.锅炉水垢中的CaSO4可用Na2CO3溶液浸泡后再用盐酸清洗 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列是部分矿物资源的利用及产品流程,有关说法正确的是
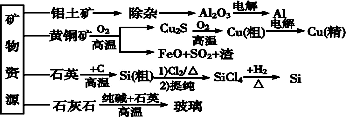

| A.粗铜电解精炼时,粗铜作阴极 |
| B.生产铝、铜、高纯硅和玻璃的过程中都涉及氧化还原反应 |
| C.黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶铁的原料 |
| D.生产玻璃过程中体现了碳酸的酸性强于硅酸 |
您最近一年使用:0次

 2C6H5OH+CO32-
2C6H5OH+CO32- 反应:
反应: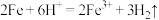

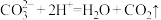
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-

