某化学兴趣小组利用如图装置模拟工业 的催化氧化过程,并研究二氧化硫的性质。已知:
的催化氧化过程,并研究二氧化硫的性质。已知: 熔点为16.8℃。
熔点为16.8℃。
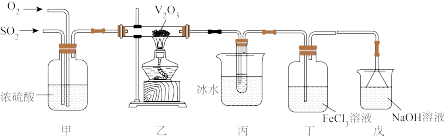
(1)该实验的操作顺序为:组装仪器→_______ →装药品→开始实验。
(2) 在乙中催化氧化,写出该反应的化学方程式
在乙中催化氧化,写出该反应的化学方程式_______ 。
(3)丙装置中冰水的作用是_______ 。
(4)写出丁中反应的离子方程式_______ 。
(5)戊装置中倒扣漏斗的作用是_______ 。
 的催化氧化过程,并研究二氧化硫的性质。已知:
的催化氧化过程,并研究二氧化硫的性质。已知: 熔点为16.8℃。
熔点为16.8℃。
(1)该实验的操作顺序为:组装仪器→
(2)
 在乙中催化氧化,写出该反应的化学方程式
在乙中催化氧化,写出该反应的化学方程式(3)丙装置中冰水的作用是
(4)写出丁中反应的离子方程式
(5)戊装置中倒扣漏斗的作用是
更新时间:2022/06/16 23:01:07
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,一实验小组欲通过如图装置探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化)

(1)该反应中MnO 被还原为Mn2+,写出相应反应的离子方程式:
被还原为Mn2+,写出相应反应的离子方程式:___________
(2)该实验探究的是___________ 因素对化学反应速率的影响。针筒内收集相同体积的CO2所用时间是①___________ ②(填“>”、“<"或“=”)
(3)本实验还可通过测定___________ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是___________

(5)草酸是一个二元弱酸,写出草酸在水中的第一步电离方程式___________ ,该步电离的平衡常数表达式K=___________

| 实验序号 | A溶液 | B溶液 |
| ① | 20mL0.1 mol/L H2C2O4溶液 | 30mL 0.01 mol/L KMnO4溶液 |
| ② | 20mL0.2mol/L H2C2O4溶液 | 30mL0.01 mol/L KMnO4溶液 |
 被还原为Mn2+,写出相应反应的离子方程式:
被还原为Mn2+,写出相应反应的离子方程式:(2)该实验探究的是
(3)本实验还可通过测定
(4)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是

(5)草酸是一个二元弱酸,写出草酸在水中的第一步电离方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】为除去粗盐中的少量 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐 滤液
滤液 精盐
精盐
(1)加入过量 溶液的目的是除去粗盐中的
溶液的目的是除去粗盐中的___________ 。
(2)第③步的目的是除去粗盐中的 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)第④步的反应的离子方程式为___________ 、___________ 。
 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
 滤液
滤液 精盐
精盐(1)加入过量
 溶液的目的是除去粗盐中的
溶液的目的是除去粗盐中的(2)第③步的目的是除去粗盐中的
 ,反应的离子方程式为
,反应的离子方程式为(3)第④步的反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液。废液处理流程如图:

(1)步骤(Ⅰ)中涉及反应的离子方程式:__ ;__ 。
(2)沉淀B中主要含有__ ,气体D是__ 。
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式__ 。
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:__ 。
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为__ 。

(1)步骤(Ⅰ)中涉及反应的离子方程式:
(2)沉淀B中主要含有
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2等中学化学教材中出现过的物质,根据它们的组成及性质进行如下分类。
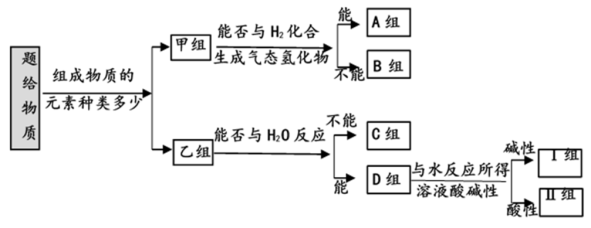
请回答下列问题:
(1)上述分类方法属于___________ 分类法(填“树状”或“交叉”)
(2)SO2是形成酸雨的主要物质,用化学方程式表示形成硫酸酸雨的原理___________ 、___________
(3)Na2O2最终位于___________ 组;它的主要用途为___________ 。(任写一条)
(4)C组某气体在标准状态下与氧气按一定体积比混合盛满一试管中,将试管倒置于水槽中一段时间,试管充满溶液,则试管中溶液溶质的物质的量浓度为___________ mol/L(已知:4NO+3O2+2H2O=4HNO3)
(5)N2H4是一种高能燃料,有强还原性,可通过Ⅰ组的某种物质和NaClO反应制得。该制备反应的化学方程式为___________ 。

请回答下列问题:
(1)上述分类方法属于
(2)SO2是形成酸雨的主要物质,用化学方程式表示形成硫酸酸雨的原理
(3)Na2O2最终位于
(4)C组某气体在标准状态下与氧气按一定体积比混合盛满一试管中,将试管倒置于水槽中一段时间,试管充满溶液,则试管中溶液溶质的物质的量浓度为
(5)N2H4是一种高能燃料,有强还原性,可通过Ⅰ组的某种物质和NaClO反应制得。该制备反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示。已知A是淡黄色固体,请回答下列问题:
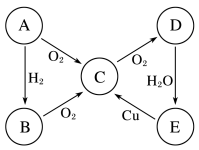
(1)写出B、E的化学式:B________ 、E________ 。
(2)C→D的化学方程式为________ ;E→C的化学方程式为________ ;B与C反应的化学方程式为________ 。
(3)将足量的物质C通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是________ (填标号)。
a.溶液没有明显变化 b.溶液中出现白色沉淀
c.若继续通入 ,则溶液中出现白色沉淀
,则溶液中出现白色沉淀

(1)写出B、E的化学式:B
(2)C→D的化学方程式为
(3)将足量的物质C通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是a.溶液没有明显变化 b.溶液中出现白色沉淀
c.若继续通入
 ,则溶液中出现白色沉淀
,则溶液中出现白色沉淀
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
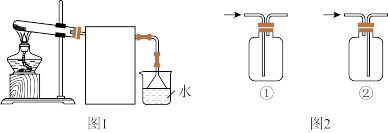
【推荐3】Ⅰ. 具有广泛的用途。实验室常用如图所示装置制取并收集
具有广泛的用途。实验室常用如图所示装置制取并收集 。
。
(1)实验室用 和
和 制取
制取 的化学方程式为
的化学方程式为_______ 。
(2)干燥 常选用的干燥剂是
常选用的干燥剂是_______ 。
(3)图1中方框内收集 的装置可选用图2中的
的装置可选用图2中的_______ (填序号)。
(4)尾气处理装置中使用倒置漏斗的作用是_______ 。
Ⅱ.二氧化硫是重要的工业原料,探究其性质具有非常重要的意义。
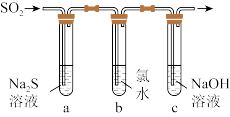
(5)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为_______ 。
②写出试管b中发生反应的离子方程式:_______ 。
(6)实验室中用如图装置测定 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为16.8℃,假设气体进入装置时均被完全吸收,且忽略空气中
的熔点为16.8℃,假设气体进入装置时均被完全吸收,且忽略空气中 的影响)
的影响)
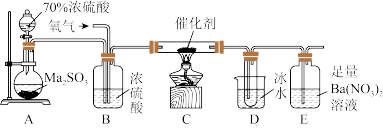
①当停止通入 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是_______ 。
②实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是_______ (用含字母的代数式表示,不用化简)。
 具有广泛的用途。实验室常用如图所示装置制取并收集
具有广泛的用途。实验室常用如图所示装置制取并收集 。
。
(1)实验室用
 和
和 制取
制取 的化学方程式为
的化学方程式为(2)干燥
 常选用的干燥剂是
常选用的干燥剂是(3)图1中方框内收集
 的装置可选用图2中的
的装置可选用图2中的(4)尾气处理装置中使用倒置漏斗的作用是
Ⅱ.二氧化硫是重要的工业原料,探究其性质具有非常重要的意义。

(5)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为
②写出试管b中发生反应的离子方程式:
(6)实验室中用如图装置测定
 被催化氧化为
被催化氧化为 的转化率。(已知
的转化率。(已知 的熔点为16.8℃,假设气体进入装置时均被完全吸收,且忽略空气中
的熔点为16.8℃,假设气体进入装置时均被完全吸收,且忽略空气中 的影响)
的影响)
①当停止通入
 ,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是②实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如表所示3组,第2组中物质X的化学式是___ 。
(2)利用如图所示的装置研究SO2的性质:
已知熔点:SO2-76.1℃,SO316.8℃沸点:SO2-10℃,SO345℃
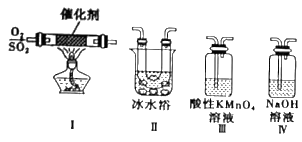
①装置I模拟工业生产SO2催化氧化的反应,其化学方程式是___ 。
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是___ 。
③乙同学按I、II、IV的顺序连接装置,装置IV中有40mL2.5mol/LNaOH溶液,反应后增重4.8g,则装置IV中发生反应所得产物的化学式是___ 。
(1)将相关的含硫物质分为如表所示3组,第2组中物质X的化学式是
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
已知熔点:SO2-76.1℃,SO316.8℃沸点:SO2-10℃,SO345℃

①装置I模拟工业生产SO2催化氧化的反应,其化学方程式是
②甲同学按I、II、III、IV的顺序连接装置,装置II的作用是
③乙同学按I、II、IV的顺序连接装置,装置IV中有40mL2.5mol/LNaOH溶液,反应后增重4.8g,则装置IV中发生反应所得产物的化学式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
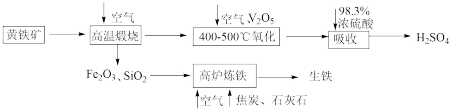
【推荐2】硫酸是重要的化工原料,可用于生产化肥、农药、炸药等。工业上以黄铁矿(主要成分为FeS2,含有少量SiO2杂质)为主要原料制备硫酸的工艺流程如下图所示:
回答下列问题:
(1)“高温煅烧”前,将黄铁矿粉碎的目的是_______ ;煅烧时发生反应的化学方程式为_______ 。
(2)“氧化”时,发生反应的化学方程式为_______ 。
(3)“吸收”时,从SO3的性质角度分析,选用98.3%浓硫酸而不用水的主要原因是_______ 。
(4)研究证明,高炉中Fe2O3与CO反应不能完全转化为CO2和Fe,据此写出高炉炼铁时Fe2O3与CO反应的化学方程式:_______ ;若投入Fe2O3的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中Fe2O3的转化率为_______ 。

回答下列问题:
(1)“高温煅烧”前,将黄铁矿粉碎的目的是
(2)“氧化”时,发生反应的化学方程式为
(3)“吸收”时,从SO3的性质角度分析,选用98.3%浓硫酸而不用水的主要原因是
(4)研究证明,高炉中Fe2O3与CO反应不能完全转化为CO2和Fe,据此写出高炉炼铁时Fe2O3与CO反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某校化学小组的同学开展了一系列的化学实验活动。
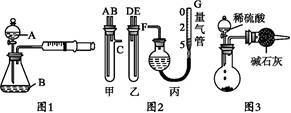
请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录______ 得到反应速率为x mol·(L·min)-1.实验开始时检查该装置气密性的方法是______ 。
(2)乙同学用图2装置测定Na2CO3和NaCl的固体混合物中Na2CO3的质量分数:
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于______ 、__ 仪器中(填仪器编号);
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器是______ ;
③仪器甲、乙接口的连接方式如下:A连接__ ,B连接______ ,C连接______ (填写各接口的编号);
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是______ 。
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差_____ ,请你分析其中使测定结果可能偏大的主要原因______ 。

请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录
(2)乙同学用图2装置测定Na2CO3和NaCl的固体混合物中Na2CO3的质量分数:
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器是
③仪器甲、乙接口的连接方式如下:A连接
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3- )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。
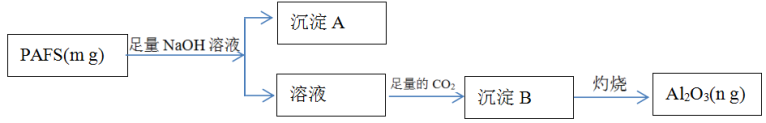
回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__ 。
(2)PAFS中铁元素的化合价为_______ ;沉淀A的化学式为_________ 。
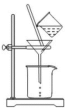
(3)如图所示,过滤操作中的一处错误是__________ 。
(4)生成沉淀B的离子方程式为______ 。
(5)PAFS中Al元素的质量分数为_______ (用同m、n的代数式表示)。
 )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。
回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
(2)PAFS中铁元素的化合价为
(3)如图所示,过滤操作中的一处错误是

(4)生成沉淀B的离子方程式为
(5)PAFS中Al元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】用海带制备单质碘,制备过程如下:
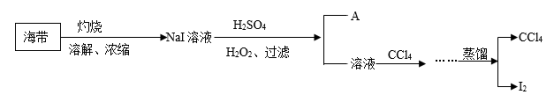
已知:常温下,碘在水中的溶解度为0.034g;碘的沸点为184℃;CCl4的沸点为77℃。
请回答:
(1)A物质是__________ 。
(2)写出在酸化下用H2O2氧化NaI的化学反应方程式_________________ 。
(3)流程中省略部分的操作是_____________ 。
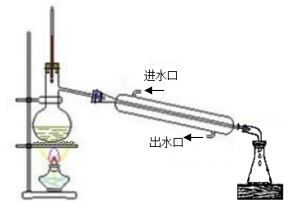
(4)蒸馏装置中错误的是__________________ (写三条)。
(5)蒸馏出的CCl4液体中常会带淡紫色,可能的原因是______________

已知:常温下,碘在水中的溶解度为0.034g;碘的沸点为184℃;CCl4的沸点为77℃。

请回答:
(1)A物质是
(2)写出在酸化下用H2O2氧化NaI的化学反应方程式
(3)流程中省略部分的操作是
(4)蒸馏装置中错误的是
(5)蒸馏出的CCl4液体中常会带淡紫色,可能的原因是
您最近一年使用:0次



