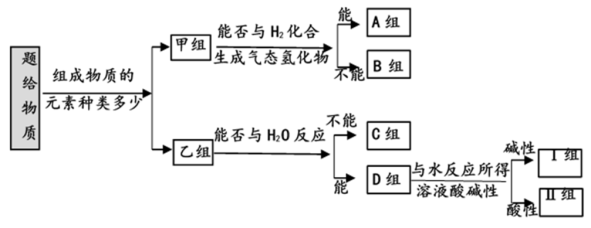
现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2等中学化学教材中出现过的物质,根据它们的组成及性质进行如下分类。
请回答下列问题:
(1)上述分类方法属于___________ 分类法(填“树状”或“交叉”)
(2)SO2是形成酸雨的主要物质,用化学方程式表示形成硫酸酸雨的原理___________ 、___________
(3)Na2O2最终位于___________ 组;它的主要用途为___________ 。(任写一条)
(4)C组某气体在标准状态下与氧气按一定体积比混合盛满一试管中,将试管倒置于水槽中一段时间,试管充满溶液,则试管中溶液溶质的物质的量浓度为___________ mol/L(已知:4NO+3O2+2H2O=4HNO3)
(5)N2H4是一种高能燃料,有强还原性,可通过Ⅰ组的某种物质和NaClO反应制得。该制备反应的化学方程式为___________ 。

请回答下列问题:
(1)上述分类方法属于
(2)SO2是形成酸雨的主要物质,用化学方程式表示形成硫酸酸雨的原理
(3)Na2O2最终位于
(4)C组某气体在标准状态下与氧气按一定体积比混合盛满一试管中,将试管倒置于水槽中一段时间,试管充满溶液,则试管中溶液溶质的物质的量浓度为
(5)N2H4是一种高能燃料,有强还原性,可通过Ⅰ组的某种物质和NaClO反应制得。该制备反应的化学方程式为
更新时间:2021-06-07 15:18:37
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
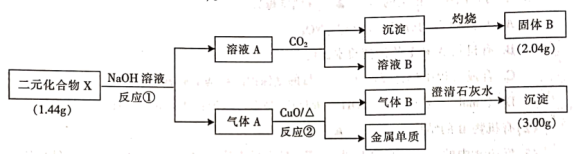
【推荐1】为探究二元化合物X的组成和性质,某研究小组设计并完成了如下实验(步骤中所加试剂均过量,部分产物已略去)。
请回答下列问题:
(1)写出X中含有的元素________ (用元素符号表示)。
(2)写出反应①的离子方程式___________ 。
(3)写出反应②的化学方程式___________ 。
(4)设计实验检验溶液B中所含溶质的阴离子:________ 。

请回答下列问题:
(1)写出X中含有的元素
(2)写出反应①的离子方程式
(3)写出反应②的化学方程式
(4)设计实验检验溶液B中所含溶质的阴离子:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
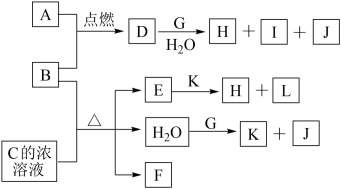
【推荐2】图中,A~L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见的金属单质,E的稀溶液为蓝色,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味的气体,且能使品红溶液褪色.
请回答下列问题:
(1)框图中所列物质中属于非电解质的物质是___ ;
(2)将D的水溶液蒸干并灼烧得到的固体物质的化学式为___ ;
(3)在一定物质的量浓度的硝酸铵溶液中滴加适量的K溶液,使溶液的pH=7,则溶液中c(Na+)___ c(NO )(选填“>”“=”或“<”)。
)(选填“>”“=”或“<”)。
(4)与F组成元素相同的一种−2价酸根离子M,M中两种元素的质量比为4:3,已知1molA单质与含1molM的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生,取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。则A单质与含M的溶液反应的离子方程式为:___ 。
(5)25℃时,若Ksp(H)=2.2×10−20,向0.022 mol∙L−1的E溶液中逐滴滴入溶液K,当开始出现沉淀时,溶液中的c(OH-)=__ 。

请回答下列问题:
(1)框图中所列物质中属于非电解质的物质是
(2)将D的水溶液蒸干并灼烧得到的固体物质的化学式为
(3)在一定物质的量浓度的硝酸铵溶液中滴加适量的K溶液,使溶液的pH=7,则溶液中c(Na+)
 )(选填“>”“=”或“<”)。
)(选填“>”“=”或“<”)。(4)与F组成元素相同的一种−2价酸根离子M,M中两种元素的质量比为4:3,已知1molA单质与含1molM的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生,取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。则A单质与含M的溶液反应的离子方程式为:
(5)25℃时,若Ksp(H)=2.2×10−20,向0.022 mol∙L−1的E溶液中逐滴滴入溶液K,当开始出现沉淀时,溶液中的c(OH-)=
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。其中A为气体,A~F 都含有相同的元素。
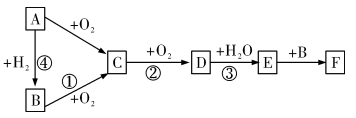
试回答下列问题:
(1)写出下列物质的化学式:C_______ 、F_______ 。
(2)在反应①中,34gB发生反应后放出452.9kJ的热量,请写出该反应的热化学方程式________ 。
(3)③的化学方程式为__________ ,该反应氧化剂与还原剂的物质的量之比为______ 。
(4)铜与E的浓溶液反应的离子方程式为__________ 。
(5)25.6g铜与含有1.4molE的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)__________ L。

试回答下列问题:
(1)写出下列物质的化学式:C
(2)在反应①中,34gB发生反应后放出452.9kJ的热量,请写出该反应的热化学方程式
(3)③的化学方程式为
(4)铜与E的浓溶液反应的离子方程式为
(5)25.6g铜与含有1.4molE的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】书到用时方恨少,该题又是周期表;众里寻他千百度,答案还得自己找!下表是元素周期表中的一部分,回答下列问题:

(1)元素①的氢化物的化学式是________ ;该元素的一种氧化物是红棕色气体,请写出该气体溶于水时发生反应的离子方程式_________________________ ;
(2)原子半径:②____ ③(填“>”“ <”或“=”),
(3)元素④的名称是______ ;
(4)元素的非金属性:⑤_____ ⑥(填“>”或“<”)。

(1)元素①的氢化物的化学式是
(2)原子半径:②
(3)元素④的名称是
(4)元素的非金属性:⑤
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】利用石灰乳和硝酸工业的尾气(含NO、 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下:

(1)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是________ ;滤渣可循环使用,滤渣的主要成分是_________ (填化学式)。
(2)该工艺需控制NO和 物质的量之比接近1∶1。若
物质的量之比接近1∶1。若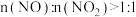 ,则会导致
,则会导致___________ ;若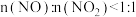 ,则会导致
,则会导致______ 。
(3)生产中溶液需保持弱碱性,在酸性溶液中 会发生分解,产物之一是NO,其反应的离子方程式为
会发生分解,产物之一是NO,其反应的离子方程式为______________________________ 。
 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,其部分工艺流程如下:
,其部分工艺流程如下:
(1)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是
(2)该工艺需控制NO和
 物质的量之比接近1∶1。若
物质的量之比接近1∶1。若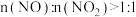 ,则会导致
,则会导致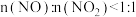 ,则会导致
,则会导致(3)生产中溶液需保持弱碱性,在酸性溶液中
 会发生分解,产物之一是NO,其反应的离子方程式为
会发生分解,产物之一是NO,其反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检验装置气密性,实验前用排水法收集半瓶NO气体。

(1)打开止水夹a,推动针筒活塞,使O2进入烧瓶。关闭止水夹,首先观察到烧瓶中的现象:_______ ,产生此现象的化学方程式为_______ 。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象为
①烧瓶中的气体从_______ 色变成_______ 色;
②烧杯中导管的水位_______ (填上升、下降或不变)。产生此现象的化学方程式为_______ 。

(1)打开止水夹a,推动针筒活塞,使O2进入烧瓶。关闭止水夹,首先观察到烧瓶中的现象:
(2)轻轻摇动烧瓶,观察到烧瓶中的现象为
①烧瓶中的气体从
②烧杯中导管的水位
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】某单质A经如下图所示的过程,请回答下列问题:
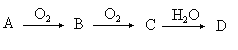
(1)若A为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:A__________ D__________
②工业生产中大量排放的B气体被雨水吸收后形成___________ 而污染环境。
③写出B→C反应的化学方程式:__________________________________________
(2)若C为淡黄色固体。
①C的电子式为___________ ,C中阴阳离子数目比为_________
②写出C→D反应的离子方程式:___________________________________________

(1)若A为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:A
②工业生产中大量排放的B气体被雨水吸收后形成
③写出B→C反应的化学方程式:
(2)若C为淡黄色固体。
①C的电子式为
②写出C→D反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
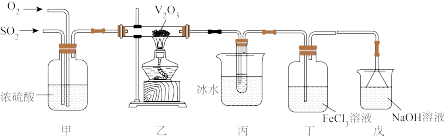
【推荐2】硫代硫酸钠(Na2S2O3),又名大苏打,易溶于水,易被氧化,遇酸易分解;其工业制备原理为2Na2S+Na2CO3+4SO2==3Na2S2O3+CO2,用途广泛,其中之一为处理含氰化钠的废水。实验室通过如下图所示装置制备Na2S2O3。
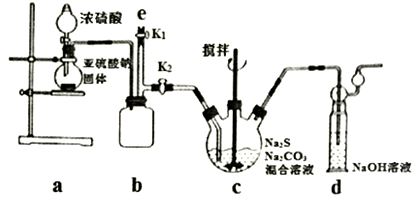
(1)实验中生成SO2的化学方程式_________________________________ 。
(2)b装置的作用是___________________ 。
(3)反应开始后,c中观察到逐渐析出了淡黄色固体,后又消失的现象,请用离子方程式解释淡黄色固体出现的原因______________________________________ 。
(4)实验结束后,在e处最好连接盛_________ 的仪器,目的是___________________ 。
(5)为了提高产品的产量,通入的SO2不能过量,原因是___________________ 。
(6)测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:取20.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准六AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定终点的现象:_____________________ ;处理后的废水是否达到排放标准:____________ (填“是”或“否”)。

(1)实验中生成SO2的化学方程式
(2)b装置的作用是
(3)反应开始后,c中观察到逐渐析出了淡黄色固体,后又消失的现象,请用离子方程式解释淡黄色固体出现的原因
(4)实验结束后,在e处最好连接盛
(5)为了提高产品的产量,通入的SO2不能过量,原因是
(6)测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:取20.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准六AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定终点的现象:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】图中,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
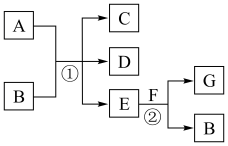
(1)A的名称为_______ ,F的重要用途有_______ 。
(2)写出反应①的化学方程式:_______ 。
(3)写出反应②的化学方程式:_______ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是_______ 。
②A与石灰乳反应制得的漂白粉的有效成分是_______ (填化学式),该物质在空气中失效的原因是(写出第一步反应即可)_______ (用化学方程式表示)。

(1)A的名称为
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是
②A与石灰乳反应制得的漂白粉的有效成分是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】根据如图所示装置(部分仪器已略去)回答下列有关问题:

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是___________ (填“I”或“II”),请写出实验甲中较不稳定物质的分解方程式___________ 。
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:___________ 。
(3)下列对Na2O2的叙述中,正确的是___________。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:
(3)下列对Na2O2的叙述中,正确的是___________。
| A.Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 |
| B.Na2O2能与水反应,所以Na2O2可以作气体的干燥剂 |
| C.Na2O2与CO2反应时,Na2O2只作氧化剂 |
| D.Na2O2与CO2反应产生氧气,可用于呼吸面具中氧气的来源 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】过氧化钠( )常用于呼吸面具和潜水艇中的供氧剂。为了验证过氧化钠作供氧剂的反应原理,设计下图实验装置进行实验。
)常用于呼吸面具和潜水艇中的供氧剂。为了验证过氧化钠作供氧剂的反应原理,设计下图实验装置进行实验。
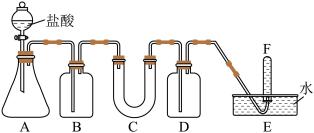
回答下列问题:
(1)用A装置制取二氧化碳气体,盛装盐酸的仪器名称是_______ 。
(2)B中盛有饱和 溶液,B装置的作用是
溶液,B装置的作用是_______ 。
(3)C中盛过氧化钠,它是一种_______ 色的固体;D中所盛试剂是_______ 。
(4)用_______ 检验F中收集到的气体,现象是_______ 。
(5)过氧化钠可作潜水艇乘员供氧剂,其反应原理用化学方程式表示为_______ 、_______ 。某潜水艇中有60名乘员,若每人每小时消耗64g氧气,假设所需要的氧气全由过氧化钠提供,则每小时所需 的质量为
的质量为_______ kg。
 )常用于呼吸面具和潜水艇中的供氧剂。为了验证过氧化钠作供氧剂的反应原理,设计下图实验装置进行实验。
)常用于呼吸面具和潜水艇中的供氧剂。为了验证过氧化钠作供氧剂的反应原理,设计下图实验装置进行实验。
回答下列问题:
(1)用A装置制取二氧化碳气体,盛装盐酸的仪器名称是
(2)B中盛有饱和
 溶液,B装置的作用是
溶液,B装置的作用是(3)C中盛过氧化钠,它是一种
(4)用
(5)过氧化钠可作潜水艇乘员供氧剂,其反应原理用化学方程式表示为
 的质量为
的质量为
您最近一年使用:0次

 的催化氧化过程,并研究二氧化硫的性质。已知:
的催化氧化过程,并研究二氧化硫的性质。已知: 熔点为16.8℃。
熔点为16.8℃。