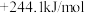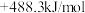已知:
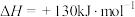 ,
,
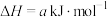 ;
; 、
、 和
和 键的键能(
键的键能( )分别为436、496和462,则
)分别为436、496和462,则 为
为

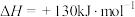 ,
,
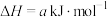 ;
; 、
、 和
和 键的键能(
键的键能( )分别为436、496和462,则
)分别为436、496和462,则 为
为| A.+130 | B.-220 | C.+350 | D.-332 |
21-22高二下·广西河池·阶段练习 查看更多[2]
更新时间:2022-05-31 14:57:52
|
【知识点】 盖斯定律及其有关计算
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐2】已知反应:2NO(g)+Br2(g)=2NOBr(g) △H=-akJ·mol-1(a>0),其反应机理如下:
①NO(g)+Br2(g)=NOBr2(g) △H1快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2慢反应。
下列说法不正确的是( )
①NO(g)+Br2(g)=NOBr2(g) △H1快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2慢反应。
下列说法不正确的是( )
| A.△H=△H1+△H2 |
| B.该反应的速率主要取决于反应① |
| C.NOBr2是该反应的中间产物,不是催化剂 |
| D.恒容时,增大Br2(g)的浓度能增加单位体积活化分子总数,加快反应速率 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐3】工业上,以煤炭为原料,通入一定比例的空气,经过系列反应可以得到满足不同需求的原料气。在C和O2的反应体系中发生如下反应:
反应ⅠC(s)+O2(g)=CO2(g) △H1=-394kJ·mol-l
反应Ⅱ2CO(g)+O2(g)=2CO2(g) △H2=-566kJ·mol-l
反应Ⅲ2C(s)+O2(g)=2CO(g) △H3
设y=△H-T△S,反应Ⅰ、Ⅱ和Ⅲ的y随温度的变化关系如图所示。

下列说法正确的是
反应ⅠC(s)+O2(g)=CO2(g) △H1=-394kJ·mol-l
反应Ⅱ2CO(g)+O2(g)=2CO2(g) △H2=-566kJ·mol-l
反应Ⅲ2C(s)+O2(g)=2CO(g) △H3
设y=△H-T△S,反应Ⅰ、Ⅱ和Ⅲ的y随温度的变化关系如图所示。

下列说法正确的是
| A.反应Ⅲ低温能自发进行,高温下不能自发进行 |
| B.图中对应于反应Ⅱ的线条是a |
| C.一定温度下,增大压强,O2浓度增大,说明在此条件下反应Ⅱ变化的幅度小于反应Ⅲ变化的幅度 |
| D.一定压强下,随着温度的升高,气体中CO与CO2的物质的量之比增大 |
您最近一年使用:0次

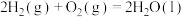
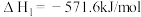

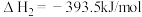
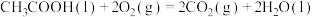
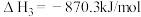
 的反应热
的反应热 为
为