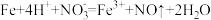下列离子方程式书写正确的是
A.NO2通入水中制硝酸: 2NO2 + H2O = 2H++  + NO + NO |
B.用Na2SO3溶液吸收过量Cl2: + Cl2+ H2O = 2H++2Cl-+ + Cl2+ H2O = 2H++2Cl-+  |
C.过量的铁粉溶于稀硝酸: Fe + 4H++  = Fe3++ NO↑+ 2H2O = Fe3++ NO↑+ 2H2O |
| D.氢氧化钠溶液腐蚀玻璃: 2Na+ + 2OH- + SiO2= Na2SiO3+ H2O |
更新时间:2022-06-01 16:53:38
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确的是
A.AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH↓+ |
B.苯酚钠溶液中通入少量二氧化碳:2 +CO2+H2O +CO2+H2O 2 2 + + |
C.乙醛与新制的碱性氢氧化铜悬浊液加热:CH3CHO+2Cu(OH)2+2OH- CH3COO-+2CuO↓+3H2O CH3COO-+2CuO↓+3H2O |
D.向NaHCO3溶液中加入醋酸: +CH3COOH=CO2↑+H2O+CH3COO- +CH3COOH=CO2↑+H2O+CH3COO- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式不正确的是
A.向(NH4)2SO4溶液中加入小粒金属钠:2 +2Na=2Na++H2↑+2NH3↑ +2Na=2Na++H2↑+2NH3↑ |
B.Fe与稀硝酸按n(Fe):n(HNO3)=1:3反应:4Fe+3 +12H+=3Fe2++Fe3++3NO↑+6H2O +12H+=3Fe2++Fe3++3NO↑+6H2O |
C.用铜作电极电解硫酸铜溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.向溴水中滴加少量Na2SO3溶液中:Br2+H2O+ =2Br-+2H++ =2Br-+2H++ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氯化亚铜(CuCl)广泛应用于化工等行业,其难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺流程如图所示:
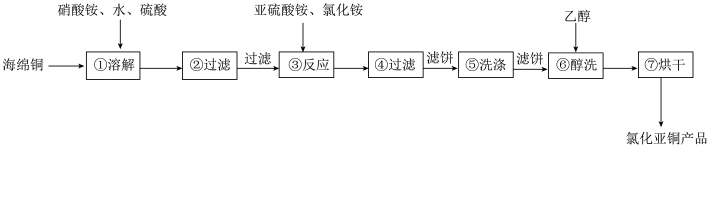
下列说法正确的是

下列说法正确的是
| A.步骤①,为加快海绵铜的溶解速度,可将其进行适当粉碎并用大火持续加热 |
| B.步骤③主要离子方程式:H2O+2Cu2++SO32-+2Cl-=CuCl↓+SO42-+2H+ |
| C.步骤⑤包括用pH=2的酸洗、水洗两步操作,为了防止CuCl被氧化,故不采用硝酸,而应采用硫酸或盐酸 |
| D.步骤⑥中醇洗主要目的是去除CuCl表面水分,但在步骤⑦中仍需要烘干,故节约成本可删除醇洗操作 |
您最近一年使用:0次
【推荐2】某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。下列说法不正确的是
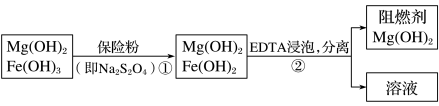

| A.步骤①中保险粉是作还原剂,步骤②中分离操作的名称是过滤 |
B.步骤①中的反应式:3Fe(OH)3+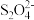 +2OH-=3Fe(OH)2+2 +2OH-=3Fe(OH)2+2 +4H2O +4H2O |
| C.Mg(OH)2可以作阻燃剂是因为它分解需要吸收大量的热 |
| D.从步骤②中可知OH-和EDTA共存时,Fe2+更易和EDTA结合,生成可溶性化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图所示,两套实验装置中进行的实验都涉及金属的腐蚀,假设其中的金属块和金属丝都是足量的。下列叙述正确的是
Ⅰ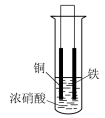 Ⅱ
Ⅱ 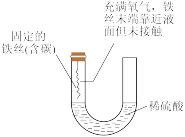
Ⅰ
 Ⅱ
Ⅱ 
| A.装置Ⅰ在反应过程中只生成NO2气体 |
| B.装置Ⅱ在开始阶段铁丝只发生析氢腐蚀 |
| C.装置Ⅱ在反应过程中能产生氢气 |
| D.装置Ⅰ在反应结束时溶液中的金属阳离子只有Cu2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向200mL稀硫酸和稀硝酸的混合溶液中缓慢加入铁粉,产生气体的体积随铁粉质量的变化如图所示

已知:①硝酸只被还原为NO气体;
②酸性条件下,氧化性: NO >Fe3+ >H+
>Fe3+ >H+
下列说法不正确的是

已知:①硝酸只被还原为NO气体;
②酸性条件下,氧化性: NO
 >Fe3+ >H+
>Fe3+ >H+下列说法不正确的是
| A.OA段产生的气体是NO, BC段产生的气体是H2 |
| B.B点溶液中的溶质为FeSO4和H2SO4 |
C.原混合溶液中SO 的物质的量为0.4mol 的物质的量为0.4mol |
D.原混合溶液中NO 的物质的量浓度为2 mol/L 的物质的量浓度为2 mol/L |
您最近一年使用:0次

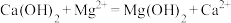
 溶液反应:
溶液反应:
 溶液中通入少量
溶液中通入少量 :
: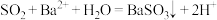
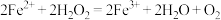
 和空气的混合气体通入
和空气的混合气体通入 和
和 的混合溶液中回收S,反应历程如图。下列说法正确的是
的混合溶液中回收S,反应历程如图。下列说法正确的是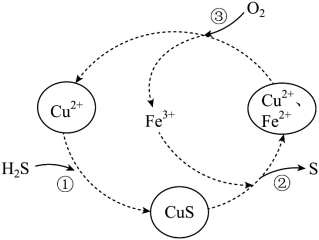
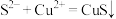
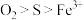
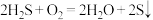
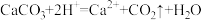
 中滴加
中滴加 至
至 沉淀完全:
沉淀完全: