研究氮及其化合物的性质,可以有效改善人类的生存环境。如图是氮元素的几种价态与物质类别的对应关系。回答下列问题:
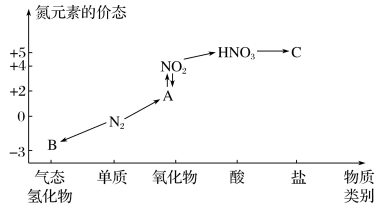
(1)写出氮气生成A的化学方程式:_______ 。
(2)物质B的电子式为_______ 。在催化剂和加热的条件下,由物质B生成物质A是工业制硝酸的重要反应,其化学方程式为_______ 。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。
(4)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。
(5)实验室中,检验溶液中含有 的操作方法是
的操作方法是_______ 。

(1)写出氮气生成A的化学方程式:
(2)物质B的电子式为
(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为(4)浓硝酸与木炭在加热条件下反应的化学方程式为
(5)实验室中,检验溶液中含有
 的操作方法是
的操作方法是
更新时间:2022-06-27 21:10:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是___________ 。
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是___________ 。
(4)CaC2是离子化合物,含有Ca2+和C 两种离子,其中C
两种离子,其中C 的电子式
的电子式___________ 。
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是
(4)CaC2是离子化合物,含有Ca2+和C
 两种离子,其中C
两种离子,其中C 的电子式
的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮的很多化合物都是重要的化工原料。
(1)羟胺( )可看成是氨分子内的一个氢原子被羟基取代的衍生物。
)可看成是氨分子内的一个氢原子被羟基取代的衍生物。 的电子式为
的电子式为___________ 。写出两种与羟胺的价电子数相同的双核分子的化学式___________ 。纯羟胺很不稳定,受热即分解为 、
、 和
和 ,则
,则 分解反应的化学方程式:
分解反应的化学方程式:___________ 。
(2)“肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(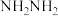 ),其反应历程如下所示。
),其反应历程如下所示。

下列说法正确的是___________ 。
a.反应涉及 、
、 键断裂和
键断裂和 键生成
键生成
b. 、
、 和
和 均为极性分子
均为极性分子
c.催化中心的 先被氧化为
先被氧化为 ,后又被还原为
,后又被还原为
若将 替换为
替换为 ,则表示该过程的化学方程式为:
,则表示该过程的化学方程式为:___________ (催化剂可用“ ”表示)。
”表示)。
(3)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________ 。联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为___________ (已知: 的
的 ;
; )。联氨与硫酸形成的酸式盐的化学式为
)。联氨与硫酸形成的酸式盐的化学式为___________ 。
(1)羟胺(
 )可看成是氨分子内的一个氢原子被羟基取代的衍生物。
)可看成是氨分子内的一个氢原子被羟基取代的衍生物。 的电子式为
的电子式为 、
、 和
和 ,则
,则 分解反应的化学方程式:
分解反应的化学方程式:(2)“肼合成酶”以其中的
 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(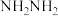 ),其反应历程如下所示。
),其反应历程如下所示。
下列说法正确的是
a.反应涉及
 、
、 键断裂和
键断裂和 键生成
键生成b.
 、
、 和
和 均为极性分子
均为极性分子c.催化中心的
 先被氧化为
先被氧化为 ,后又被还原为
,后又被还原为
若将
 替换为
替换为 ,则表示该过程的化学方程式为:
,则表示该过程的化学方程式为: ”表示)。
”表示)。(3)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
,无色液体)是一种应用广泛的化工原料,实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 的
的 ;
; )。联氨与硫酸形成的酸式盐的化学式为
)。联氨与硫酸形成的酸式盐的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空。
(1)电子式: O2:_______ CO2:_______ NH4Cl:_______ Mg(OH)2:_______
(2)用电子式写出K2S的形成过程_______ 。
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是_______ (填序号,下同),属于电解质的是_______ ,上述条件下能导电的是_______ 。
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是_______ (填序号,下同),互为同素异形体的一组是_______ 。
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成_______ 种不同的氯化氢分子,其对应的相对分子质量有_______ 种。
(1)电子式: O2:
(2)用电子式写出K2S的形成过程
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在盛有AgNO 3 、HBr、Na 2 CO 3 、CaCl 2 和Na I五种溶液的试剂瓶上标有①②③④⑤的标号。将它们两两混合,现象如下表所列,试推断各瓶所盛放的物质。
结论:①______ ,②______ ,③______ ,④______ ,⑤______ 。
| ① | ② | ③ | ④ | ⑤ | |
| ① | 无色气体 | 白色沉淀 | 白色沉淀 | 无明显现象 | |
| ② | 无色气体 | 无明显现象 | 浅黄色沉淀 | 无明显现象 | |
| ③ | 白色沉淀 | 无明显现象 | 白色沉淀 | 无明显现象 | |
| ④ | 白色沉淀 | 浅黄色沉淀 | 白色沉淀 | 黄色沉淀 | |
| ⑤ | 无明显现象 | 无明显现象 | 无明显现象 | 黄色沉淀 |
结论:①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。

回答下列问题:
(1)已知D可用于实验室制 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______ 。
(3)取 某84消毒液(有效成分
某84消毒液(有效成分 含量为
含量为 ),加水稀释,配制成
),加水稀释,配制成 稀溶液。
稀溶液。
①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、_______ 。
②关于配制过程的下列说法中,正确的是_______ (填字母)。
A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
B.未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C.定容时,俯视观察刻度线可能导致结果偏低
D.定容摇匀后,将溶液保存于容量瓶中,随用随取
③稀释后的溶液中, 的物质的量浓度为
的物质的量浓度为_______  。
。
(4)工业上“侯氏制碱法”以 、
、 、
、 及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:

①实验室分离出沉淀的操作名称是_______ ;煅烧炉里进行的化学反应方程式为:_______ 。
②检验产品 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有_______ 。

回答下列问题:
(1)已知D可用于实验室制
 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(3)取
 某84消毒液(有效成分
某84消毒液(有效成分 含量为
含量为 ),加水稀释,配制成
),加水稀释,配制成 稀溶液。
稀溶液。①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②关于配制过程的下列说法中,正确的是
A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
B.未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C.定容时,俯视观察刻度线可能导致结果偏低
D.定容摇匀后,将溶液保存于容量瓶中,随用随取
③稀释后的溶液中,
 的物质的量浓度为
的物质的量浓度为 。
。(4)工业上“侯氏制碱法”以
 、
、 、
、 及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
①实验室分离出沉淀的操作名称是
②检验产品
 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种易溶于水的白色固体,分别由 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A______ ;D______ 。
(2)写出下列反应的离子方程式:
①B+D→:______ ;
③C+HCl→气体:______ 。
(3)在作实验反思时,有同学提出:如果溶液中同时存在 和
和 ,
, 会对
会对 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在 ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断盐的化学式分别为:A
(2)写出下列反应的离子方程式:
①B+D→:
③C+HCl→气体:
(3)在作实验反思时,有同学提出:如果溶液中同时存在
 和
和 ,
, 会对
会对 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在 ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 向溶液中滴加过量的 溶液 溶液 | 除去 | 略 |
| 第二步 | 向第一步实验后的溶液中滴加 | 检验 | 略 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮的氧化物是主要的大气污染物,必须脱除才能排放。
(1)臭氧与空气中的氮氧化物和_______ (填字母)在紫外线照射下产生光化学烟雾。
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为_______ 。
(3)工业上在催化剂作用下用 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是_______ 。
(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为_______ 。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量_______ (填:“大于”、“小于”、“等于”) 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是_______ 。

(1)臭氧与空气中的氮氧化物和
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和
 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为(3)工业上在催化剂作用下用
 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用
 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收
 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究氮及其化合物的性质与转化,对降低含氮物质的污染有着重大意义。回答下列问题:
(1)实验室用氯化铵与氢氧化钙反应制备 ,反应的化学方程式为
,反应的化学方程式为_______ ,收集 应用向
应用向_______ (填“上”或“下”)排空气法。
(2)向干燥的蓝色石蕊试纸上滴加浓硝酸,预测可观察到的现象为_______ 。
(3)水体中过量氨氮(以 表示)会导致水体富营养化。用
表示)会导致水体富营养化。用 可将其氧化生成无污染的气体单质,除去
可将其氧化生成无污染的气体单质,除去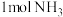 需消耗
需消耗 的物质的量为
的物质的量为_______ mol。
(4)用锌可去除酸性水体中的 以修复环境,反应初始时,
以修复环境,反应初始时, 转化为
转化为 ,此时反应的离子方程式为
,此时反应的离子方程式为_______ 。
(1)实验室用氯化铵与氢氧化钙反应制备
 ,反应的化学方程式为
,反应的化学方程式为 应用向
应用向(2)向干燥的蓝色石蕊试纸上滴加浓硝酸,预测可观察到的现象为
(3)水体中过量氨氮(以
 表示)会导致水体富营养化。用
表示)会导致水体富营养化。用 可将其氧化生成无污染的气体单质,除去
可将其氧化生成无污染的气体单质,除去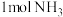 需消耗
需消耗 的物质的量为
的物质的量为(4)用锌可去除酸性水体中的
 以修复环境,反应初始时,
以修复环境,反应初始时, 转化为
转化为 ,此时反应的离子方程式为
,此时反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮和氮的化合物与人类有密切关系。
(1)下列属于氮的固定的是_______ (填序号)。
①工业上N2和H2合成NH3
②N2和O2放电条件下生成NO
③NH3催化氧化生成NO
写出反应③的化学方程式_______ 。
(2)①治理NO污染通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用于氧化NO的是_______ (填序号)。
ANaCl溶液 B. K2Cr2O7溶液 C. Na2CO3溶液 D. KMnO4溶液
②NO也可用NaClO碱性溶液氧化并将其转化为硝酸盐化肥,写出该反应的离子方程式:_______ 。
③目前处理柴油车尾气中NOx和PM2.5等的方法之一,是用车用尿素[CO(NH2)2]溶液在选择性催化还原系统中将NOx无害化处理,写出该系统无害化处理NO的化学方程式:_______ 。
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应,用Rh做催化剂时该反应的过程示意图如下:
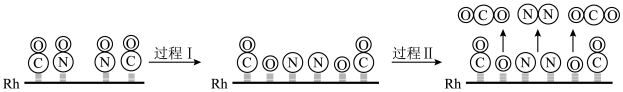
①过程I为_______ 过程(填“吸热”或“放热”)。该反应中氧化产物为_______ ,当生成1molN2时,转移电子_______ mol。
②已知过程I的焓变(lmolCO参加)为akJ/mol,过程II的焓变为bkJ/mol,则该反应的热化学方程式为_______ 。
(1)下列属于氮的固定的是
①工业上N2和H2合成NH3
②N2和O2放电条件下生成NO
③NH3催化氧化生成NO
写出反应③的化学方程式
(2)①治理NO污染通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用于氧化NO的是
ANaCl溶液 B. K2Cr2O7溶液 C. Na2CO3溶液 D. KMnO4溶液
②NO也可用NaClO碱性溶液氧化并将其转化为硝酸盐化肥,写出该反应的离子方程式:
③目前处理柴油车尾气中NOx和PM2.5等的方法之一,是用车用尿素[CO(NH2)2]溶液在选择性催化还原系统中将NOx无害化处理,写出该系统无害化处理NO的化学方程式:
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应,用Rh做催化剂时该反应的过程示意图如下:

①过程I为
②已知过程I的焓变(lmolCO参加)为akJ/mol,过程II的焓变为bkJ/mol,则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】64gCu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗的HNO3的物质的量是__ (填字母代号)。
A.0.5mol B.1.0mol C.2.0mol D.3.0mol
产生的气体分别是__ ,其物质的量之比是__ 。
A.0.5mol B.1.0mol C.2.0mol D.3.0mol
产生的气体分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.(1)在100 mL 0.8mol/L硝酸溶液中加入足量铜粉,则被溶解的铜的质量为_______ g。
(2)在上述溶液中再加入足量稀硫酸,又有_______ g铜溶解。
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显_________ (酸、碱、中)性,原因是(用离子方程式表示)____________________________________ ,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH_____ 7 (填“>”、“<”或“=”).
(2)氨水显碱性的原因(用离子方程式表示)______________________ ,向氨水中加入NH4Cl固体,氨水的电离程度________ (填“增大”、“减小”或“不变”),溶液的pH将________ (填“增大”、“减小”或“不变”).
(2)在上述溶液中再加入足量稀硫酸,又有
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显
(2)氨水显碱性的原因(用离子方程式表示)
您最近一年使用:0次
【推荐3】I.储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。请回答下列问题:
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目___________ 。
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是___________ ,被氧化的元素是___________ (填元素符号) 。
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
(4)请配平下列离子方程式___________ 。
___________Fe2++___________H++___________ =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2O
II.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是___________ (填序号,下同)。
(6)可能是HNO2还原产物的是___________ 。
(7)不可能是N2的氧化产物是___________ 。
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
| A.酸性 | B.氧化性 | C.氧化性和酸性 | D.还原性和酸性 |
___________Fe2++___________H++___________
 =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2OII.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是
(6)可能是HNO2还原产物的是
(7)不可能是N2的氧化产物是
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次



