早在1914年就有人发现,引入有机基团可降低离子化合物的熔点,如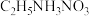 的熔点只有12℃,比
的熔点只有12℃,比 的熔点170℃低了很多。到20世纪90年代,人们把室温或稍高于室温时呈液态的离子化合物定义为离子液体。大多数离子液体含有体积很大的阴、阳离子(如下图所示)。
的熔点170℃低了很多。到20世纪90年代,人们把室温或稍高于室温时呈液态的离子化合物定义为离子液体。大多数离子液体含有体积很大的阴、阳离子(如下图所示)。
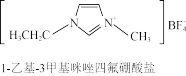
(1)1-乙基-3甲基咪唑四氟硼酸盐中涉及的元素除氢元素外,其余元素均位于元素周期表的___________ 区,基态F原子核外电子的运动状态有___________ 种。
(2) 极易溶于水且水溶液呈碱性的原因与氢键有关,用“…”表示氢键,结合
极易溶于水且水溶液呈碱性的原因与氢键有关,用“…”表示氢键,结合 的电离推测
的电离推测 可能的结构式为
可能的结构式为___________ 。
(3)硅元素与碳元素同主族,硅元素和卤素单质反应可以得到 。
。
 的熔沸点如下表所示
的熔沸点如下表所示
20℃时, 、
、 、
、 、
、 呈液态的是
呈液态的是___________ (填化学式),熔沸点依次升高的原因是___________ 。
(4)下列有关该离子液体说法正确的是___________。
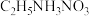 的熔点只有12℃,比
的熔点只有12℃,比 的熔点170℃低了很多。到20世纪90年代,人们把室温或稍高于室温时呈液态的离子化合物定义为离子液体。大多数离子液体含有体积很大的阴、阳离子(如下图所示)。
的熔点170℃低了很多。到20世纪90年代,人们把室温或稍高于室温时呈液态的离子化合物定义为离子液体。大多数离子液体含有体积很大的阴、阳离子(如下图所示)。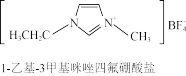
(1)1-乙基-3甲基咪唑四氟硼酸盐中涉及的元素除氢元素外,其余元素均位于元素周期表的
(2)
 极易溶于水且水溶液呈碱性的原因与氢键有关,用“…”表示氢键,结合
极易溶于水且水溶液呈碱性的原因与氢键有关,用“…”表示氢键,结合 的电离推测
的电离推测 可能的结构式为
可能的结构式为(3)硅元素与碳元素同主族,硅元素和卤素单质反应可以得到
 。
。 的熔沸点如下表所示
的熔沸点如下表所示 |  |  |  | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
 、
、 、
、 、
、 呈液态的是
呈液态的是(4)下列有关该离子液体说法正确的是___________。
A.该离子液体的阳离子中C原子和N原子的杂化轨道类型均为 、 、 |
B.离子液体中C、N、H三种元素的电负性由大到小的顺序为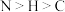 |
| C.该离子液体的熔沸点低于氯化钠晶体,是因为阴阳离子体积较大,使得阴阳离子间距离较大,离子键较弱 |
| D.离子液体中微粒间作用力较大,一般比有机溶剂难挥发,是很好的“绿色”溶剂 |
更新时间:2022-07-04 16:52:23
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是nsnnpn+1;C的p能级上未成对的电子比B少一个;D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A的单质能生成具有刺激性气味的气体,该气体极易溶于水。)
(1)B原子核外电子排布式为___________ 。
(2)A与E化合时原子间以___________ 键相结合,D与C化合时原子间以___________ 键相结合。
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:___________ 。
(4)A与B形成化合物时,中心原子采取___________ 杂化成键,其立体结构为___________ ,属于___________ (填“极性”或“非极性”)分子。
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:___________ 。
(6)五种元素中电负性最大的是___________ (填元素名称)。
(1)B原子核外电子排布式为
(2)A与E化合时原子间以
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:
(4)A与B形成化合物时,中心原子采取
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:
(6)五种元素中电负性最大的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】三醋酸锰[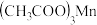 ]是一种很好的有机反应氧化剂,可用如下反应制备:
]是一种很好的有机反应氧化剂,可用如下反应制备: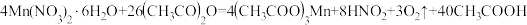 。请回答下列问题:
。请回答下列问题:
(1)三醋酸锰[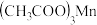 ]中阳离子的价层电子排布式为
]中阳离子的价层电子排布式为_______ ,该价层电子排布式中电子的自旋状态_______ (填“相同”或“相反”)。
(2)过渡元素锰能形成很多重要的配合物。三醋酸锰就是一种配合物,其结构如图所示,其中配位键数为_______ 。

(3)Mn2+能形成配离子为八面体的配合物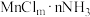 ,在该配合物的配离子中,Mn2+位于八面体的中心。若含1mol该配合物的溶液与足量
,在该配合物的配离子中,Mn2+位于八面体的中心。若含1mol该配合物的溶液与足量 溶液作用可生成
溶液作用可生成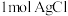 沉淀,则化学式中的n为
沉淀,则化学式中的n为_______ 。
(4) 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(5) 的立体构型是
的立体构型是_____ ,醋酸酐[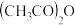 ]中所含σ键数与π键数之比为
]中所含σ键数与π键数之比为____ 。
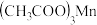 ]是一种很好的有机反应氧化剂,可用如下反应制备:
]是一种很好的有机反应氧化剂,可用如下反应制备: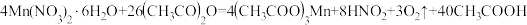 。请回答下列问题:
。请回答下列问题:(1)三醋酸锰[
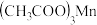 ]中阳离子的价层电子排布式为
]中阳离子的价层电子排布式为(2)过渡元素锰能形成很多重要的配合物。三醋酸锰就是一种配合物,其结构如图所示,其中配位键数为

(3)Mn2+能形成配离子为八面体的配合物
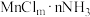 ,在该配合物的配离子中,Mn2+位于八面体的中心。若含1mol该配合物的溶液与足量
,在该配合物的配离子中,Mn2+位于八面体的中心。若含1mol该配合物的溶液与足量 溶液作用可生成
溶液作用可生成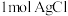 沉淀,则化学式中的n为
沉淀,则化学式中的n为(4)
 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为(5)
 的立体构型是
的立体构型是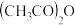 ]中所含σ键数与π键数之比为
]中所含σ键数与π键数之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜可以形成许多结构和性质特殊的化合物或合金。回答下列问题:
(1)基态铜原子价电子的轨道表示式为___________ ;同周期中与铜原子未成对电子数相同的元素有___________ 种。
(2)含H2O2的稀硫酸溶解铜可得到CuSO4溶液,通入氨气先形成蓝色沉淀然后溶解得到深蓝色 溶液。
溶液。
①H、N、O、S四种元素的电负性由大到小的顺序为___________ ;其中第一电离能最大的为___________ (填元素名称)。
②液态NH3与液态H2O2中存在的分子间作用力类型___________ (填“完全相同”或“部分相同”);NH3分子中 小于
小于 中的
中的 的原因为
的原因为___________ 。
③ 溶液中Cu2+的存在形式为
溶液中Cu2+的存在形式为 ,则铜的杂化方式可能为
,则铜的杂化方式可能为___________ (填标号)。
A. B.
B. C.
C. D.
D.
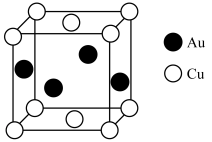
(3)已知: 为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为
为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为___________ g·cm-3(用含a、 的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为___________ 。
(1)基态铜原子价电子的轨道表示式为
(2)含H2O2的稀硫酸溶解铜可得到CuSO4溶液,通入氨气先形成蓝色沉淀然后溶解得到深蓝色
 溶液。
溶液。①H、N、O、S四种元素的电负性由大到小的顺序为
②液态NH3与液态H2O2中存在的分子间作用力类型
 小于
小于 中的
中的 的原因为
的原因为③
 溶液中Cu2+的存在形式为
溶液中Cu2+的存在形式为 ,则铜的杂化方式可能为
,则铜的杂化方式可能为A.
 B.
B. C.
C. D.
D.
(3)已知:
 为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为
为阿伏加德罗常数的值。铜与金(Au)可形成一种具有有序结构的储氢合金,其晶胞采取面心立方最密堆积方式,结构如图所示,该晶胞参数为anm。该合金晶胞密度为 的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
的式子表示,列出计算式即可);晶胞中铜原子与金原子以原子数之比为1:1可以形成四面体,四面体空隙中填充氢原子后化学式为H4CuAu,则四面体空隙的填充率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】化合物M的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q核外最外层电子数与Y核外电子总数相同,X是元素周期表中原子半径最小的原子。

(1)M的化学键类型有______ ,其阴离子结构简式为______ ,Y的杂化方式为______ 。
(2)Y、Z、Q第一电离能大到小的顺序是______ (用元素符号填空)。
(3)由X、Z形成ZX3分子的空间构型是______ 。
(4)基态Z原子价电子排布图为______ 。
(5)X2Z-ZX2分子中孤电子对与σ键的数目之比为______ ,其相对分子质量与Y2X4分子接近,但沸点远高于Y2X4的原因是______ 。

(1)M的化学键类型有
(2)Y、Z、Q第一电离能大到小的顺序是
(3)由X、Z形成ZX3分子的空间构型是
(4)基态Z原子价电子排布图为
(5)X2Z-ZX2分子中孤电子对与σ键的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)基态N原子的价电子的轨道表示式为___________ , 是
是___________ (填“极性分子”或“非极性分子”)。
(2)N及其同族的P、As均可形成类似的氢化物,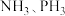 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ (填化学式)。
(3)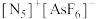 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为___________ 。
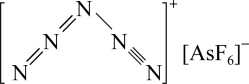
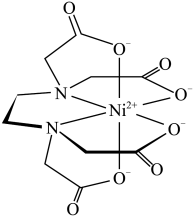
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有___________ 个,其中提供孤对电子的原子为O、___________ (写元素符号)。
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为___________ 。
②已知晶胞参数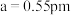 ,则该晶体的密度为
,则该晶体的密度为___________  (用
(用 表示阿伏加德罗常数的值,只列出计算表达式即可。)
表示阿伏加德罗常数的值,只列出计算表达式即可。)
(1)基态N原子的价电子的轨道表示式为
 是
是(2)N及其同族的P、As均可形成类似的氢化物,
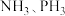 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)
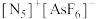 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为②已知晶胞参数
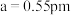 ,则该晶体的密度为
,则该晶体的密度为 (用
(用 表示阿伏加德罗常数的值,只列出计算表达式即可。)
表示阿伏加德罗常数的值,只列出计算表达式即可。)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
【推荐3】[选修3—物质结构与性质( )
Ⅰ下列物质的结构或性质与氢键无关的是
Ⅱ钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为_________ ,其价层电子排布图为______________ 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为____ 、 _____ 。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是__ 对,分子的立体构型为___ ;SO3气态为单分子,该分子中S原子的杂化轨道类型为__ ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为__ ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为__ (填图2中字母),该分子中含有_______ 个σ键。

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为___ ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为___ 。
Ⅰ下列物质的结构或性质与氢键无关的是
| A.乙醚的沸点 | B.乙醇在水中的溶解度 |
| C.氢化镁的晶格能 | D.DNA的双螺旋结构 |
回答下列问题:
(1)钒在元素周期表中的位置为
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。

(1)TiX4熔点变化趋势的原因_______ 。
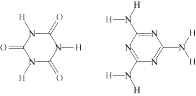
(2)多重氢键在生命体、分子自组装和响应型功能材料领域都有重要应用。三聚氰酸和三聚氰胺(1∶1)可以通过多重氢键自组装构成二维片状结构,被形象地称为“分子饼”。请用虚线在下图中直接画出两个分子间存在的氢键_______ 。

(1)TiX4熔点变化趋势的原因
(2)多重氢键在生命体、分子自组装和响应型功能材料领域都有重要应用。三聚氰酸和三聚氰胺(1∶1)可以通过多重氢键自组装构成二维片状结构,被形象地称为“分子饼”。请用虚线在下图中直接画出两个分子间存在的氢键

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】镧(La)、镍(Ni)是生产新型储氢材料的原料。HC≡N、CH3CH(OH)COONH4是重要的无机、有机含氮化合物。回答下列问题:
(1)基态镍原子的未成对电子与三价铁离子未成对电子数之比为____ 。
(2)基态氮原子比基态氧原子第一电离能大的原因是_____ 。
(3)与HC≡N电子数相等的有机分子的结构简式为______ 。
(4)CH3CH(OH)COONH4,中具有相同杂化轨道的碳原子、氮原子的个数比为____ 。
(5)四羰基镍、氧化镍的物理性质如下:
由此判断:[Ni(CO)4]是配合物,其配位体是____ 。[Ni(CO)4]分子是____ 分子(填“极性”或“非极性”)。[Ni(CO)4]比NiO熔点低的原因是____ 。
(6)有一种镧镍合金是重要的储氢材料,其晶体属六方晶系,晶胞结构如图1所示。其储氢原理是氢分子先变为氢原子,氢原子进入合金的孔隙中。图2所示晶体中两个镧原子和2个镍原子组成的四面体孔隙中只能进入1个氢原子,晶胞中的所有类似四面体中都有氢原子进入,即达到储氢稳定状态。当需要氢气时,给储氢合金加热,氢原子变为氢气逸出。

晶体中Ni、La的原子个数比=__ 。每升该储氢材料达到储氢稳定状态,储氢原子__ mol。
(1)基态镍原子的未成对电子与三价铁离子未成对电子数之比为
(2)基态氮原子比基态氧原子第一电离能大的原因是
(3)与HC≡N电子数相等的有机分子的结构简式为
(4)CH3CH(OH)COONH4,中具有相同杂化轨道的碳原子、氮原子的个数比为
(5)四羰基镍、氧化镍的物理性质如下:
| 名称(化学式) | 状态 | 熔点 | 溶解性 | 说明 |
| 四羰基镍 [Ni(CO)4] | 无色挥发性剧毒液体 | -25℃ | 不溶于水,易溶于苯、四氯化碳等有机溶剂 | 正四面体分子、分子中碳原子与镍成键 |
| 氧化镍(NiO) | 绿色粉末状固体 | 1980℃ | 不溶于水 | 阴离子、阳离子构成 |
(6)有一种镧镍合金是重要的储氢材料,其晶体属六方晶系,晶胞结构如图1所示。其储氢原理是氢分子先变为氢原子,氢原子进入合金的孔隙中。图2所示晶体中两个镧原子和2个镍原子组成的四面体孔隙中只能进入1个氢原子,晶胞中的所有类似四面体中都有氢原子进入,即达到储氢稳定状态。当需要氢气时,给储氢合金加热,氢原子变为氢气逸出。

晶体中Ni、La的原子个数比=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为_________ ,C、N、O三种元素的第一电离能由大到小的顺序为_________ 。
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2−, 1 mol CN−中含有的π键的数目为_________ 。与CN−互为等电子体的分子有_______ (写出一种即可)。
(3)在络离子[Cu(NH3)4] 2+中 NH3 的 VSEPR 模型为____________ ,其中N原子的杂化轨道类型为_________ 。
(4)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_______________________ 。
(5)晶体是由无数晶胞___________ 而成。铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为______ ,若该晶胞的晶胞参数为d nm,则该合金的密度为______ g/cm3 (不必化简,用NA表示阿伏加德罗常数)。

(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2−, 1 mol CN−中含有的π键的数目为
(3)在络离子[Cu(NH3)4] 2+中 NH3 的 VSEPR 模型为
(4)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是
(5)晶体是由无数晶胞

您最近一年使用:0次



