二甲醚(CH3OCH3)气体是一种可再生绿色新能源,被誉为“21 世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:___________ 。
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式___________ 。
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=___________ mol/(L·min )。
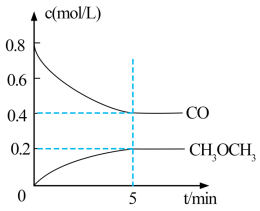
②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是___________ 。
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示
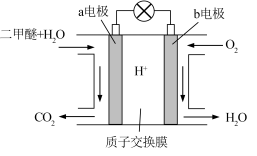
①该电池的负极是___________ (填“a 电极”或“b 电极”)
②H+通过质子交换膜时的移动方向是___________ 。(填选项字母)
A.从左向右 B.从右向左
③通入O2的电极反应式是___________ 。
(5)标况下每转移6mol电子需要氧气多少L______ ?(写出解题过程)
(1)写出二甲醚一种同分异构体的结构简式:
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=

②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示

①该电池的负极是
②H+通过质子交换膜时的移动方向是
A.从左向右 B.从右向左
③通入O2的电极反应式是
(5)标况下每转移6mol电子需要氧气多少L
更新时间:2022-06-22 09:33:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)过氧化钠(Na2O2)是常见的供氧剂,是航空航天和潜水常用呼吸面具的主要成分,请写出过氧化钠的电子式:___ 。
(2)1g甲烷气体完全燃烧生成液态水时放56kJ的热量,请写出甲烷完全燃烧的热化学方程式:___ 。
(3)取久置硫酸酸化的硫酸亚铁溶液加入KSCN溶液,溶液显血红色,请用离子方程式解释原因①:___ ;②Fe3++3SCN-=Fe(SCN)3。
(4)酸性:H2SO4<HClO4,HClO4的沸点为90℃,已知能发生H2SO4(浓)+NaClO4 HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:___ 。
(2)1g甲烷气体完全燃烧生成液态水时放56kJ的热量,请写出甲烷完全燃烧的热化学方程式:
(3)取久置硫酸酸化的硫酸亚铁溶液加入KSCN溶液,溶液显血红色,请用离子方程式解释原因①:
(4)酸性:H2SO4<HClO4,HClO4的沸点为90℃,已知能发生H2SO4(浓)+NaClO4
 HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】研究化学反应时,既要关注物质变化,又要关注能量变化。请回答以下问题:
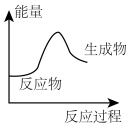
(1)下列反应中能量变化与如图一致的是___________(填字母)。
(2)如图是1mol  (g)和1mol CO(g)反应生成1mol
(g)和1mol CO(g)反应生成1mol  (g)和1mol NO(g)过程中能量变化示意图。
(g)和1mol NO(g)过程中能量变化示意图。
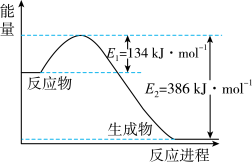
①该反应是___________ (填“吸热”或“放热”)反应。
②请写出该反应的热化学方程式:___________ 。
③若在该反应体系中加入催化剂,则对反应热___________ (填“有”或“没有”)影响。
(3)化学反应的焓变与反应物和生成物的键能有关。
已知:
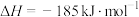
则H-Cl的键能为___________  。
。
(4)实验小组设计用盐酸与氢氧化钠溶液在如图装置中进行中和反应。图中仪器A的作用是___________ ;碎泡沫塑料的作用是___________ 。
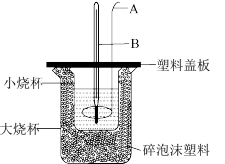
(1)下列反应中能量变化与如图一致的是___________(填字母)。

| A.甲烷燃烧 | B.生石灰与水反应 |
| C.镁与稀硫酸的反应 | D.氢氧化钡晶体和氯化铵晶体反应 |
 (g)和1mol CO(g)反应生成1mol
(g)和1mol CO(g)反应生成1mol  (g)和1mol NO(g)过程中能量变化示意图。
(g)和1mol NO(g)过程中能量变化示意图。
①该反应是
②请写出该反应的热化学方程式:
③若在该反应体系中加入催化剂,则对反应热
(3)化学反应的焓变与反应物和生成物的键能有关。
已知:

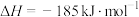
| 共价键 | H-H | Cl-Cl |
键能/( ) ) | 436 | 247 |
 。
。(4)实验小组设计用盐酸与氢氧化钠溶液在如图装置中进行中和反应。图中仪器A的作用是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物对我们的生产、生活有重要的影响。回答下列问题:
(1)机动车发动机工作时会引发 与
与 的反应,该反应是吸热反应,
的反应,该反应是吸热反应, 与
与 的总能量比2molNO的总能量
的总能量比2molNO的总能量___________ (填“高”或“低”)。
(2)已知:
 ,
,
 。下列能量变化示意图中,正确的是___________(填字母)。
。下列能量变化示意图中,正确的是___________(填字母)。
(3) 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
根据上述数据分析最稳定的物质是___________ (填“ ”“
”“ ”或“
”或“ ”),写出
”),写出 和
和 生成
生成 的热化学方程式:
的热化学方程式:___________ 。
(4)火箭的常规燃料是液态四氧化二氮和液态肼( ),
), 作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:①
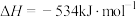
②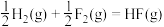
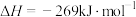
③
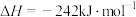
请写出肼和氟气反应的热化学方程式:___________ 。
(1)机动车发动机工作时会引发
 与
与 的反应,该反应是吸热反应,
的反应,该反应是吸热反应, 与
与 的总能量比2molNO的总能量
的总能量比2molNO的总能量(2)已知:

 ,
,
 。下列能量变化示意图中,正确的是___________(填字母)。
。下列能量变化示意图中,正确的是___________(填字母)。A.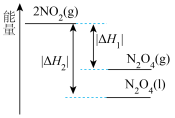 | B.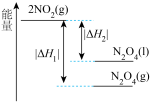 |
C.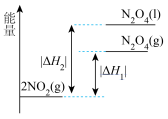 | D.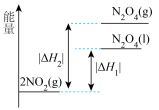 |
 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:| 化学键 |  |  |  |
能量 | 946 | 154.8 | 283 |
 ”“
”“ ”或“
”或“ ”),写出
”),写出 和
和 生成
生成 的热化学方程式:
的热化学方程式:(4)火箭的常规燃料是液态四氧化二氮和液态肼(
 ),
), 作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:①

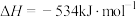
②
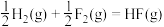
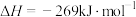
③

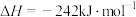
请写出肼和氟气反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.臭氧( )在水中易分解,一定条件下,
)在水中易分解,一定条件下, 的浓度减少一半所需的时间(
的浓度减少一半所需的时间( )如下表所示。
)如下表所示。
已知: 的起始浓度为0.0216
的起始浓度为0.0216  。
。
(1)pH增大能加速 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是___________ 。
(2)在30℃、pH=4.0条件下, 的分解速率为
的分解速率为___________  。
。
(3)据表中的递变规律,推测 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为___________ (填字母)。
a.40℃、pH=3.0 b.10℃、pH=4.0 c.30℃、pH=7.0
Ⅱ.一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应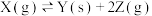
 ,反应达到最大限度前,测得X的浓度与反应时间的数据如表所示:
,反应达到最大限度前,测得X的浓度与反应时间的数据如表所示:
试回答下列问题:
(4)0~3min内,用Z表示的平均反应速率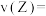
___________ 。
(5)分析该反应中反应物的浓度随时间的变化规律,得出的结论是___________ 。由此结论推出 为
为___________ 。
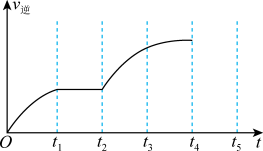
(6)该反应的逆反应速率随时间变化的关系如图所示, 时改变了某一反应条件,则改变的条件为
时改变了某一反应条件,则改变的条件为___________ 。
 )在水中易分解,一定条件下,
)在水中易分解,一定条件下, 的浓度减少一半所需的时间(
的浓度减少一半所需的时间( )如下表所示。
)如下表所示。已知:
 的起始浓度为0.0216
的起始浓度为0.0216  。
。| pH | 3.0 | 4.0 | 5.0 | 6.0 |
 /min /min | ||||
 /℃ /℃ | ||||
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是(2)在30℃、pH=4.0条件下,
 的分解速率为
的分解速率为 。
。(3)据表中的递变规律,推测
 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为a.40℃、pH=3.0 b.10℃、pH=4.0 c.30℃、pH=7.0
Ⅱ.一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应
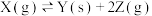
 ,反应达到最大限度前,测得X的浓度与反应时间的数据如表所示:
,反应达到最大限度前,测得X的浓度与反应时间的数据如表所示:反应时间 /min /min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
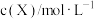 | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 |  | 0.0375 |
(4)0~3min内,用Z表示的平均反应速率
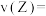
(5)分析该反应中反应物的浓度随时间的变化规律,得出的结论是
 为
为(6)该反应的逆反应速率随时间变化的关系如图所示,
 时改变了某一反应条件,则改变的条件为
时改变了某一反应条件,则改变的条件为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据有关信息完成以下四个小题:【(1)、(2) 填编号】
(1)有以下各组微粒或物质:
其中互为同分异构体的有______ ;互为同素异形体的有________ 。
(2)现有①干冰 ②金刚石 ③NH4Cl ④Na2S四种物质,按下列要求回答(填序号):
熔化时不需要破坏化学键的是____________ ;既存在离子键又存在共价键的是________ 。
(3)向一个容积为2 L的密闭容器中充入7 mol SO2和4 mol O2,在一定温度和压强下,发生如下反应:2SO2(g)+O2(g)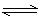 2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则O2的平均反应速率为
2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则O2的平均反应速率为__________ mol/(L·s)。
(4)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为_______________________________________ 。
(1)有以下各组微粒或物质:
| A.正丁烷和异丁烷 | B.金刚石、石墨和C60 |
| C.冰和干冰 | D.35Cl和37Cl |
| E.NO和NO2; |
其中互为同分异构体的有
(2)现有①干冰 ②金刚石 ③NH4Cl ④Na2S四种物质,按下列要求回答(填序号):
熔化时不需要破坏化学键的是
(3)向一个容积为2 L的密闭容器中充入7 mol SO2和4 mol O2,在一定温度和压强下,发生如下反应:2SO2(g)+O2(g)
 2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则O2的平均反应速率为
2SO3(g),经4 s后达到平衡状态,测得SO2的物质的量是3 mol,则O2的平均反应速率为(4)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
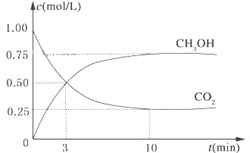
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=______ mol/(L•min);
(2)氢气的转化率=______ ;
(3)该反应的平衡常数为______ (保留小数点后2位);
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是______ 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1______ c2的关系(填“>”、“<”或“=”)
 CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)氢气的转化率=
(3)该反应的平衡常数为
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)氨的催化氧化反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①反应在第lmin到第2min时,NH3的平均反应速率为_____ 。
②反应在第3min时改变了条件,改变的条件可能是_____ (填序号)。
A.使用催化剂 B.减小压强 C.升高温度 D.增加O2的浓度
③说明4NH3(g)+5O2(g) 4NO(g)+6H2O(g)达到平衡状态的是
4NO(g)+6H2O(g)达到平衡状态的是_____ (填序号)。
A.单位时间内生成nmolNO的同时生成nmolNH3
B.百分含量w(NH3)=w(NO)
C.反应速率v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6
D.在恒温恒容的容器中,混合气体的平均相对分子质量不再变化
(2)图是某燃料电池的结构示意图,电解质为硫酸溶液。回答下列问题。

①若使用甲烷为燃料,则a极的电极反应式为_____ 。
②若使用氢气为燃料,电解质溶液换成NaOH溶液,去掉质子交换膜。a极的电极反应式为_____ 。每转移1mol电子,消耗H2的体积为_____ L。(标准状况下)。
(1)氨的催化氧化反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:| c(NH3)mol/L | c(O2)mol/L | c(NO)mol/L | |
| 第0min | 0.8 | 1.6 | 0 |
| 第1min | a | 1.35 | 0.2 |
| 第2min | 0.3 | 0.975 | 0.5 |
| 第3min | 0.3 | 0.975 | 0.5 |
| 第4min | 0.7 | 1.475 | 0.1 |
②反应在第3min时改变了条件,改变的条件可能是
A.使用催化剂 B.减小压强 C.升高温度 D.增加O2的浓度
③说明4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)达到平衡状态的是
4NO(g)+6H2O(g)达到平衡状态的是A.单位时间内生成nmolNO的同时生成nmolNH3
B.百分含量w(NH3)=w(NO)
C.反应速率v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6
D.在恒温恒容的容器中,混合气体的平均相对分子质量不再变化
(2)图是某燃料电池的结构示意图,电解质为硫酸溶液。回答下列问题。

①若使用甲烷为燃料,则a极的电极反应式为
②若使用氢气为燃料,电解质溶液换成NaOH溶液,去掉质子交换膜。a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业制硫酸在接触室中发生的主要反应为2SO2(g)+O2(g) 2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:
2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:
(1)用SO3表示从0~2s内该反应的平均速率v(SO3)=___ 。
(2)该反应达到最大限度时SO2的转化率为___ 。
(提示:转化率=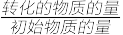 ×100%)
×100%)
(3)该反应达到最大限度时O2的浓度为___ 。
(4)下列叙述能说明上述反应达到平衡状态的是___ 。
A.容器内压强保持不变
B.v(SO2)=2v(O2)
C.SO3的浓度不再变化
D.SO2、O2、SO3为浓度之比为2∶1∶2
E.单位时间内每消耗2molSO2,同时生成2molSO3
 2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:
2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(SO2)(mol) | 4 | 3.2 | 1.6 | 1.4 | 1.4 |
(1)用SO3表示从0~2s内该反应的平均速率v(SO3)=
(2)该反应达到最大限度时SO2的转化率为
(提示:转化率=
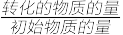 ×100%)
×100%)(3)该反应达到最大限度时O2的浓度为
(4)下列叙述能说明上述反应达到平衡状态的是
A.容器内压强保持不变
B.v(SO2)=2v(O2)
C.SO3的浓度不再变化
D.SO2、O2、SO3为浓度之比为2∶1∶2
E.单位时间内每消耗2molSO2,同时生成2molSO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。

(1)从3 min到9 min,υ(H2)=________ ;
(2)能说明上述反应达到平衡状态的是____________ (填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________ 。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________ 。
(5)一定温度下,第9分钟时υ逆(CH3OH)_______ (填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
(1)从3 min到9 min,υ(H2)=
(2)能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为
(4)平衡时混合气体中CH3OH(g)的体积分数是
(5)一定温度下,第9分钟时υ逆(CH3OH)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】肼(N2H4)﹣空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼﹣空气燃料电池放电时:负极的电极反应式:________ ,正极的电极反应式:________
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电能是现代社会应用最广泛的能源之一、某原电池装置如图所示。其中,
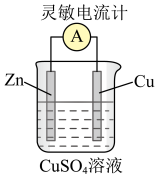
(1)Zn电极为原电池的___________ 极 (填“正” 或“负”)
(2)Cu电极上发生的电极反应式是___________ 。
(3)能证明产生电能的实验现象是___________ 。
(4)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是___________ (填序号)。
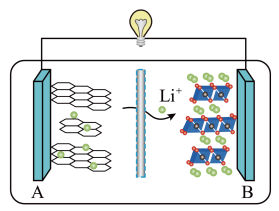
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动

(1)Zn电极为原电池的
(2)Cu电极上发生的电极反应式是
(3)能证明产生电能的实验现象是
(4)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是

①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示: 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是______ kJ。
(2)下列化学反应在理论上可以设计成原电池的是______。
(3)下图是某兴趣小组设计的原电池示意图:_____________ 。
②将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是______ (填“锌极”或“铜极”,下同),溶液中 移向
移向______ 。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示:
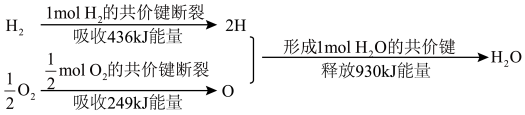
 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是(2)下列化学反应在理论上可以设计成原电池的是______。
A.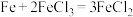 | B. |
C.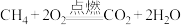 | D.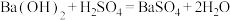 |
(3)下图是某兴趣小组设计的原电池示意图:
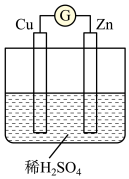
②将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是 移向
移向
您最近一年使用:0次



