已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器。)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 溶解 | 将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解。 |
| ② | ||
| ③ | ||
| ④ | ||
| ⑤ | 洗涤沉淀 | |
| ⑥ | 检验沉淀 是否洗净 |
12-13高一·全国·课时练习 查看更多[7]
(已下线)2012年沪科版高中化学10.2结晶水合物中结晶水含量的测练习卷(已下线)2012年苏教版高中化学选修6 1.1海带中碘元素的分离及检验练习卷(已下线)2012-2013学年江苏省江都市甘棠中学高二下学期期末考试化学试卷(已下线)2012-2013学年江苏省郑梁梅中学高二下学期期末考试化学试卷黑龙江省哈尔滨市第三中学2017-2018学年高一上学期第一次验收考试化学试题化学沪科版化学高二上:10.2《结晶水合物中结晶水含量的测定》测试(已下线)1.3.2 过滤、结晶、蒸馏-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
更新时间:2016-12-09 04:26:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)FeCl3 溶液和 Fe(OH)3 胶体的本质区别是:_____________ 。
(2)工业上制玻璃的原料有纯碱、石英和_____________ (填名称)。
(3)工业上金属钠可用来制备钛等金属,利用了金属钠的____________ 性。
(4)盛放 NaOH 溶液的玻璃试剂瓶应选用____________ 塞(填“玻璃”或“橡胶”)。
(5)用四氯化碳萃取溴水后,分液时有机层从分液漏斗的_____________ (填“下口放出”或“上口倒出”)。
(6)6.20 g Na2O 晶体中含离子数目是_____________ (NA为阿伏伽德罗常数的数值)。
(7)等质量的 NH3 和 H2S 中,氢原子的个数比是_________ 。
(8)加热某碱式碳酸镁晶体[4MgCO3∙Mg(OH)2∙5H2O]至质量不再变化时,得到 10.0g 残留固体和__________ L CO2(标准状况下)。
(1)FeCl3 溶液和 Fe(OH)3 胶体的本质区别是:
(2)工业上制玻璃的原料有纯碱、石英和
(3)工业上金属钠可用来制备钛等金属,利用了金属钠的
(4)盛放 NaOH 溶液的玻璃试剂瓶应选用
(5)用四氯化碳萃取溴水后,分液时有机层从分液漏斗的
(6)6.20 g Na2O 晶体中含离子数目是
(7)等质量的 NH3 和 H2S 中,氢原子的个数比是
(8)加热某碱式碳酸镁晶体[4MgCO3∙Mg(OH)2∙5H2O]至质量不再变化时,得到 10.0g 残留固体和
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)有下列四组混合物,请选择合适的分离方法进行分离。(填字母)
A.过滤 B.蒸发 C.分液 D.萃取 E.蒸馏 F.升华
①氯化钠溶液提取氯化钠晶体______ 。
②乙醚和苯的混合物______ 。(乙醚和苯沸点分别为34.6℃,80.1℃)
③水和溴苯的混合物______ 。
④氯化钠和碘的固体混合物______ 。
(2)请用下列10种物质的序号填空:只含有极性键的是______ ;既有离子键又有非极性键的是_____ ;既有离子键又有极性键的是_______ 。
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
(3)X、Y为前20号元素,能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,且X原子半径大于Y原子,其电子式为:___________ ;若XY2为共价化合物,且X、Y均为非金属元素,则XY2的结构式为:__________ 。
A.过滤 B.蒸发 C.分液 D.萃取 E.蒸馏 F.升华
①氯化钠溶液提取氯化钠晶体
②乙醚和苯的混合物
③水和溴苯的混合物
④氯化钠和碘的固体混合物
(2)请用下列10种物质的序号填空:只含有极性键的是
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
(3)X、Y为前20号元素,能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,且X原子半径大于Y原子,其电子式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在中学化学实验中学过的可用于分离或提纯物质的方法很多,如重结晶、过滤、盐析……。请将分离或提纯下列各混合物最适宜方法的名称填到横线上。
(1)除去氯化钠溶液中的石灰石:____ 。
(2)除去碘中混有的碘化钠固体:____ 。
(3)除去乙醇中溶解的少量食盐:____ 。
(4)除去Fe(OH)3胶体中混有的Cl-:____ 。
(1)除去氯化钠溶液中的石灰石:
(2)除去碘中混有的碘化钠固体:
(3)除去乙醇中溶解的少量食盐:
(4)除去Fe(OH)3胶体中混有的Cl-:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
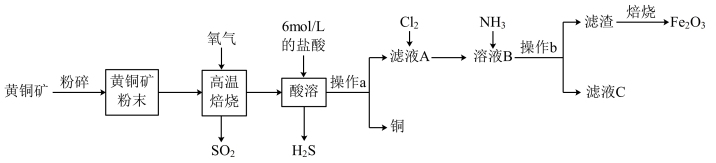
(1)将黄铜矿粉碎的目的是____ 。
(2)高温熔烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子____ mol。
(3)操作a为____ 。
(4)向滤液A中通入Cl2的目的是____ 。
(5)向溶液B中通入NH3后发生反应的离子方程式为____ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
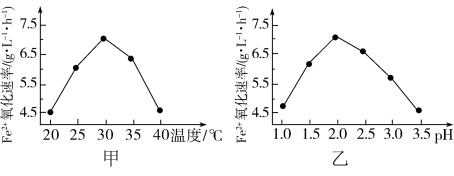
由图甲和图乙判断使用硫杆菌的最佳条件为___ ,若反应温度过高,反应速率下降,其原因是___ 。

(1)将黄铜矿粉碎的目的是
(2)高温熔烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3后发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次




