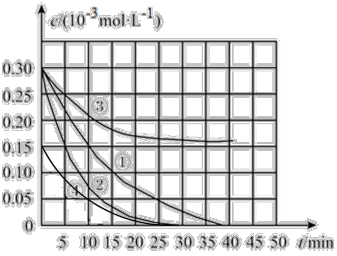
用Na2FeO4溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示。下列说法错误的是
| 实验编号 | 温度/℃ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |
| ④ | 25 | 1 |
| A.实验①中0~15min内M的降解速率为1.33×10−5mol·L−1·min−1 |
| B.若其他条件相同,则实验①②说明升高温度,M的降解速率增大 |
| C.若其他条件相同,则实验①③说明pH越大,越不利于M的降解 |
| D.若其他条件相同,则实验①④说明M的浓度越小,降解的速率越快 |
2017·浙江·一模 查看更多[18]
江苏省连云港市灌南县两校联考2023-2024学年高一下学期3月月考化学试题四川省成都外国语学校2022-2023学年高二上学期12月月考化学试题湖南省长沙市雅礼中学2021-2022学年高一下学期期末考试化学试题(已下线)【浙江新东方】双师223高一下必修第二册RJ第6章综合拓展黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题浙江省金华市东阳中学2019-2020学年高二下学期期中考试化学试题(已下线)考点08 化学反应速率及其影响因素-2020年高考化学命题预测与模拟试题分类精编第六章 化学反应与能量 综合拓展——B拓展区 夯实基础(人教版(2019)第二册)第二章 化学反应与能量学 综合拓展——B 拓展区 夯实基础(人教版必修2)2020届高考二轮复习《化学反应速率与化学平衡》专题卷2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析河南省实验中学2020届高三12月月考化学试题【全国百强校】贵州省铜仁市思南中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】浙江省余姚中学2017-2018学年高二下学期期中考试化学试题2018年3月浙江省暨阳联考化学试题辽宁省大连育明高级中学2018届高三人教版选修四9.8同步周测二化学试题(已下线)浙江省2017届高三“超级全能生”选考科目8月联考(A卷)化学试题
更新时间:2022-07-12 17:22:06
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在反应C(s)+CO2(g)⇌2CO(g)中,可使反应速率明显增大的措施是:
①升高温度或增大压强;②增加碳的量;③恒容通入CO2;④恒压下充入N2降低压强;⑤恒容下通入N2
①升高温度或增大压强;②增加碳的量;③恒容通入CO2;④恒压下充入N2降低压强;⑤恒容下通入N2
| A.①④ | B.②④ | C.①③ | D.③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式如下所示:
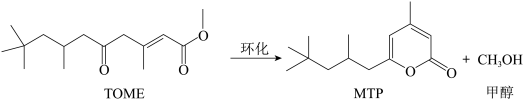
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计,发生的其他副反应忽略不计。

已知:转化率= ,也可以用百分数表示。下列说法错误的是
,也可以用百分数表示。下列说法错误的是

为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计,发生的其他副反应忽略不计。

已知:转化率=
 ,也可以用百分数表示。下列说法错误的是
,也可以用百分数表示。下列说法错误的是| A.X、Y两点消耗反应物TOME的速率v正(X)<v正(Y) |
| B.X、Z两点该化学反应的瞬时速率大小为v(X)>v(Z) |
C.210℃时,0~150 min之间用MTP表示该化学反应的速率为 |
D.若Z点处于化学平衡,则平衡时溶液体系中甲醇的百分含量为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
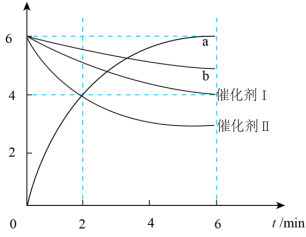
【推荐1】在相同条件下,2L密闭容器中研究催化剂Ⅰ、Ⅱ对反应X 2Y的影响,各物质物质的量n随反应时间t的部分变化曲线如图。下列说法
2Y的影响,各物质物质的量n随反应时间t的部分变化曲线如图。下列说法不正确 的是
 2Y的影响,各物质物质的量n随反应时间t的部分变化曲线如图。下列说法
2Y的影响,各物质物质的量n随反应时间t的部分变化曲线如图。下列说法
| A.b曲线可能表示未加入催化剂时X的物质的量随t的变化 |
| B.a曲线表示使用催化剂Ⅱ时Y的物质的量随t的变化 |
| C.与催化剂Ⅰ相比,使用催化剂Ⅱ反应活化能更高 |
D.使用催化剂Ⅱ时,0~2min内,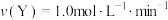 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下,向2L恒容密闭容器中加入6mol M和2mol N,发生反应3M(g)+N(g) xP(g)+2Q(s),2min末该反应达到平衡,生成1.6mol Q,并测得P的浓度为0.8 mol·L-1。下列判断错误的是
xP(g)+2Q(s),2min末该反应达到平衡,生成1.6mol Q,并测得P的浓度为0.8 mol·L-1。下列判断错误的是
 xP(g)+2Q(s),2min末该反应达到平衡,生成1.6mol Q,并测得P的浓度为0.8 mol·L-1。下列判断错误的是
xP(g)+2Q(s),2min末该反应达到平衡,生成1.6mol Q,并测得P的浓度为0.8 mol·L-1。下列判断错误的是| A.x=2 |
| B.0~2min内,M的平均反应速率为0.6 mol·L-1·min-1 |
| C.N的平衡转化率为40% |
| D.混合气体的密度不再变化,不能说明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】探究草酸(H2C2O4)的性质,室温下进行以下两组实验:(已知:室温下,H2C2O4的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5)
下列有关实验说法正确的是( )
| 实验 | 装置 | 试剂a |
| ① |  | 0.1mol·L-1NaOH溶液VmL |
| ② | 0.01mol·L-1酸性KMnO4溶液mL |
| A.若实验①中V=2,则混合后溶液中:c(C2O42-)>c(H2C2O4) |
| B.若实验①中V=4,则混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-) |
| C.实验②反应的离子方程式为5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O |
| D.若实验②测得KMnO4溶液的褪色时间为40s,则这段时间内的平均反应速率v(KMnO4)=2.5×10-4mol•L-1•s-1 |
您最近一年使用:0次

 与Fe反应制
与Fe反应制
 与盐酸反应时增大压强
与盐酸反应时增大压强

