几种短周期元素的原子半径及主要化合价如图所示,下列叙述正确的是
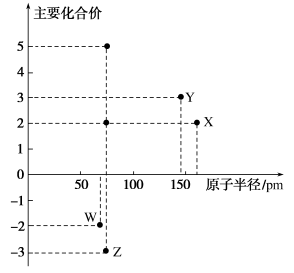

| A.X、Y的最高价氧化物都是两性氧化物 |
B.Y的最高价氧化物对应的水化物能溶于 溶液 溶液 |
| C.Z的非金属性强于W |
| D.X的单质在第三周期中还原性最强 |
21-22高一·全国·单元测试 查看更多[1]
更新时间:2022-08-17 22:06:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】四种短周期主族元素X、W、Y、Z的原子序数依次增大,W(n+ 1)+ 、Xn-的简单离子具有相同的电子层结构,X是地壳含量最大的元素,X与Y同族,下列说法正确的是
1)+ 、Xn-的简单离子具有相同的电子层结构,X是地壳含量最大的元素,X与Y同族,下列说法正确的是
 1)+ 、Xn-的简单离子具有相同的电子层结构,X是地壳含量最大的元素,X与Y同族,下列说法正确的是
1)+ 、Xn-的简单离子具有相同的电子层结构,X是地壳含量最大的元素,X与Y同族,下列说法正确的是| A.简单离子半径:W<X<Y<Z | B.W与Z形成的化合物熔融状态下不导电 |
| C.气态氢化物的热稳定性:X<Y<Z | D.最高价氧化物的水化物的酸性:Y>Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是:


| A.X可能是一种氢化物 |
| B.若Y为单质,Y生成Z属于化合反应 |
| C.E可能是一种有色气体 |
| D.F中M元素的化合价可能为+5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】六种短周期主族元素U、V、W、X、Y、Z的原子序数依次增大,其中V和Y同主族,W为短周期中原子半径最大的元素,X的原子序数是Z的最外层电子数的2倍。已知U的气态氢化物能与其最高价氧化物对应的水化物化合生成离子化合物,单质Y为黄色粉末。下列说法不正确的是
| A.W、X、Y、Z同周期,单质熔点:X>W>Z |
| B.Y和Z的氢化物的水溶液酸性:Z>Y,说明非金属性:Z>Y |
| C.V、W、X三种元素组成的化合物的水溶液可用作木材防火剂 |
| D.U、Z可形成化合物UZ3,各原子最外层均形成8电子的稳定结构 |
您最近一年使用:0次
【推荐1】W、X、Y和Z为原子序数依次增大的四种短周期主族元素。W与X可形成一种红棕色有刺激性气味的气体;Y的周期序数是族序数的3倍;Z的最外层电子数与W的电子总数相同。下列叙述正确的是
A.第一电离能: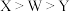 | B.简单离子半径: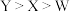 |
C.简单氢化物的稳定性: | D.氧化物对应水化物的酸性: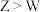 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.能与酸反应生成盐和水的这类物质通常称为碱性氧化物 |
| B.在人类研究物质的微观结构的过程中,光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器先后得到了使用 |
| C.汤姆生发现原子中存在电子,从而提出了“葡萄干面包式”原子结构模型 |
| D.元素周期律是元素原子核外电子排布随元素核电荷数的递增呈现周期性变化的必然结果 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各组微粒按半径由大到小的顺序排列的是( )
| A.Mg、Ca、K、Na | B.Na+、Al3+、Cl-、F- |
| C.Br-、Br、Cl、S | D.S2-、Cl-、K+、Na+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学上存在许多的递变关系,下列递变关系完全正确的是
| A.原子半径:Na>Mg>Al>Cl;离子半径:Na+>Mg2+>Al3+>Cl- |
| B.稳定性:HF>HCl>HBr>HI;熔沸点:HF>HCl>HBr>HI |
| C.熔沸点:Li>Na>K>Rb;密度:Li<Na<K<Rb |
| D.酸性:HClO4>H2SO4>H2CO3;非金属性Cl>S>C |
您最近一年使用:0次




