回答下列问题:
(1)根据Mn原子的核外电子排布情况,回答下列问题:
①价层电子排布图为_______ 。
②在Mn原子的核外电子中,有_______ 种运动状态不同的电子,最高化合价为_______ 。
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_______ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为_______ 。
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ ,电子占据最高能级的电子云轮廓图为_______ 形。
②Li、B、H元素的电负性由大到小的排列顺序为_______ 。离子半径Li+_______ H-(填“>”“=”或“<”)。
(4)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是_______ (填“金属”或“非金属”),元素X与元素Y形成的化合物属于_______ (填“离子化合物”或“共价化合物”),该化合物中显负价的是_______ (填“X”或“Y”)。
(1)根据Mn原子的核外电子排布情况,回答下列问题:
①价层电子排布图为
②在Mn原子的核外电子中,有
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(4)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
更新时间:2022-05-17 21:42:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】各能级所含有原子轨道数目
| 能级符号 | ns | np | nd | nf |
| 轨道数目 |
您最近一年使用:0次
【推荐2】(1)①Cu元素基态原子的外围电子排布式为______________ 。
②元素C、N、O的第一电离能由大到小的排列顺序为________ 。
(2)下列说法正确的是________ (填序号)。
A.第一电离能:As>Ga
B.电负性:As>Ga
C.原子半径:As>Ga
(3)①锗(Ge)是用途很广的半导体材料,基态锗原子的外围电子排布式为________ 。
②在第二周期中,第一电离能位于硼元素与氮元素之间的元素有________ 种。
(4)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:Ga与B同主族,Ga的基态原子的核外电子排布式为________ ,B、C、O三种元素的第一电离能由大到小的顺序是________ 。
②元素C、N、O的第一电离能由大到小的排列顺序为
(2)下列说法正确的是
A.第一电离能:As>Ga
B.电负性:As>Ga
C.原子半径:As>Ga
(3)①锗(Ge)是用途很广的半导体材料,基态锗原子的外围电子排布式为
②在第二周期中,第一电离能位于硼元素与氮元素之间的元素有
(4)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:Ga与B同主族,Ga的基态原子的核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】第三代半导体材料的优异性能和对新兴产业的巨大推动作用,使得发达国家都把发展第三代半导体材料及其相关器件等列为半导体重要新兴技术领域,投入巨资支持发展。第三代半导体材料有氮化镓、碳化硅等。请回答下列问题:
(1)硅原子占据电子的能级符号有________________ ,其中占据电子的能量最高的能级符号为________ ,该能层已经容纳了________ 个电子。
(2)N原子中,有电子占据的最高能层符号为________ ,该能层已经容纳的电子数为______ 个。
(3)镓为元素周期表中第31号元素,位于元素周期表第四周期。镓原子具有________ 个能层,每个能层已经容纳的电子数之比为______________ 。
(1)硅原子占据电子的能级符号有
(2)N原子中,有电子占据的最高能层符号为
(3)镓为元素周期表中第31号元素,位于元素周期表第四周期。镓原子具有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ;SO2的空间构型为___________ (用文字描述)。
(2)Fe2+基态核外电子排布式为___________ 。
(3)H2O分子中的键角___________  离子中的键角(填“大于”、“等于”、“小于”)。
离子中的键角(填“大于”、“等于”、“小于”)。
(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(5)N元素的电负性___________ O元素的电负性(填“大于”、“等于”、“小于”)。
 和
和 ,NOx也可在其他条件下被还原为N2。
,NOx也可在其他条件下被还原为N2。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(2)Fe2+基态核外电子排布式为
(3)H2O分子中的键角
 离子中的键角(填“大于”、“等于”、“小于”)。
离子中的键角(填“大于”、“等于”、“小于”)。(4)N2分子中σ键与π键的数目比n(σ)∶n(π)=
(5)N元素的电负性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。基态Cl原子有_______ 种空间运动状态的电子,最高能级的电子其电子云轮廓图为_______ 形;Ti属于_______ 区(填“s”或“p”或“d”或“f”)。
(2)结合VSEPR理论模型及杂化轨道理论分析以下问题:
①ZnCO3中,阴离子空间结构为_______ ,C原子的杂化方式为_______ 。
②S8与热的浓NaOH溶液反应的产物之一为Na2S3,S 的空间结构为
的空间结构为_______ ,其中心原子轨道采取_______ 杂化。
(3)下列物质中:①白磷②CH2=CH2③BF3④NCl3⑤COS⑥H2S含有极性键的非极性分子的是_______ 。
(1)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。基态Cl原子有
(2)结合VSEPR理论模型及杂化轨道理论分析以下问题:
①ZnCO3中,阴离子空间结构为
②S8与热的浓NaOH溶液反应的产物之一为Na2S3,S
 的空间结构为
的空间结构为(3)下列物质中:①白磷②CH2=CH2③BF3④NCl3⑤COS⑥H2S含有极性键的非极性分子的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
①预测周期表中电负性最大的元素应为____________ ;估计钙元素的电负性的取值范围:0.8<X<___________ 。
②写出K的基态原子的电子排布式:_____________________________________ 。
③根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是_____________ ;简述元素电负性X的大小与元素金属性、非金属性之间的关系____________________ 。
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
请仔细分析,回答下列有关问题:
①预测周期表中电负性最大的元素应为
②写出K的基态原子的电子排布式:
③根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
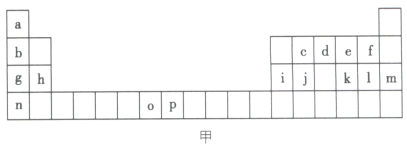
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:___________ 。
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:___________ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的 、
、 可知,气态基态
可知,气态基态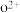 再失去一个电子比基态气态
再失去一个电子比基态气态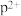 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是___________ 。
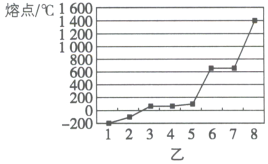
(5)第三周期8种元素按单质熔点高低的顺序排列如图乙所示,其中电负性最大的是___________ (填图中的序号)。
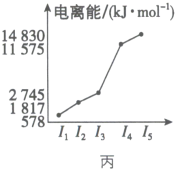
(6)图甲中的某主族元素的电离能情况如图丙所示,则该元素是___________ (填元素符号)。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
比较两元素的
 、
、 可知,气态基态
可知,气态基态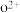 再失去一个电子比基态气态
再失去一个电子比基态气态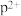 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(5)第三周期8种元素按单质熔点高低的顺序排列如图乙所示,其中电负性最大的是

(6)图甲中的某主族元素的电离能情况如图丙所示,则该元素是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:答下列有关问题:
(1)预测周期表中电负性最大的元素应为____________ ;估计钙元素的电负性的取值范围:___________ < X <___________ 。
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是___________ ;简述元素电负性X的大小与元素金属性、非金属性之间的关系________________ 。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为________ ,其理由是____________________________________ 。
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
您最近一年使用:0次



