化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:
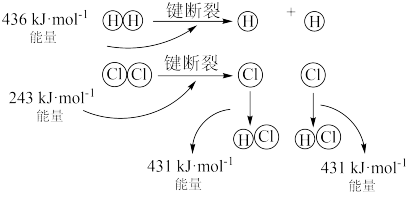
该反应为_______ (填“放热”或“吸热”)反应,其吸收或放出的热量为_______ 。
(2)下列变化中属于吸热反应的是_______ (填序号)。
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C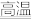 2CO
2CO
⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)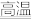 CO+ H2
CO+ H2
⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。
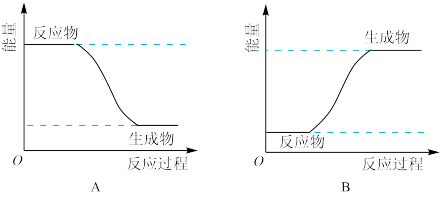
若E1>E2,则该反应可用图_______ (填“A”或“B")表示。
Ⅱ.回答下列问题
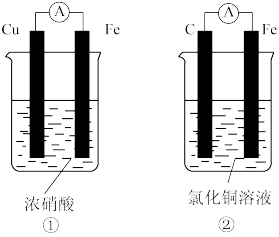
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是_______ (填装置序号),其正极的电极反应式为_______ ;若构建该原电池时两个电极的质量相等,当导线中通过0.4mol电子时,两个电极的质量差为_______ g。
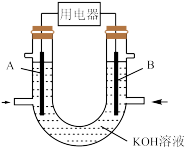
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则_______ (填“A”或“B”)处电极入口通CH4,其电极反应式为_______ 。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:

该反应为
(2)下列变化中属于吸热反应的是
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C
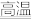 2CO
2CO⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)
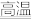 CO+ H2
CO+ H2⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。

若E1>E2,则该反应可用图
Ⅱ.回答下列问题
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是

将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则

更新时间:2022-08-24 22:59:27
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)能源是现代社会物质文明的原动力,与我们每个人息息相关。下图是 反应过程中的能量变化图。
反应过程中的能量变化图。
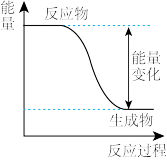
①由图可知,反应物的总键能_______ (填“ ”、“
”、“ ”或“
”或“ ”)生成物的总键能。
”)生成物的总键能。
②已知 氢气完全燃烧生成水蒸气时放出
氢气完全燃烧生成水蒸气时放出 的能量,且氧气中
的能量,且氧气中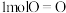 键完全断裂时需要吸收
键完全断裂时需要吸收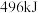 的能量,水蒸气中
的能量,水蒸气中 键形成时放出
键形成时放出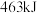 的能量,则氢气中
的能量,则氢气中 键断裂时吸收的能量为
键断裂时吸收的能量为_______ 。
(2)化学电池在通讯、交通及日常生活中有着广泛的应用。
①铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O Pb+PbO2+2H2SO4,铅蓄电池放电时是将
Pb+PbO2+2H2SO4,铅蓄电池放电时是将_______ 能转化为_______ 能,负极是_______ (填物质化学式)。
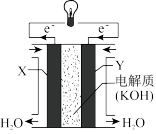
②下图为氢氧燃料电池的构造示意图,由此判断Y极为电池的_______ 极,电极反应式为_______ ; 向
向_______ (填“正”或“负”)极作定向移动,电路中每转移 电子,标准状况下负极上消耗气体的体积是
电子,标准状况下负极上消耗气体的体积是_______ L。
③为了验证 与
与 氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是
氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是_______ 。
A. B.
B. 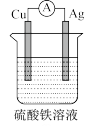 C.
C.  D.
D. 
(1)能源是现代社会物质文明的原动力,与我们每个人息息相关。下图是
 反应过程中的能量变化图。
反应过程中的能量变化图。 
①由图可知,反应物的总键能
 ”、“
”、“ ”或“
”或“ ”)生成物的总键能。
”)生成物的总键能。②已知
 氢气完全燃烧生成水蒸气时放出
氢气完全燃烧生成水蒸气时放出 的能量,且氧气中
的能量,且氧气中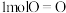 键完全断裂时需要吸收
键完全断裂时需要吸收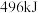 的能量,水蒸气中
的能量,水蒸气中 键形成时放出
键形成时放出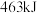 的能量,则氢气中
的能量,则氢气中 键断裂时吸收的能量为
键断裂时吸收的能量为(2)化学电池在通讯、交通及日常生活中有着广泛的应用。
①铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4+2H2O
 Pb+PbO2+2H2SO4,铅蓄电池放电时是将
Pb+PbO2+2H2SO4,铅蓄电池放电时是将②下图为氢氧燃料电池的构造示意图,由此判断Y极为电池的
 向
向 电子,标准状况下负极上消耗气体的体积是
电子,标准状况下负极上消耗气体的体积是
③为了验证
 与
与 氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是
氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是A.
 B.
B.  C.
C.  D.
D. 
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①H 1________ 0,ΔH 3____ 0。(填“>”或“<”)
②N2(g)+O2(g) === 2NO(g) ΔH=_____ kJ·mol-1。
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) ===5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是______ (填字母)。

(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) === 4NO(g)+CO2(g)+2H2O(g) ΔH= -574 kJ·mol-1
CH4(g)+4NO(g) === 2N2(g)+CO2(g)+2H2O(g) ΔH= -1160 kJ·mol-1
H2O(l) === H2O(g) ΔH=44 kJ·mol-1CH4 与NO2 反应生成N2(g)和H2O(g)的热化学方程式为______ ,1.6gCH4还原NO2 生成N2和液态水时放出的热量为____ kJ。
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为____ 。
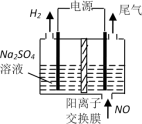
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | ΔH 1 | ΔH 2 | ΔH 3 |
| 热量值kJ·mol-1 | 945 | 498 | 630 |
①H 1
②N2(g)+O2(g) === 2NO(g) ΔH=
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) ===5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是

(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) === 4NO(g)+CO2(g)+2H2O(g) ΔH= -574 kJ·mol-1
CH4(g)+4NO(g) === 2N2(g)+CO2(g)+2H2O(g) ΔH= -1160 kJ·mol-1
H2O(l) === H2O(g) ΔH=44 kJ·mol-1CH4 与NO2 反应生成N2(g)和H2O(g)的热化学方程式为
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为
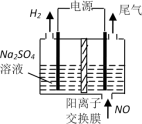
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)化学家GethardErtl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如图:

下列说法正确的是___ (填标号)。
a.①表示N2、H2分子中均是单键
b.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
c.③→④需要吸收能量
d.②→③需要吸收能量
(2)已知N2(g)+O2(g) 2NO(g)K(298K)=5×10-31;N2(g)+3H2(g)
2NO(g)K(298K)=5×10-31;N2(g)+3H2(g)  2NH3(g)K(298K)=4.1×106,请分析工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
2NH3(g)K(298K)=4.1×106,请分析工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是___ 。
(3)对于反应N2(g)+3H2(g) 2NH3(g),在一定条件下氨的平衡含量如表。
2NH3(g),在一定条件下氨的平衡含量如表。
哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是___ 。(提示:温度会影响催化剂的活性)
(4)一定温度下,向容积恒定的密闭容器中充入1mol氮气和3mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1mol氮气和3mol氢气,氮气的平衡转化率_____ (填“变大”“变小”或“不变”)。
(5)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行实验,所得结果如图所示(其他条件相同),则实际生产中适宜选择的催化剂是___ (填“A"“B”或“C”)。

(1)化学家GethardErtl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如图:

下列说法正确的是
a.①表示N2、H2分子中均是单键
b.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
c.③→④需要吸收能量
d.②→③需要吸收能量
(2)已知N2(g)+O2(g)
 2NO(g)K(298K)=5×10-31;N2(g)+3H2(g)
2NO(g)K(298K)=5×10-31;N2(g)+3H2(g)  2NH3(g)K(298K)=4.1×106,请分析工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
2NH3(g)K(298K)=4.1×106,请分析工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是(3)对于反应N2(g)+3H2(g)
 2NH3(g),在一定条件下氨的平衡含量如表。
2NH3(g),在一定条件下氨的平衡含量如表。| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(4)一定温度下,向容积恒定的密闭容器中充入1mol氮气和3mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1mol氮气和3mol氢气,氮气的平衡转化率
(5)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行实验,所得结果如图所示(其他条件相同),则实际生产中适宜选择的催化剂是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种用途。冷敷袋的作用原理可以是_______(双选,填标号)。
(2)以下是三种常见冷敷袋所盛装的主要物质,请从(1)的选项中找出其对应的主要工作原理。
①冰 ②硝酸铵+水 ③硝酸铵+水合碳酸钠
①②③对应的主要工作原理分别是_______ [对应填(1)中选项的标号]。
(3)已知:拆开1 mol H2中的化学键需要吸收436 kJ能量,拆开1 mol O2中的化学键需要吸收496 kJ能量,形成水分子中的1 mol H- O键能够释放463kJ能量。2molH2(g)和1molO2(g)发生反应:2H2(g)+O2(g)=2H2O(g),从微观角度看:断裂反应物中的化学键吸收的总能量E吸=_______ kJ;形成生成物中的化学键放出的总能量E放=_______ kJ。 所以该反应要放出能量。
(4)某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一组实验,实验结果记录如下:
实验1中正极反应式为_______ ;实验2中负极材料为_______ 。
(5)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示。A、B两个电极均由多孔的碳块组成。

该电池的正极反应式为_______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种用途。冷敷袋的作用原理可以是_______(双选,填标号)。
| A.放热的化学变化。 | B.吸热的化学变化 |
| C.放热的物理变化 | D.吸热的物理变化 |
①冰 ②硝酸铵+水 ③硝酸铵+水合碳酸钠
①②③对应的主要工作原理分别是
(3)已知:拆开1 mol H2中的化学键需要吸收436 kJ能量,拆开1 mol O2中的化学键需要吸收496 kJ能量,形成水分子中的1 mol H- O键能够释放463kJ能量。2molH2(g)和1molO2(g)发生反应:2H2(g)+O2(g)=2H2O(g),从微观角度看:断裂反应物中的化学键吸收的总能量E吸=
(4)某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一组实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Mg、Al | NaOH溶液 | 偏向Mg |
(5)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示。A、B两个电极均由多孔的碳块组成。

该电池的正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】在容积为2L的恒容密闭容器中充入3molA,发生可逆反应3A(g) 3B(g)+C(?),能量变化如图所示。
3B(g)+C(?),能量变化如图所示。
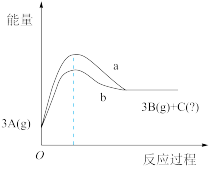
(1)由图可以判断该反应是____ 反应(填“吸热”或“放热”),曲线a和曲线b相比较,可能隐含的反应条件是_____ 。
(2)反应10s后,测得B的浓度为1mol·L-1,此10s内,以A表示的平均反应速率为____ mol·L-1·s-1。
(3)若C为气体,能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是___ (填字母)。
a. b.
b.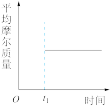 c.
c. d.
d.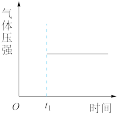
(4)若C为固体,取0.3molA在1L密闭容器中充分反应,平衡时测得B的浓度为0.21mol·L-1。若使反应从逆反应开始,起始时在容器中加入0.3molB,同样条件下,要使平衡时B的浓度仍为0.21mol·L-1,则C的物质的量的取值范围是____ 。
(5)如果平衡后保持温度不变,将容器体积缩小一倍,新平衡时A的浓度是原来的2.2倍,则C是____ 态。
 3B(g)+C(?),能量变化如图所示。
3B(g)+C(?),能量变化如图所示。
(1)由图可以判断该反应是
(2)反应10s后,测得B的浓度为1mol·L-1,此10s内,以A表示的平均反应速率为
(3)若C为气体,能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是
a.
 b.
b. c.
c. d.
d.
(4)若C为固体,取0.3molA在1L密闭容器中充分反应,平衡时测得B的浓度为0.21mol·L-1。若使反应从逆反应开始,起始时在容器中加入0.3molB,同样条件下,要使平衡时B的浓度仍为0.21mol·L-1,则C的物质的量的取值范围是
(5)如果平衡后保持温度不变,将容器体积缩小一倍,新平衡时A的浓度是原来的2.2倍,则C是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图1所示是 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,说明这个反应是
过程中的能量变化示意图,说明这个反应是___________ (填“吸热”或“放热”)反应, 和
和 的总能量
的总能量___________ (填“>”“<”或“=”) 和
和 的总能量。
的总能量。

(2)某温度时,在一个 的密闭容器中,
的密闭容器中, 三种物质物质的量随时间的变化曲线如图2所示。根据图中数据,试填写下列空白:
三种物质物质的量随时间的变化曲线如图2所示。根据图中数据,试填写下列空白:
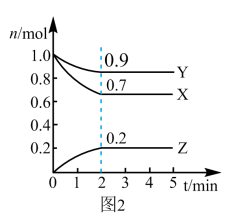
①该反应在___________  时达到平衡状态,该反应从开始到平衡的平均反应速率为
时达到平衡状态,该反应从开始到平衡的平均反应速率为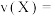
___________ , 的平衡转化率为
的平衡转化率为___________ 。
②该反应的化学方程式为_______________________ 。
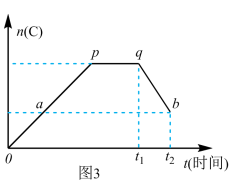
(3)恒温恒容条件下,对于反应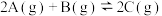 在反应过程中
在反应过程中 的物质的量
的物质的量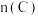 随着时间变化关系如图3所示,现从
随着时间变化关系如图3所示,现从 时刻开始对反应体系升高温度,
时刻开始对反应体系升高温度,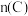 的变化如图
的变化如图 所示。则
所示。则 两点的正反应速率
两点的正反应速率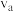
___________ 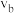 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图1所示是
 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,说明这个反应是
过程中的能量变化示意图,说明这个反应是 和
和 的总能量
的总能量 和
和 的总能量。
的总能量。
(2)某温度时,在一个
 的密闭容器中,
的密闭容器中, 三种物质物质的量随时间的变化曲线如图2所示。根据图中数据,试填写下列空白:
三种物质物质的量随时间的变化曲线如图2所示。根据图中数据,试填写下列空白:
①该反应在
 时达到平衡状态,该反应从开始到平衡的平均反应速率为
时达到平衡状态,该反应从开始到平衡的平均反应速率为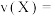
 的平衡转化率为
的平衡转化率为②该反应的化学方程式为
(3)恒温恒容条件下,对于反应
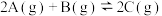 在反应过程中
在反应过程中 的物质的量
的物质的量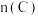 随着时间变化关系如图3所示,现从
随着时间变化关系如图3所示,现从 时刻开始对反应体系升高温度,
时刻开始对反应体系升高温度,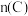 的变化如图
的变化如图 所示。则
所示。则 两点的正反应速率
两点的正反应速率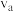
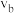 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=_______ kJ/mol;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是_______ (填标号),判断的理由是_______ 。
A.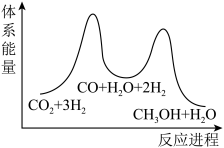 B.
B.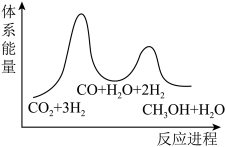
C.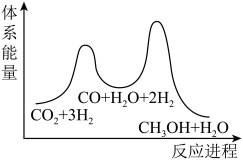 D.
D.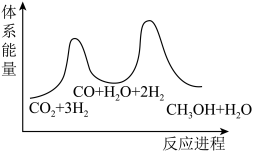
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
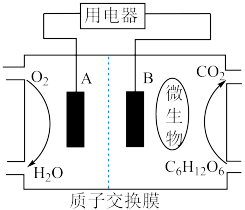
①B为生物燃料电池的_______ (填“正”或“负”)极。
②正极反应式为_______ 。
③电池工作过程中,H+将移向_______ (填“正”或“负”)极。
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=
A.
 B.
B.
C.
 D.
D.
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①B为生物燃料电池的
②正极反应式为
③电池工作过程中,H+将移向
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】微型纽扣电池在现代生活中有广泛应用。下图是一种银锌电池,其电极分别是 和Zn,电解质溶液为KOH溶液。总反应为
和Zn,电解质溶液为KOH溶液。总反应为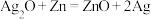 ,其中一个电极反应为
,其中一个电极反应为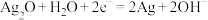 。
。___________ 。
(2)写出另一电极的电极反应式___________ 。
(3)在电池使用的过程中,电解质溶液中KOH的物质的量怎样变化?___________ (增大、减小、不变)。
(4)当电池工作时通过电路对外提供了1mol电子,计算消耗的负极的质量___________ 。
(5)利用下列反应: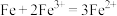 ,选择适当的材料和试剂设计一个原电池。
,选择适当的材料和试剂设计一个原电池。
①请在答卷上的原电池示意图中,标出电极名称、电极材料和电解质溶液。___________ ___________ 。
③电解质溶液中,阳离子向___________ 极移动。
 和Zn,电解质溶液为KOH溶液。总反应为
和Zn,电解质溶液为KOH溶液。总反应为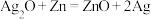 ,其中一个电极反应为
,其中一个电极反应为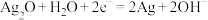 。
。
(2)写出另一电极的电极反应式
(3)在电池使用的过程中,电解质溶液中KOH的物质的量怎样变化?
(4)当电池工作时通过电路对外提供了1mol电子,计算消耗的负极的质量
(5)利用下列反应:
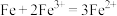 ,选择适当的材料和试剂设计一个原电池。
,选择适当的材料和试剂设计一个原电池。①请在答卷上的原电池示意图中,标出电极名称、电极材料和电解质溶液。
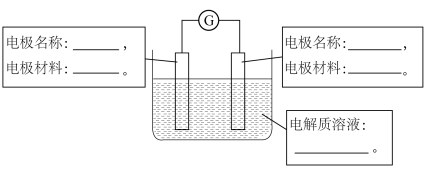
③电解质溶液中,阳离子向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I.化学反应中的能量变化通常表现为热量变化,研究热量变化具有重要的意义。
(1)下列变化属于吸热反应的是___________ (填序号)。
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦Ba(OH)2∙8H2O晶体与NH4Cl晶体的反应 ⑧灼热的木炭与CO2的反应 ⑨甲烷在空气中燃烧的反应
(2)工业合成氨反应: 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
①若1mol N2完全反应生成NH3可___________ (填“吸收”或“放出”)热量___________ kJ。
②如果将1mol N2和3mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是___________ 。
Ⅱ.甲醇(CH3OH)是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;___________ (填“正”或“负”)极,该电极反应式为:___________ 。
(4)当电路中通过1mol电子时,在电极B附近消耗O2的体积为___________ L(标准状况);电池工作一段时间后,电解质溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(1)下列变化属于吸热反应的是
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜 ⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦Ba(OH)2∙8H2O晶体与NH4Cl晶体的反应 ⑧灼热的木炭与CO2的反应 ⑨甲烷在空气中燃烧的反应
(2)工业合成氨反应:
 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mol H—H键、1mol N—H键、1mol N≡N键放出的能量分别为436kJ、391kJ、945.2kJ。则:①若1mol N2完全反应生成NH3可
②如果将1mol N2和3mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是
Ⅱ.甲醇(CH3OH)是优质的清洁燃料,可制作碱性甲醇燃料电池,工作原理如下图所示;

(4)当电路中通过1mol电子时,在电极B附近消耗O2的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业上制硫酸的主要反应之一为: ,反应过程中能量的变化如下图所示。
,反应过程中能量的变化如下图所示。
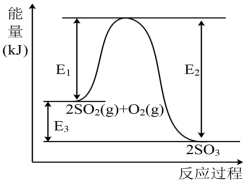
(1)向反应体系中加入催化剂后,图中
___________ (填“增大”、“减小”或“不变”,下同),
___________ 。
(2)已知:
 ;
;
 ;若
;若 与
与 反应产生
反应产生 和
和 ,则该反应的热化学方程式为
,则该反应的热化学方程式为___________ 。
(3)在接触室中,某温度下,反应的起始浓度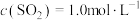 ,
,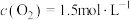 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为___________ 。
(4)在 温度时,该反应的平衡常数K=
温度时,该反应的平衡常数K=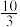 ,若在此温度下,向1L的恒容密闭容器中,充入0.03mol
,若在此温度下,向1L的恒容密闭容器中,充入0.03mol 、0.16mol
、0.16mol ,和0.03mol
,和0.03mol ,则反应开始时向
,则反应开始时向___________ (填“正反应方向”或“逆反应方向”)进行,正反应速率___________ (填“>”、“=”或“<”)逆反应速率。
(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是___________。(填字母)
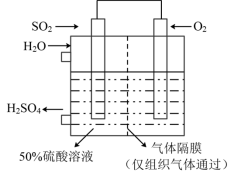
(6)若以如图所示装置生产硫酸,将 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为___________ 。
 ,反应过程中能量的变化如下图所示。
,反应过程中能量的变化如下图所示。
(1)向反应体系中加入催化剂后,图中


(2)已知:

 ;
;
 ;若
;若 与
与 反应产生
反应产生 和
和 ,则该反应的热化学方程式为
,则该反应的热化学方程式为(3)在接触室中,某温度下,反应的起始浓度
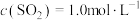 ,
,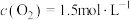 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为(4)在
 温度时,该反应的平衡常数K=
温度时,该反应的平衡常数K=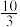 ,若在此温度下,向1L的恒容密闭容器中,充入0.03mol
,若在此温度下,向1L的恒容密闭容器中,充入0.03mol 、0.16mol
、0.16mol ,和0.03mol
,和0.03mol ,则反应开始时向
,则反应开始时向(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是___________。(填字母)
A. 的体积分数不再发生变化 的体积分数不再发生变化 |
| B.恒容时,容器内压强不再发生变化 |
| C.容器内,气体原子总数不再发生变化 |
D.相同时间内消耗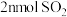 的同时生成 的同时生成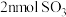 |
 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1)甲烷还原方法是在一定温度、压强及催化剂作用下可消除氮氧化物大气污染,NO、O2和 的混合物反应体系主要发生如下反应:
的混合物反应体系主要发生如下反应:
Ⅰ
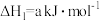
Ⅱ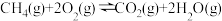

Ⅲ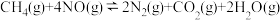
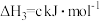
①则反应Ⅳ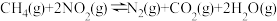
 =
=___________ kJ/mol(用a、b、c表示)。
②若该温度下反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为K1、K2、K3,则反应Ⅳ的平衡常数K4=___________ (用K1、K2、K3表示)。
(2)利用电化学装置可消除氮氧化物污染,变废为宝。
①化学家正在研究尿素动力燃料电池直接去除城市废水中的尿素,既能产生净化的水,又能发电,尿素燃料电池结构如图所示:
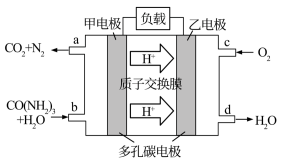
甲的电极反应式为___________ ;理论上每净化1mol尿素,消耗O2的体积约为___________ L(标准状况下)。
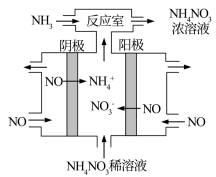
②图为电解NO制备 的装置。该装置中阴极的电极反应式为
的装置。该装置中阴极的电极反应式为___________ ;“反应室”中发生反应的离子方程式为___________ 。
(3)①科学家正在研究一种以乙烯( )为还原剂的脱除NO原理,其脱除机理如图,该脱除反应的化学方程式为
)为还原剂的脱除NO原理,其脱除机理如图,该脱除反应的化学方程式为___________ 。

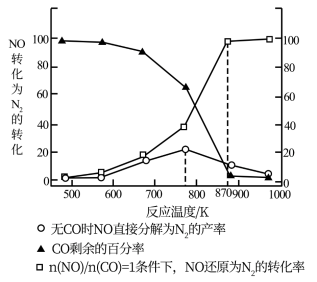
②某研究小组在实验室以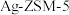 为催化剂,测得NO转化为
为催化剂,测得NO转化为 的转化率随温度变化情况如图所示:若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是
的转化率随温度变化情况如图所示:若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是___________ 。
(1)甲烷还原方法是在一定温度、压强及催化剂作用下可消除氮氧化物大气污染,NO、O2和
 的混合物反应体系主要发生如下反应:
的混合物反应体系主要发生如下反应:Ⅰ

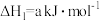
Ⅱ
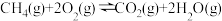

Ⅲ
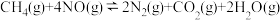
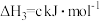
①则反应Ⅳ
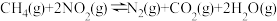
 =
=②若该温度下反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为K1、K2、K3,则反应Ⅳ的平衡常数K4=
(2)利用电化学装置可消除氮氧化物污染,变废为宝。
①化学家正在研究尿素动力燃料电池直接去除城市废水中的尿素,既能产生净化的水,又能发电,尿素燃料电池结构如图所示:

甲的电极反应式为
②图为电解NO制备
 的装置。该装置中阴极的电极反应式为
的装置。该装置中阴极的电极反应式为
(3)①科学家正在研究一种以乙烯(
 )为还原剂的脱除NO原理,其脱除机理如图,该脱除反应的化学方程式为
)为还原剂的脱除NO原理,其脱除机理如图,该脱除反应的化学方程式为
②某研究小组在实验室以
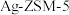 为催化剂,测得NO转化为
为催化剂,测得NO转化为 的转化率随温度变化情况如图所示:若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是
的转化率随温度变化情况如图所示:若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
解题方法
【推荐3】研究人员进行了一组实验:
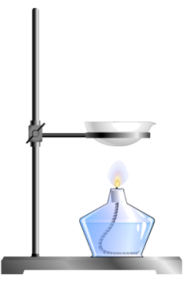
实验一:如图,研究人员将氢氧化钠溶液加入反应容器,随后加入锌粉,随后加热。一段时间后反应完全,停止加热,锌粉仍有剩余,向反应所得溶液中加入一块铜片,并接触剩余的锌,铜片表面出现银白色金属,并伴随少量气体产生。
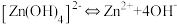
已知:
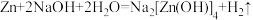
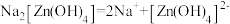
(1)如图,实验一使用的仪器为_______ ,为了防止加热过程中液体沸腾溅出,采取的办法是_______ 。
(2)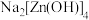 中含有的化学键包括
中含有的化学键包括_______ 。
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)写出氢氧化钠与锌反应的离子方程式:_______ 。
(4)写出实验一中构成的原电池正负极反应:负极:_______ ;正极:_______ 。
(5)研究人员在铜片表面变黄后立刻停止加热,放入水中,这样做的目的是_______ 。
(6)黄铜和黄金外表相似,但化学性质仍然有所区别。若使用硝酸对二者进行鉴别,则现象与结论为_______ 。
(7)若将铜片插入实验一过滤后的上清液中,可否仍然出现上述现象?请解释:_______ 。
实验一:如图,研究人员将氢氧化钠溶液加入反应容器,随后加入锌粉,随后加热。一段时间后反应完全,停止加热,锌粉仍有剩余,向反应所得溶液中加入一块铜片,并接触剩余的锌,铜片表面出现银白色金属,并伴随少量气体产生。
已知:
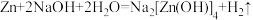
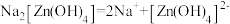

(1)如图,实验一使用的仪器为
(2)
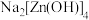 中含有的化学键包括
中含有的化学键包括a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)写出氢氧化钠与锌反应的离子方程式:
(4)写出实验一中构成的原电池正负极反应:负极:
(5)研究人员在铜片表面变黄后立刻停止加热,放入水中,这样做的目的是
(6)黄铜和黄金外表相似,但化学性质仍然有所区别。若使用硝酸对二者进行鉴别,则现象与结论为
(7)若将铜片插入实验一过滤后的上清液中,可否仍然出现上述现象?请解释:
您最近一年使用:0次



