苯乙烯(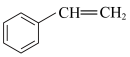 )常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
)常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
I.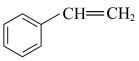


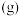

II.

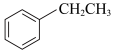
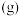
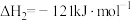
III.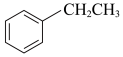


IV.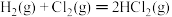

回答下列问题:
(1)①根据上述反应计算得△H3=___________ kJ/mol。
②设NA为阿伏加德罗常数的值。反应II每生成5.3 g苯乙烷,放出的热量为___________ kJ,转移的电子数为___________ NA。
(2)相关化学键的键能数据如下表所示。
①x=___________ 。
②完全燃烧5.2 g苯乙烯,消耗氧气___________ mol。
 )常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:
)常用来合成橡胶,还广泛应用于制药、染料、农药等行业,是石化行业的重要基础原料,苯乙烯与各物质之间反应的能量变化如下:I.



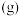

II.



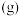
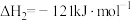
III.



IV.
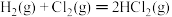

回答下列问题:
(1)①根据上述反应计算得△H3=
②设NA为阿伏加德罗常数的值。反应II每生成5.3 g苯乙烷,放出的热量为
(2)相关化学键的键能数据如下表所示。
| 化学键 | Cl-Cl | H-Cl | H-H |
| 键能/(kJ/mol) | 243 | x | 436 |
②完全燃烧5.2 g苯乙烯,消耗氧气
更新时间:2022-09-04 18:51:28
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】已知分解100 g CaCO3需要177.7 kJ的热量,而12 g碳完全燃烧,则放出393 kJ的热。求:
(1)煅烧1 t石灰石需要多少热量?
(2)这些热量全部由碳燃烧提供,问理论上要消耗多少克碳?
(1)煅烧1 t石灰石需要多少热量?
(2)这些热量全部由碳燃烧提供,问理论上要消耗多少克碳?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
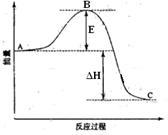
(1)图中A、C分别表示______ 、______ ,E的大小对该反应的反应热有无影响?_______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ,理由是________________________ ;
(2)图中△H=__ KJ·mol-1;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H__ (要求写计算过程)。

(1)图中A、C分别表示
(2)图中△H=
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)已知:① C(s) + O2(g)=CO2(g) H=-393.5 kJ•mol-1
②2CO(g) + O2(g)=2CO2(g) H=-566 kJ•mol-1
③TiO2(s) + 2Cl2(g)=TiCl4(s) + O2(g) H=+141 kJ•mol-1
则TiO2(s) + 2Cl2(g) + 2C(s)=TiCl4(s) + 2CO(g)的H=_________________ 。
(2)氯化银在水中存在沉淀溶解平衡AgCl(s) Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 mol•L-1氯化铝溶液中,银离子浓度最大可达到
Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 mol•L-1氯化铝溶液中,银离子浓度最大可达到_____________ mol•L-1。
(3)20 ℃时,0.1 mol•L-1 NH4Al(SO4)2溶液的pH=3,则:2c(SO42-)-c(NH4+)-3c(Al3+)≈______________ mol•L-1(填数值)。
②2CO(g) + O2(g)=2CO2(g) H=-566 kJ•mol-1
③TiO2(s) + 2Cl2(g)=TiCl4(s) + O2(g) H=+141 kJ•mol-1
则TiO2(s) + 2Cl2(g) + 2C(s)=TiCl4(s) + 2CO(g)的H=
(2)氯化银在水中存在沉淀溶解平衡AgCl(s)
 Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 mol•L-1氯化铝溶液中,银离子浓度最大可达到
Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 mol•L-1氯化铝溶液中,银离子浓度最大可达到(3)20 ℃时,0.1 mol•L-1 NH4Al(SO4)2溶液的pH=3,则:2c(SO42-)-c(NH4+)-3c(Al3+)≈
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)若在常温常压下,l克乙醇完全燃烧生成二氧化碳和液态水放热约为30kJ的热量。写出乙醇燃烧热的热化学方程式__________________________________ 。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小关系。
已知:H2(g)+Cl2(g) 2HCl(g) △H=-185kJ/mol,断裂1 molH-H键吸收的能量为436kJ,断裂1 molCl-Cl键吸收的能量为247kJ,则形成1 molH-Cl键放出的能量为
2HCl(g) △H=-185kJ/mol,断裂1 molH-H键吸收的能量为436kJ,断裂1 molCl-Cl键吸收的能量为247kJ,则形成1 molH-Cl键放出的能量为___________ kJ。
(3)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s) K2S(s)+N2(g)+3CO2(g) △H=xkJ/mol
K2S(s)+N2(g)+3CO2(g) △H=xkJ/mol
已知:碳的燃烧热△H1=akJ·mol-1
S(s)+2K(s) K2S(s) △H2=bkJ·mol-1
K2S(s) △H2=bkJ·mol-1
2K(s)+N2(g)+3O2(g) 2KNO3(s) △H3=ckJ·mol-1则x为
2KNO3(s) △H3=ckJ·mol-1则x为___________ kJ。
(4)根据以下三个热化学方程式:
2H2S(g)+3O2(g) 2SO2(g)+2H2O(1) △H=-Q1kJ/mol
2SO2(g)+2H2O(1) △H=-Q1kJ/mol
2H2S(g)+O2(g) 2S(g)+2H2O(1) △H=-Q2kJ/mol
2S(g)+2H2O(1) △H=-Q2kJ/mol
2H2S(g)+O2(g) 2S(g)+2H2O(g)△H=-Q3kJ/mol
2S(g)+2H2O(g)△H=-Q3kJ/mol
判断Q1、Q2、Q3三者大小关系:________________ 。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小关系。
已知:H2(g)+Cl2(g)
 2HCl(g) △H=-185kJ/mol,断裂1 molH-H键吸收的能量为436kJ,断裂1 molCl-Cl键吸收的能量为247kJ,则形成1 molH-Cl键放出的能量为
2HCl(g) △H=-185kJ/mol,断裂1 molH-H键吸收的能量为436kJ,断裂1 molCl-Cl键吸收的能量为247kJ,则形成1 molH-Cl键放出的能量为(3)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)
 K2S(s)+N2(g)+3CO2(g) △H=xkJ/mol
K2S(s)+N2(g)+3CO2(g) △H=xkJ/mol已知:碳的燃烧热△H1=akJ·mol-1
S(s)+2K(s)
 K2S(s) △H2=bkJ·mol-1
K2S(s) △H2=bkJ·mol-12K(s)+N2(g)+3O2(g)
 2KNO3(s) △H3=ckJ·mol-1则x为
2KNO3(s) △H3=ckJ·mol-1则x为(4)根据以下三个热化学方程式:
2H2S(g)+3O2(g)
 2SO2(g)+2H2O(1) △H=-Q1kJ/mol
2SO2(g)+2H2O(1) △H=-Q1kJ/mol2H2S(g)+O2(g)
 2S(g)+2H2O(1) △H=-Q2kJ/mol
2S(g)+2H2O(1) △H=-Q2kJ/mol2H2S(g)+O2(g)
 2S(g)+2H2O(g)△H=-Q3kJ/mol
2S(g)+2H2O(g)△H=-Q3kJ/mol判断Q1、Q2、Q3三者大小关系:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】I.写出下列反应的热化学方程式。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_____________________ 。
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为________________________ 。
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是_____________________ 。
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________ mol,放出的热量为______________ kJ(用含有a和b的代数式表示)。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】已知:H2(g)+ O2(g)
O2(g) H2O(l),反应过程中能量变化如图所示,则:
H2O(l),反应过程中能量变化如图所示,则:

①a、b、c分别代表什么意义?
a___________________________________ ;
b_____________________________ ;
c___________________________________ 。
②该反应是______ 反应(填“吸热”或“放热”),ΔH_______ 0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是______ 。(请写两条)
(3)已知:H2(g)+ O2(g)
O2(g) H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1
H2(l) H2(g) ΔH=+0.92 kJ·mol-1
H2(g) ΔH=+0.92 kJ·mol-1
O2(l) O2(g) ΔH=+6.84 kJ·mol-1
O2(g) ΔH=+6.84 kJ·mol-1
请写出1mol液氢和液氧生成液态水的热化学方程式:______________________________ 。
 O2(g)
O2(g) H2O(l),反应过程中能量变化如图所示,则:
H2O(l),反应过程中能量变化如图所示,则:
①a、b、c分别代表什么意义?
a
b
c
②该反应是
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是
(3)已知:H2(g)+
 O2(g)
O2(g) H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1H2(l)
 H2(g) ΔH=+0.92 kJ·mol-1
H2(g) ΔH=+0.92 kJ·mol-1 O2(l)
 O2(g) ΔH=+6.84 kJ·mol-1
O2(g) ΔH=+6.84 kJ·mol-1请写出1mol液氢和液氧生成液态水的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】氮的化合物在生产、生活中广泛存在
(1)键能是气态原子形成1mol化学键释放的最低能量。已知下列化学键的键能如表所示,写出1mol气态肼(NH2-NH2)燃烧生成氮气和水蒸气的热化学方程式_________
(2)用焦炭还原NO的反应为:2NO(g)+C(s)  N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
该反应为_____________ (填“放热”或“吸热”)反应乙容器中的反应在60min时达到平衡状态,则0-60min内用NO的浓度变化表示的平均反应速率V(NO)=_________
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
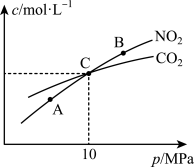
①A、B两点的浓度平衡常数关系:Kc(A)_____________ Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是_____________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=____________ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)键能是气态原子形成1mol化学键释放的最低能量。已知下列化学键的键能如表所示,写出1mol气态肼(NH2-NH2)燃烧生成氮气和水蒸气的热化学方程式
| 化学键 | N≡N | O=O | N-N | N-H | O-H |
| 键能/(kJ/mol) | 946 | 497 | 193 | 391 | 463 |
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
该反应为
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp(C)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】CO2是一种廉价的碳资源,其综合利用具有重要意义,CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)  2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=___________ 。
 2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜)=S(s,斜方) ΔH= -0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是____ [填“S(单斜)”或“S(斜方)”]。
(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)= H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=______ ,若破坏1 molH-H键需消耗的能量436kJ,破坏1 molH-Cl键需消耗的能量431kJ,则破坏1 molCl-Cl键需消耗的能量是_________ 。
(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:____ 。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为______ 。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为____ 。

(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)=
 H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为

您最近一年使用:0次



