关于锂的结构和性质的判断错误的是
①与水反应比钠剧烈
②原子半径比钠小
③其氧化物露置于空气中易吸收CO2
④它的阳离子最外层电子数与Na+的最外层电子数相同
⑤通常作为还原剂
①与水反应比钠剧烈
②原子半径比钠小
③其氧化物露置于空气中易吸收CO2
④它的阳离子最外层电子数与Na+的最外层电子数相同
⑤通常作为还原剂
| A.①④ | B.②③ | C.③⑤ | D.只有① |
22-23高一上·全国·课时练习 查看更多[1]
(已下线)4.1元素周期表-同步学习必备知识
更新时间:2022-09-06 16:20:13
|
相似题推荐
单选题
|
容易
(0.94)
【推荐1】下列关于物质性质的比较中不正确的是
| A.碱性:KOH>NaOH>LiOH |
| B.金属性:Na>Mg>Al |
| C.原子半径:Na>S>O |
| D.酸性强弱:H3PO4>H2SO3>HClO4 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】北京大学研究团队制作出碳基芯片,性能远超过同规格硅基芯片。下列有关碳与硅的比较正确的是
| A.碳原子半径大 | B.碳元素金属性强 |
| C.碳元素非金属性强 | D.碳原子最高正化合价大于硅 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列各组化合物的性质比较,不正确的是
| A.酸性:HClO4>HBrO4>HIO4 | B.稳定性:PH3>H2S> HCl |
| C.非金属性:F>O>S | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列说法正确的是
| A.Si、P、S、Cl原子半径依次增大 |
| B.HF、HCl、HBr、HI稳定性依次减弱 |
| C.C、N、O、F 元素的最高正化合价依次升高 |
| D.NaOH、Mg(OH)2、Al(OH)3碱性依次增强 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】现有四种短周期元素的有关信息如表所示
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期序数 | 单质常用于制合金 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 单质是重要的半导体材料 |
| 丙 | 原子最外层电子数是内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质,最外层电子是电子层数的三倍 | 丁的一种单质与 溶液反应生成丁的另一种单质 溶液反应生成丁的另一种单质 |
| A.甲、乙、丙、丁 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.乙、甲、丁、丙 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】在下列各元素中,化合价最高的是
| A.1s22s22p2 | B.1s22s22p6 | C.1s22s22p5 | D.1s22s22p63s23p4 |
您最近一年使用:0次




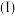
 四种短周期主族元素组成的矿物,可表示为
四种短周期主族元素组成的矿物,可表示为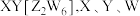 的简单离子的电子层结构相同,
的简单离子的电子层结构相同, 的原子半径比
的原子半径比 的大,
的大, 的单质是常见的半导体材料,
的单质是常见的半导体材料, 是地壳中含量最多的元素。下列说法不正确的是
是地壳中含量最多的元素。下列说法不正确的是 价
价


