氯氧化铜[xCuO·yCuCl2·zH2O]在农业上可用作杀菌剂。以废铜(主要杂质为Fe)为原料,经溶解氧化、调节pH、过滤等步骤,可制备氯氧化铜。
(1)工业上用H2O2和HCl溶解氧化废铜时,反应生成Cu2+时的离子方程式为___________ 。
(2)加Cu2(OH)2CO3调节混合液pH时,其优点是___________ 。
(3)为测定氯氧化铜的组成,现进行如下实验:
步骤I:称取2.5100 g氯氧化铜固体,放入锥形瓶中,加入一定量30%的硝酸使固体完全溶解。滴加K2CrO4溶液作指示剂,用1.00mol·L-1 AgNO3标准溶液滴定溶液中的Cl-,滴定至终点时消耗AgNO3标准溶液20.00 mL(已知Ag2CrO4为砖红色沉淀)。
步骤II:称取2.5100 g氯氧化铜固体,放入锥形瓶中,加入一定量硫酸使固体完全溶解。溶液中加入过量的KI固体,充分反应后向溶液中滴入数滴淀粉溶液,用2.00 mol·L-1 Na2S2O3标准溶液滴定,滴定至终点时消耗Na2S2O3标准溶液10.00 mL。
已知步骤II中所发生的反应如下:
2Cu2++4I-=2CuI↓+I2; 2Na2S2O3+I2=2NaI+Na2S4O6。
①步骤I滴定终点时的实验现象是___________ 。
② 通过计算确定氯氧化铜的化学式______ (写出计算过程)。
(1)工业上用H2O2和HCl溶解氧化废铜时,反应生成Cu2+时的离子方程式为
(2)加Cu2(OH)2CO3调节混合液pH时,其优点是
(3)为测定氯氧化铜的组成,现进行如下实验:
步骤I:称取2.5100 g氯氧化铜固体,放入锥形瓶中,加入一定量30%的硝酸使固体完全溶解。滴加K2CrO4溶液作指示剂,用1.00mol·L-1 AgNO3标准溶液滴定溶液中的Cl-,滴定至终点时消耗AgNO3标准溶液20.00 mL(已知Ag2CrO4为砖红色沉淀)。
步骤II:称取2.5100 g氯氧化铜固体,放入锥形瓶中,加入一定量硫酸使固体完全溶解。溶液中加入过量的KI固体,充分反应后向溶液中滴入数滴淀粉溶液,用2.00 mol·L-1 Na2S2O3标准溶液滴定,滴定至终点时消耗Na2S2O3标准溶液10.00 mL。
已知步骤II中所发生的反应如下:
2Cu2++4I-=2CuI↓+I2; 2Na2S2O3+I2=2NaI+Na2S4O6。
①步骤I滴定终点时的实验现象是
② 通过计算确定氯氧化铜的化学式
更新时间:2022-09-03 15:44:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】四氯化锡在有机合成、染料工业中有广泛的应用,其极易水解,熔点为 、沸点为
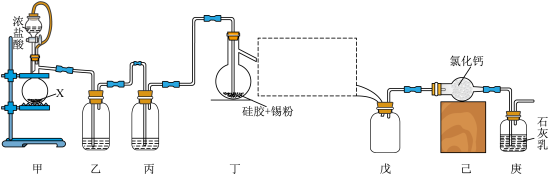
、沸点为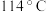 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂 是
是______ (填化学式);装置丙的作用是______ ;方框中仪器的名称是______ 。
(2)当______ (填现象)时,点燃装置丁处的酒精灯。
(3)写出装置庚中反应的化学方程式:______ 。
(4)制得的产品中含少量 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,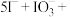
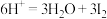 ,
, 。
。
①实验中必须使用______ (填“酸”或“碱”)式滴定管;若滴定时未用标准液润洗滴定管,则测得 的纯度
的纯度______ (填“偏高”或“偏低”)。
②滴定时应选用的指示剂为______ ; 的纯度为
的纯度为______ 。
 、沸点为
、沸点为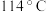 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂
 是
是(2)当
(3)写出装置庚中反应的化学方程式:
(4)制得的产品中含少量
 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,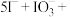
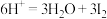 ,
, 。
。①实验中必须使用
 的纯度
的纯度②滴定时应选用的指示剂为
 的纯度为
的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验I:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。

(1)装置③的作用是________________________ ,装置①的作用是________________________
(2)装置②中制备ClO2的化学方程式为____________________ 产生ClO2的还原剂是装置④中制备NaClO2的化学方程式为_____________________________
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③____________ ;④低于60℃干燥,得到成品。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO +4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O =2I-+S4O
=2I-+S4O )。
)。
(4)达到滴定终点时的现象为______________________________
(5)该样品中NaClO2的质量分数为(用含m、c、V的代数式表示)。______________
(6)在滴定操作正确无误的情况下,此实验测得结果_____________ (填“偏高”或“偏低”),原因用离子方程式表示为_____________________
实验I:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。

(1)装置③的作用是
(2)装置②中制备ClO2的化学方程式为
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO
 +4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O )。
)。(4)达到滴定终点时的现象为
(5)该样品中NaClO2的质量分数为(用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验测得结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮化锶(Sr3N2)是工业上生产荧光粉的原材料。已知:锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应产生氨气。
I.利用装置A和B制备

(1)装置A中仪器b名称为___________ ,a导管的作用是___________ ;实验时先点燃装置___________ 处酒精灯(填“A”或“B”),一段时间后,点燃另一只酒精灯。
(2)装置B中广口瓶盛放的试剂是___________ (填名称)。碱石灰的作用是___________ 。
(3)装置A制备N2的化学方程式为___________ 。
Ⅱ.测定产品的纯度
称取6.0g产品,放入干燥的三颈瓶中,然后加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用200.00mL1.0000mol/L的盐酸标准溶液完全吸收(吸收液体体积变化忽略不计)从烧杯中量取20.00mL的吸收液放入锥形瓶中,用1.0000mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00 mLNaOH溶液(图中夹持装置略)
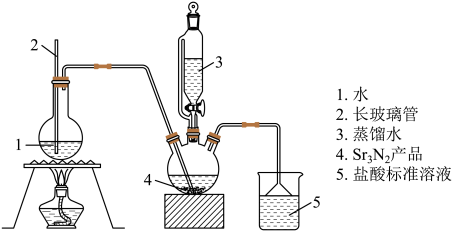
(4)三颈烧瓶中发生反应产生氨气的化学方程式为___________ 。
(5)产品纯度为___________ (精确到小数点后1位)。
(6)下列实验操作可能使氮化锶(Sr3N2)测定结果偏低的___________(填标号)。
I.利用装置A和B制备

(1)装置A中仪器b名称为
(2)装置B中广口瓶盛放的试剂是
(3)装置A制备N2的化学方程式为
Ⅱ.测定产品的纯度
称取6.0g产品,放入干燥的三颈瓶中,然后加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用200.00mL1.0000mol/L的盐酸标准溶液完全吸收(吸收液体体积变化忽略不计)从烧杯中量取20.00mL的吸收液放入锥形瓶中,用1.0000mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00 mLNaOH溶液(图中夹持装置略)

(4)三颈烧瓶中发生反应产生氨气的化学方程式为
(5)产品纯度为
(6)下列实验操作可能使氮化锶(Sr3N2)测定结果偏低的___________(填标号)。
| A.锥形瓶洗涤干净后未干燥,直接装入待测液 |
| B.滴定时未用NaOH标准溶液润洗滴定管 |
| C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失 |
| D.读数时,滴定前平视,滴定后俯视 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐1】化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L−1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________ 。
(2)Ⅱ中发生反应的离子方程式是_______________________________ 。
(3)Ⅲ中发生反应的化学方程式是_________________________________ 。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是______________________________ 。
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是________ 。
(6)Ⅴ中滴定至终点的现象是_____________________________ 。
(7)废水中苯酚的含量为___________ g·L−1(苯酚摩尔质量:94 g·mol −1)。
(8)由于Br2具有____________ 性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L−1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(2)Ⅱ中发生反应的离子方程式是
(3)Ⅲ中发生反应的化学方程式是
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是
(6)Ⅴ中滴定至终点的现象是
(7)废水中苯酚的含量为
(8)由于Br2具有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】一氧化二氯(Cl2O)是一种常用的氯化剂。常温下,Cl2O是棕黄色、有刺激性气味的气体,熔 点为-120.6°C,沸点为2.0°C,易与水反应生成次氯酸。实验室欲用氯气通入含水8%的碳酸钠固体中 制备并收集少量纯净的Cl2O,请用下列装置设计实验并探究相关物质的性质。
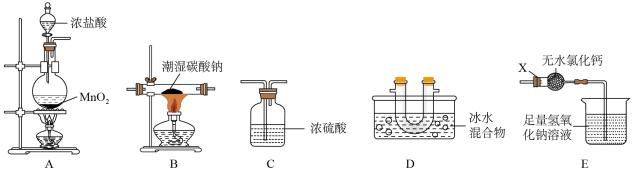
(1)装置E中仪器X的名称为______ 。
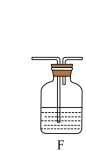
(2)装置的连接顺序是A__________ (每个装置限用一次)。
(3)装置F中盛装试剂的名称为______ ,装置E中无水氯化钙的作用是 ________ .。
(4)装置B残留固体中除NaCl外还含有一种酸式盐M,写出装置B中发生反应的化学方程式_______ 。
(5)证明残留固体中含有M的最简单的实验方案是:_______ 。
(6)测定残留固体中M的质量分数:取mg样品加适量蒸馏水使之溶解,加入几滴酚酞,用0.1 mol/L 的盐酸标准溶液滴定至溶液由红色变为无色,消耗盐酸V1mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸V2 mL.。
①实验时用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、____ 。
②求残留固体中M的质量分数__________ (用含m、V1和 的代数式表示)。
的代数式表示)。
③若用甲基橙作指示剂滴定结束时,滴定管尖头有气泡,测定结果将____ 填“偏高"、“偏低”或“不变”)。


(1)装置E中仪器X的名称为
(2)装置的连接顺序是A
(3)装置F中盛装试剂的名称为
(4)装置B残留固体中除NaCl外还含有一种酸式盐M,写出装置B中发生反应的化学方程式
(5)证明残留固体中含有M的最简单的实验方案是:
(6)测定残留固体中M的质量分数:取mg样品加适量蒸馏水使之溶解,加入几滴酚酞,用0.1 mol/L 的盐酸标准溶液滴定至溶液由红色变为无色,消耗盐酸V1mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸V2 mL.。
①实验时用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、
②求残留固体中M的质量分数
 的代数式表示)。
的代数式表示)。③若用甲基橙作指示剂滴定结束时,滴定管尖头有气泡,测定结果将
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】实验室现有一包NaCl、FeCl3、Al2(SO4)3组成的粉末,某课外小组同学为测定其中NaCl的含量,取13.69 g样品进行如下实验(所加试剂均为过量)。

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是______ (填序号)。
(2)生成沉淀C的离子方程式是_________________________________ 。
(3)根据上述实验,判断下列说法正确的是______ (填字母)。
a.溶液D是无色的碱性溶液
b.溶液D中至少含有5种离子
c.向溶液D中加入过量稀硫酸,产生白色沉淀
d.仅用硝酸银一种试剂不能检验溶液D中的氯离子
(4)样品中NaCl的物质的量为______ 。

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是
(2)生成沉淀C的离子方程式是
(3)根据上述实验,判断下列说法正确的是
a.溶液D是无色的碱性溶液
b.溶液D中至少含有5种离子
c.向溶液D中加入过量稀硫酸,产生白色沉淀
d.仅用硝酸银一种试剂不能检验溶液D中的氯离子
(4)样品中NaCl的物质的量为
您最近一年使用:0次



