某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验I:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。

(1)装置③的作用是________________________ ,装置①的作用是________________________
(2)装置②中制备ClO2的化学方程式为____________________ 产生ClO2的还原剂是装置④中制备NaClO2的化学方程式为_____________________________
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③____________ ;④低于60℃干燥,得到成品。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO +4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O =2I-+S4O
=2I-+S4O )。
)。
(4)达到滴定终点时的现象为______________________________
(5)该样品中NaClO2的质量分数为(用含m、c、V的代数式表示)。______________
(6)在滴定操作正确无误的情况下,此实验测得结果_____________ (填“偏高”或“偏低”),原因用离子方程式表示为_____________________
实验I:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。

(1)装置③的作用是
(2)装置②中制备ClO2的化学方程式为
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO
 +4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O )。
)。(4)达到滴定终点时的现象为
(5)该样品中NaClO2的质量分数为(用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验测得结果
15-16高三上·天津南开·阶段练习 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】为抑制新冠病毒传播,含氯消毒剂被广泛使用。常见的含氯消毒剂有次氯酸盐、ClO2、有机氯化物等。用NaCl电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2。
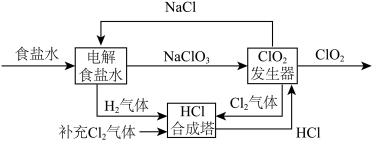
完成下列填空:
(1)Cl原子的最外层电子层上具有_____ 种不同能量的电子;HClO的电子式是_________ ;
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:_________________________
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:_____ 。
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2_____ mol。
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
①NaClO溶液呈碱性的原因是_________________________ (用离子方程式表示)。
②调节NaClO溶液pH时不能选用盐酸的原因为________________ 。
③由表中数据可推断,该实验得到的结论是_____________________
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。_______________

完成下列填空:
(1)Cl原子的最外层电子层上具有
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
NaClO溶液浓度/ (mg·L-1) | 不同pH下的细菌杀灭率/% | ||
pH=4.0 | pH=6.5 | pH=9.0 | |
250 | 98.90 | 77.90 | 53.90 |
①NaClO溶液呈碱性的原因是
②调节NaClO溶液pH时不能选用盐酸的原因为
③由表中数据可推断,该实验得到的结论是
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】铈(Ce)是一种重要的稀土金属元素,常见化合价为+3和+4,在工业上应用广泛。某课题组以回收废旧的电脑显示屏的玻璃粉(含SiO2、CeO2、Fe2O3、和FeO等)为原料,设如下工艺流程回收CeO2,并获得硫酸铁铵晶体[Fe2(SO4)3•2(NH4)2SO4•3H2O]
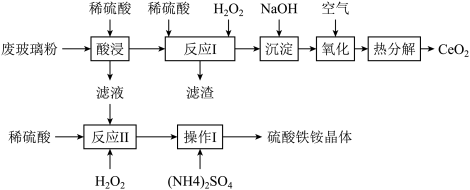
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液;②酸浸时CeO2不反应;③“反应I”所得溶液中含有Ce3+。
试回答下列问题
(1)“滤渣”的化学式为______ 。
(2)在酸性条件下,H2O2、Fe3+、CeO2三种物质中,氧化性最强的是______ ;如将稀硫酸改为盐酸,则“酸浸”过程可能产生的大气污染物是______ 。
(3)“反应Ⅰ”的离子方程式为______ 。
(4)“氧化”反应的化学方程式为______ 。
(5)“操作Ⅰ”依次为:低温蒸发结晶、过滤、______ 常温晾干等操作。所得硫酸铁铵常用作净水剂,在去除酸性废水中的悬浮物时效率降低,原因是______ 。
(6)科学家利用CeO2在太阳能作用下将H2O、CO2转化成H2、CO,其过程如下:mCeO2 (m-x)CeO2•xCe+xO2,
(m-x)CeO2•xCe+xO2,
(m-x)CeO2•xCe+xH2O+xCO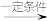 mCeO2+xH2+xCO。在该总转化过程中,CeO2作
mCeO2+xH2+xCO。在该总转化过程中,CeO2作______ ,从能量转化的角度,该过程的重要意义是______ 。

已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液;②酸浸时CeO2不反应;③“反应I”所得溶液中含有Ce3+。
试回答下列问题
(1)“滤渣”的化学式为
(2)在酸性条件下,H2O2、Fe3+、CeO2三种物质中,氧化性最强的是
(3)“反应Ⅰ”的离子方程式为
(4)“氧化”反应的化学方程式为
(5)“操作Ⅰ”依次为:低温蒸发结晶、过滤、
(6)科学家利用CeO2在太阳能作用下将H2O、CO2转化成H2、CO,其过程如下:mCeO2
 (m-x)CeO2•xCe+xO2,
(m-x)CeO2•xCe+xO2,(m-x)CeO2•xCe+xH2O+xCO
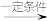 mCeO2+xH2+xCO。在该总转化过程中,CeO2作
mCeO2+xH2+xCO。在该总转化过程中,CeO2作
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】KIO3是常见的食盐加碘剂,实验室制备KIO3晶体的流程如图:
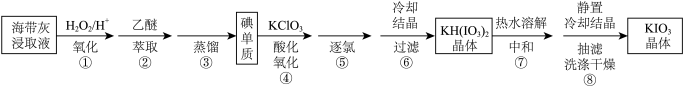
已知:①碘易溶于乙醚,乙醚难溶于水;
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为_____ 。
(2)步骤④中,每1mol碘单质被氧化,转移_____ mol电子。
(3)步骤⑦“中和”的化学方程式为_____ 。步骤⑧中“洗涤”时,最好选用_____ 作为洗涤剂。
(4)以NaIO3为原料制备 的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:
的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:_____ 。
(5)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为_____ mol。I2在KI溶液中可发生反应I2+I- I
I ,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是_____ 。

已知:①碘易溶于乙醚,乙醚难溶于水;
②KIO3在水中的溶解度:20℃为8.1g,80℃为21.8g;KIO3难溶于乙醇。
(1)步骤①“氧化”的离子方程式为
(2)步骤④中,每1mol碘单质被氧化,转移
(3)步骤⑦“中和”的化学方程式为
(4)以NaIO3为原料制备
 的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:
的方法是:先向NaIO3溶液中加入过量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2,请写出上述制备I2的总反应的离子方程式:(5)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1molI2,消耗的KI至少为
 I
I ,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
,KI3易溶于水。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某课题小组利用硫渣与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:四氯化锡(SnCl4)常温下为无色液体、易水解。
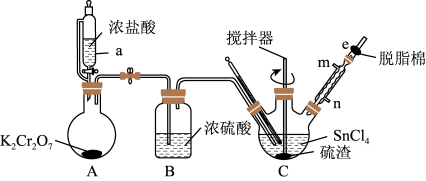
硫渣的化学组成
氯气与硫渣反应相关产物的熔沸点
(1)仪器a的名称_______ ,A中发生反应的化学方程式_______ 。
(2)e中所加物质为_______ ,作用为_______ 。
(3)装置中存在一处缺陷会导致SnCl4产率降低,改进的方法是_______ 。
(4)三颈烧瓶中得到的粗产品进行提纯的方法_______ ;提纯后剩余的固体渣经过处理,可回收的主要金属有_______ 。
(5)已知SnCl4产品中含有少量AsCl3杂质,碘量法可用于测量产品的纯度:取10. 00 g产品溶于水,加入0.100 mol/L标准I2溶液20. 00 mL,并加入少量的淀粉溶液;用0.100×10-2 mol/L的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20. 00 mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O= H3AsO3+ 3HCl
②H3AsO3+I2+H2O= H3AsO4+2HI
③2 +I2=2I-+
+I2=2I-+
则产品中SnCl4的质量分数_______ (保留小数点后1位);若滴定后发现滴管尖嘴处产生了气泡,则测量结果_______ (填“偏高”或“偏低”)。

硫渣的化学组成
| 物质 | Sn | Cu2S | Pb | As | 其他杂质 |
| 质量分数% | 64.43 | 25.82 | 7.34 | 1.23 | 1.18 |
物质 性质 | SnCl4 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 1490 | 951 | 130 | 444 |
(2)e中所加物质为
(3)装置中存在一处缺陷会导致SnCl4产率降低,改进的方法是
(4)三颈烧瓶中得到的粗产品进行提纯的方法
(5)已知SnCl4产品中含有少量AsCl3杂质,碘量法可用于测量产品的纯度:取10. 00 g产品溶于水,加入0.100 mol/L标准I2溶液20. 00 mL,并加入少量的淀粉溶液;用0.100×10-2 mol/L的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20. 00 mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O= H3AsO3+ 3HCl
②H3AsO3+I2+H2O= H3AsO4+2HI
③2
 +I2=2I-+
+I2=2I-+
则产品中SnCl4的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】草酸合铁(Ⅲ)酸钾的体Kx[Fey(C2O4)z] ·nH2O 可用于摄影和蓝色印刷。为确定其组成,某化学兴趣小组在没有氧气干扰下进行如下实验:
实验I.草酸根含量的测定
称取0.9820g样品放入锥形瓶中,加入适量稀硫酸和一定量水,加热至343~358K,用0.2000mol/L KMnO4溶液滴定,滴定过程中草酸转变成CO2逸出反应容器,KMnO4转变成Mn2+。达到滴定终点时,共消耗KMnO4 溶液12.00 mL。
实验II. 铁含量的测定
将上述滴定过的保留液充分加热,使淡紫红色消失。冷却后,调节溶液pH并加入过量的KI固体,充分反应后调节pH至7左右,滴入几滴淀粉溶液作指示剂,用0.2500mol/LNa2S2O3标准溶液滴定至终点。共消耗Na2S2O3溶液8.00mL.(已知: 实验II中涉及的部分离子方程式为I2+2S2O32-=2I-+S4O62-)
请根据上述实验回答下列问题:
(1)实验I在滴定过程中反应的离子方程式为________________ 。
(2)MnO4-在酸性条件下,加热能分解为O2,同时生成Mn2+,若实验II中没有对实验I的保留液进行充分加热,则测定的Fe3+的含量将会____ (填“偏高”、“偏低”或“不变”。)
(3)实验II用淀粉溶液作指示剂,则滴定终点观察到的现象为_________ 。
实验I.草酸根含量的测定
称取0.9820g样品放入锥形瓶中,加入适量稀硫酸和一定量水,加热至343~358K,用0.2000mol/L KMnO4溶液滴定,滴定过程中草酸转变成CO2逸出反应容器,KMnO4转变成Mn2+。达到滴定终点时,共消耗KMnO4 溶液12.00 mL。
实验II. 铁含量的测定
将上述滴定过的保留液充分加热,使淡紫红色消失。冷却后,调节溶液pH并加入过量的KI固体,充分反应后调节pH至7左右,滴入几滴淀粉溶液作指示剂,用0.2500mol/LNa2S2O3标准溶液滴定至终点。共消耗Na2S2O3溶液8.00mL.(已知: 实验II中涉及的部分离子方程式为I2+2S2O32-=2I-+S4O62-)
请根据上述实验回答下列问题:
(1)实验I在滴定过程中反应的离子方程式为
(2)MnO4-在酸性条件下,加热能分解为O2,同时生成Mn2+,若实验II中没有对实验I的保留液进行充分加热,则测定的Fe3+的含量将会
(3)实验II用淀粉溶液作指示剂,则滴定终点观察到的现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】实验室用硫酸厂烧渣(主要成分为Fe2O3及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)〔Fe(OH)(SO4)〕n和绿矾(FeSO4·7H2O),过程如下:
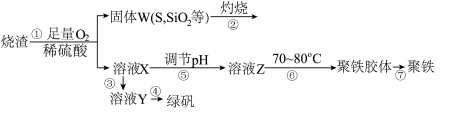
(1)在①中已知FeS中铁元素生成Fe3+,S元素生成单质硫,写出FeS、O2、H2SO4反应的离子方程式___ ;
(2)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是_____ (填编号);A.品红溶液 B.酸性KMnO4溶液 C.紫色石蕊溶液 D.溴水
(3)在③中,需加入的物质是______ ;
(4)在④中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有_____ ;
(5)在⑥中,将溶液Z控制到70~80℃的目的是__ ;
(6)为测量聚铁样品中铁元素的质量分数,进行下列实验(假设杂质中不含铁元素和硫元素):称取一定质量样品,将样品溶于足量的_____ 后(填化学式,下同),滴加过量的__ ,产生不溶于酸的沉淀,过滤、洗涤、干燥,称量固体的质量来计算该聚铁样品中铁元素的质量分数。
(7)若用步骤③④制取绿矾,测定3g烧渣中氧化铁的质量分数
①取所得绿矾产品,溶解,配制成1000mL溶液;量取25.00mL待测溶液于锥形瓶中,配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需_______ 。
②用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为15.00mL。判断此滴定实验达到终点的方法是______ ;若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果______ (填“偏高”“偏低”“无影响”)。
③计算烧渣中铁元素的质量分数为______ 。

(1)在①中已知FeS中铁元素生成Fe3+,S元素生成单质硫,写出FeS、O2、H2SO4反应的离子方程式
(2)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是
(3)在③中,需加入的物质是
(4)在④中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有
(5)在⑥中,将溶液Z控制到70~80℃的目的是
(6)为测量聚铁样品中铁元素的质量分数,进行下列实验(假设杂质中不含铁元素和硫元素):称取一定质量样品,将样品溶于足量的
(7)若用步骤③④制取绿矾,测定3g烧渣中氧化铁的质量分数
①取所得绿矾产品,溶解,配制成1000mL溶液;量取25.00mL待测溶液于锥形瓶中,配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需
②用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为15.00mL。判断此滴定实验达到终点的方法是
③计算烧渣中铁元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等。
I.制备
称取14.0gCuSO4·5H2O、16.0gNa2CO3∙10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含 为止,取出沉淀,风干,得到蓝绿色晶体。
为止,取出沉淀,风干,得到蓝绿色晶体。
(1)①混合物发生反应时有“滋滋”声的原因是____________ 。
②检验生成物已洗涤干净的方法是___________________________ 。
Ⅱ.组成测定
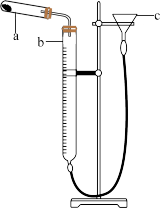
有同学查阅资料发现用Cu(OH)2∙CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2∙nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如图所示。通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。
(2)①仪器b的名称是____________ 。②检查装置气密性的方法是______________ 。
③三次平行实验测定结果如下表,则该样品中m:n=_____________ ,若量气管中所盛液体为水,则该测定值比理论值___ (填“偏大”、“偏小”或“不变”)。
I.制备
称取14.0gCuSO4·5H2O、16.0gNa2CO3∙10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含
 为止,取出沉淀,风干,得到蓝绿色晶体。
为止,取出沉淀,风干,得到蓝绿色晶体。
(1)①混合物发生反应时有“滋滋”声的原因是
②检验生成物已洗涤干净的方法是
Ⅱ.组成测定
有同学查阅资料发现用Cu(OH)2∙CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2∙nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如图所示。通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。
(2)①仪器b的名称是
③三次平行实验测定结果如下表,则该样品中m:n=
实验序号 | 样品质量/g | CO2体积/mL(以折算成标准状况下) |
1 | 0.542 | 44.82 |
2 | 0.542 | 44.80 |
3 | 0.542 | 44.78 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。南宁二中2023级化学兴趣小组在实验室中模拟“侯氏制碱法”制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
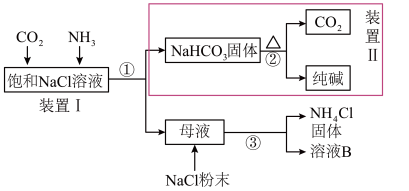
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是___________ (填序号)。过滤时,所需要的玻璃仪器:烧杯、___________ 、___________ 。
(2)向装置Ⅰ的饱和 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量___________ (填“ ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为___________ 。
(3)检验装置Ⅱ中制备的纯碱含有 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,___________ 。
(4)向母液中加入一定量 粉末,存在
粉末,存在 。为使
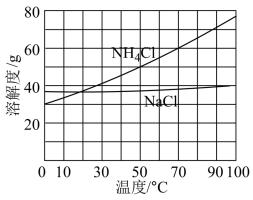
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。
(5)整个实验流程中,可循环利用的物质的化学式是___________ 。
(6)若装置Ⅱ中得到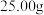 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为___________ 。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是
(2)向装置Ⅰ的饱和
 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量 ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为(3)检验装置Ⅱ中制备的纯碱含有
 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,(4)向母液中加入一定量
 粉末,存在
粉末,存在 。为使
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为
(5)整个实验流程中,可循环利用的物质的化学式是
(6)若装置Ⅱ中得到
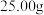 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酰氯 常用作氯化剂和氯磺化剂,可用于医药、农药、染料工业。现在拟用干燥的
常用作氯化剂和氯磺化剂,可用于医药、农药、染料工业。现在拟用干燥的 和
和 在活性炭催化下制取硫酰氯。反应的化学方程式为:
在活性炭催化下制取硫酰氯。反应的化学方程式为: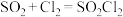 ,实验装置如图所示:
,实验装置如图所示:
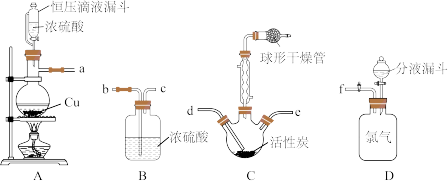
查阅资料:①SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会产生白雾。
②长期放置或者100℃以上发生分解,生成二氧化硫和氯气。
请回答下列问题:
(1)盛装Cu的仪器名称为_______ ,化合物SO2Cl2中S元素的化合价是_______ 。
(2)装置A中发生反应的化学方程式为:_______ ,D为储气装置,用于提供氯气,则装置D的分液漏斗中盛放的试剂为_______ 。
(3)球形干燥管中装有碱石灰,其作用是_______ ,硫酰氯在潮湿空气中产生三氧化硫和盐酸酸雾的化学方程式为_______ 。
(4)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为: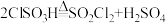 ,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是
,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是_______ 。
(5)当装置A中排出1.12L(已折算成标准状况)气体并全部参与反应时,最终得到2.70g纯净的硫酰氯,则硫酰氯的产率为_______ 。
 常用作氯化剂和氯磺化剂,可用于医药、农药、染料工业。现在拟用干燥的
常用作氯化剂和氯磺化剂,可用于医药、农药、染料工业。现在拟用干燥的 和
和 在活性炭催化下制取硫酰氯。反应的化学方程式为:
在活性炭催化下制取硫酰氯。反应的化学方程式为: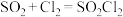 ,实验装置如图所示:
,实验装置如图所示:
查阅资料:①SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇潮湿空气会产生白雾。
②长期放置或者100℃以上发生分解,生成二氧化硫和氯气。
请回答下列问题:
(1)盛装Cu的仪器名称为
(2)装置A中发生反应的化学方程式为:
(3)球形干燥管中装有碱石灰,其作用是
(4)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:
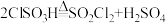 ,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是
,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是(5)当装置A中排出1.12L(已折算成标准状况)气体并全部参与反应时,最终得到2.70g纯净的硫酰氯,则硫酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)仪器A的名称为_______ 。
(2)ClO2可将废水中的CN-氧化成CO2和N2,该反应的离子方程式是_______ 。
(3)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2.某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。
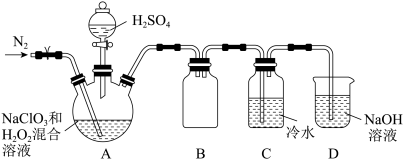
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是_______ 。
②装置B的作用是_______ 。
③装置A用于生成ClO2气体,该反应的化学方程式是_______ 。
(4)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入_______ 作指示剂,用0.1000mol•L-1的Na2S2O3标准液滴定锥形瓶中的溶液(I2+2 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是_______ ,C中ClO2溶液的浓度是_______ mol•L-1。
(1)仪器A的名称为
(2)ClO2可将废水中的CN-氧化成CO2和N2,该反应的离子方程式是
(3)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2.某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置B的作用是
③装置A用于生成ClO2气体,该反应的化学方程式是
(4)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入
 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】三氯化磷(PCl3)是一种基础化工原料使用广泛需求量大。实验室可用白磷与氯气反应制备三氯化磷,实验装置如图所示(夹持装置未画出)。

已知:①氯气与白磷反应放出热量(温度高于75℃)。
②PCl3和PCl5遇水强烈反应并产生大量的白雾。
③PCl3和PCl5的物理常数如下:
回答下列问题:
(1)仪器X的名称是___ ;装置A中发生反应的离子方程式为___ 。
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若装置C或D中发生堵塞时B中的现象是__ 。
(3)为防止装置D因局部过热而炸裂,实验开始前应在圆底烧瓶的底部放少量__ (填“干沙”或“ 水”)。
水”)。
(4)装置E的烧杯中冰盐水的作用是___ 。
(5)装置F的作用:一是防止空气中水蒸气的进入;二是___ 。
(6)前期白磷过量生成PCl3,后期氯气过量生成PCl5,从PC13和PCl5的混合物中分离出PCl3的最佳方法是___ 。

已知:①氯气与白磷反应放出热量(温度高于75℃)。
②PCl3和PCl5遇水强烈反应并产生大量的白雾。
③PCl3和PCl5的物理常数如下:
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 76℃ |
| PCl5 | 146℃ | 200℃分解 |
回答下列问题:
(1)仪器X的名称是
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若装置C或D中发生堵塞时B中的现象是
(3)为防止装置D因局部过热而炸裂,实验开始前应在圆底烧瓶的底部放少量
 水”)。
水”)。(4)装置E的烧杯中冰盐水的作用是
(5)装置F的作用:一是防止空气中水蒸气的进入;二是
(6)前期白磷过量生成PCl3,后期氯气过量生成PCl5,从PC13和PCl5的混合物中分离出PCl3的最佳方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸盐是一种新型绿色净水消毒剂,热稳定性差,在碱性条件下能稳定存在,溶于水发生反应:4FeO42-+10H2O=4Fe(OH)3+3O2↑+8OH-。回答下列问题:
(1)工业上湿法制备高铁酸钾(K2FeO4)的工艺如图:
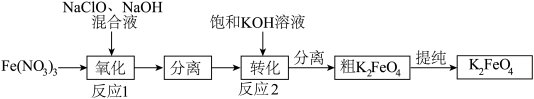
①Na2FeO4中铁元素的化合价为___ ,高铁酸钠用于杀菌消毒时的化学反应类型为___ (填“氧化还原反应”、“复分解反应”或“化合反应”)。
②反应2加入饱和KOH溶液可转化析出K2FeO4,理由是__ 。
(2)化学氧化法生产高铁酸钠(Na2FeO4)是利用Fe(OH)3、过饱和的NaClO溶液和NaOH浓溶液反应,该反应的化学方程式为___ ;理论上每制备0.5mol的Na2FeO4消耗NaClO的质量为___ (保留小数点后1位)。
(3)采用三室膜电解技术制备Na2FeO4的装置如图甲所示,阳极的电极反应式为__ 。电解后,阴极室得到的A溶液中溶质的主要成分为___ (填化学式)。
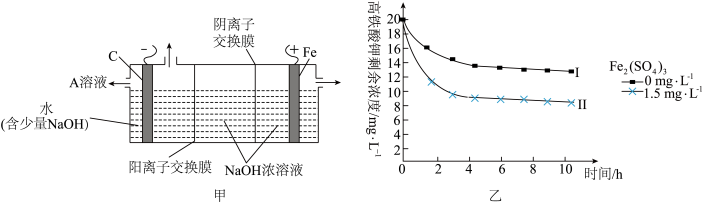
(4)将一定量的K2FeO4投入一定浓度的Fe2(SO4)3溶液中,测得剩余K2FeO4浓度变化如图乙所示,推测曲线I和曲线Ⅱ产生差异的原因是___ 。
(1)工业上湿法制备高铁酸钾(K2FeO4)的工艺如图:

①Na2FeO4中铁元素的化合价为
②反应2加入饱和KOH溶液可转化析出K2FeO4,理由是
(2)化学氧化法生产高铁酸钠(Na2FeO4)是利用Fe(OH)3、过饱和的NaClO溶液和NaOH浓溶液反应,该反应的化学方程式为
(3)采用三室膜电解技术制备Na2FeO4的装置如图甲所示,阳极的电极反应式为

(4)将一定量的K2FeO4投入一定浓度的Fe2(SO4)3溶液中,测得剩余K2FeO4浓度变化如图乙所示,推测曲线I和曲线Ⅱ产生差异的原因是
您最近一年使用:0次



