三氯化磷(PCl3)是一种基础化工原料使用广泛需求量大。实验室可用白磷与氯气反应制备三氯化磷,实验装置如图所示(夹持装置未画出)。

已知:①氯气与白磷反应放出热量(温度高于75℃)。
②PCl3和PCl5遇水强烈反应并产生大量的白雾。
③PCl3和PCl5的物理常数如下:
回答下列问题:
(1)仪器X的名称是___ ;装置A中发生反应的离子方程式为___ 。
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若装置C或D中发生堵塞时B中的现象是__ 。
(3)为防止装置D因局部过热而炸裂,实验开始前应在圆底烧瓶的底部放少量__ (填“干沙”或“ 水”)。
水”)。
(4)装置E的烧杯中冰盐水的作用是___ 。
(5)装置F的作用:一是防止空气中水蒸气的进入;二是___ 。
(6)前期白磷过量生成PCl3,后期氯气过量生成PCl5,从PC13和PCl5的混合物中分离出PCl3的最佳方法是___ 。

已知:①氯气与白磷反应放出热量(温度高于75℃)。
②PCl3和PCl5遇水强烈反应并产生大量的白雾。
③PCl3和PCl5的物理常数如下:
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 76℃ |
| PCl5 | 146℃ | 200℃分解 |
回答下列问题:
(1)仪器X的名称是
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若装置C或D中发生堵塞时B中的现象是
(3)为防止装置D因局部过热而炸裂,实验开始前应在圆底烧瓶的底部放少量
 水”)。
水”)。(4)装置E的烧杯中冰盐水的作用是
(5)装置F的作用:一是防止空气中水蒸气的进入;二是
(6)前期白磷过量生成PCl3,后期氯气过量生成PCl5,从PC13和PCl5的混合物中分离出PCl3的最佳方法是
更新时间:2019-11-30 13:04:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
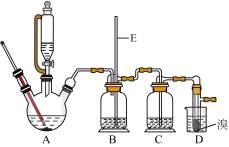
【推荐1】实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置(加热、夹持装置已略去)如图所示:
回答下列问题:
(1)装置D中发生的主要反应的化学方程式为__________ 。
(2)装置B中长玻璃管E的作用是__________ 。
(3)在装置C中应加入氢氧化钠溶液 ,其目的是吸收反应可能生成_____________ 的气体。
(4)反应过程中应用冷水冷却装置D,其主要目的是______________ ;但又不能过度冷却(如用冰水),其原因是__________ ;将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在_______ 层(填“上”或“下”)。
(5)若产物中有少量副产物乙醚,最好用_________ 方法除去。
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 常温下状态 | 无色液体 | 无色液体 | 无色液体 |
密度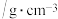 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)装置D中发生的主要反应的化学方程式为
(2)装置B中长玻璃管E的作用是
(3)在装置C中应加入氢氧化钠溶液 ,其目的是吸收反应可能生成
(4)反应过程中应用冷水冷却装置D,其主要目的是
(5)若产物中有少量副产物乙醚,最好用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)写出下列仪器的名称:①__________ ②____________ 。
(2)仪器③中使用前必须检查是否_________________ 。
(3)若利用装置A分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的一种仪器名称为__________ 。冷凝管中冷凝水应从____ (填“f”或“g”)口进,在①中注入液体混合物后,加几片碎瓷片的目的是_____________ 。

(1)写出下列仪器的名称:①
(2)仪器③中使用前必须检查是否
(3)若利用装置A分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的一种仪器名称为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】结合图回答问题:如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)写出上述装置中仪器的名称:①________ 。
(2)若利用上述装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________ ,图1中仪器 ②是从______ 口进水(填a或b)。
(3)图2在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______
(4)从氯化钾溶液中得到氯化钾固体,选择装置______ (填代表装置图的序号,下同);除去自来水中的Cl−等杂质,选择装置______ 。
(5)实验室常用上述装置分离碘水中的碘,进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________ (填序号)。
①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。

(1)写出上述装置中仪器的名称:①
(2)若利用上述装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有
(3)图2在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是
(4)从氯化钾溶液中得到氯化钾固体,选择装置
(5)实验室常用上述装置分离碘水中的碘,进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:
①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学课外兴趣小组为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
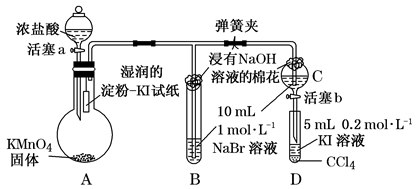
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ. ……
(1)盛放浓盐酸的仪器名称为____________________ 。
(2)在烧瓶内发生反应时,体现浓盐酸的性质为__________________ 。
(3)验证氯气的氧化性强于碘的实验现象是__________________________ 。
(4)B中溶液发生反应的离子方程式是____________________________ 。
(5)浸有NaOH溶液的棉花的作用为______________________________ 。
(6)为验证溴的氧化性强于碘,过程Ⅳ的操作步骤和现象是______________ 。
(7)过程Ⅲ实验的目的是________________________________ 。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ. ……
(1)盛放浓盐酸的仪器名称为
(2)在烧瓶内发生反应时,体现浓盐酸的性质为
(3)验证氯气的氧化性强于碘的实验现象是
(4)B中溶液发生反应的离子方程式是
(5)浸有NaOH溶液的棉花的作用为
(6)为验证溴的氧化性强于碘,过程Ⅳ的操作步骤和现象是
(7)过程Ⅲ实验的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】太和一中理化创新社的同学们为了探究在实验室制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有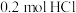 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是_____________________ 。
(2)①装置B的作用是_______________________ ,现象是_____________________ 。
②装置C和D出现的不同现象说明的问题是__________________________ 。
③装置E的作用是_______________________________ 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________ 与_________ 之间(填装置字母序号),装置中应放入___________________________ 。
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(1)若用含有
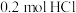 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是(2)①装置B的作用是
②装置C和D出现的不同现象说明的问题是
③装置E的作用是
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】草酸是一种酸,草酸晶体(H2C2O4•2H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O。
(1)草酸的水溶液的pH___ 7(填“>”、“=”、“<”)
(2)实验室可用加热草酸晶体分解的方法获得CO。
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是____ ;
②最后用图1装置收集CO,气体应从___ 端进入(选填“a”或“b”)。

(3)实验图2中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是___ 。
按图3装置将草酸钙晶体(H2C2O4•xH2O)样品高温加热,使其完全分解。
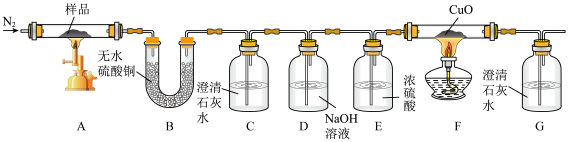
(4)B中观察到硫酸铜变蓝,说明反应生成了_____ ;
(5)C、G中澄清石灰水均变浑浊,说明反应还生成___ 和___ 气体。
(6)反应开始前通入氮气的目的是____ 。
(1)草酸的水溶液的pH
(2)实验室可用加热草酸晶体分解的方法获得CO。
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是
②最后用图1装置收集CO,气体应从

(3)实验图2中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是
按图3装置将草酸钙晶体(H2C2O4•xH2O)样品高温加热,使其完全分解。

(4)B中观察到硫酸铜变蓝,说明反应生成了
(5)C、G中澄清石灰水均变浑浊,说明反应还生成
(6)反应开始前通入氮气的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组参考工业制硝酸的化学原理,在实验室用下列各装置进行组合来制备硝酸并验证硝酸的性质(所给装置必须用到并且只能用一次,各装置中的试剂均足量。已知常温下CaCl2能吸收氨气)。

(1)装置的连接顺序为(用a、b、c、d等字母表示):b接( ) ,( ) 接( ) ,( ) 接( ) 。
(2)写出氨气催化氧化的化学方程式______________________ ;
(3)进行实验时,装置A中碱石灰的作用是_____________ ,D中的现象是_______________ ;
(4)能证明有硝酸生成的现象是__________________________________________ ;
(5)实验开始时,下列操作顺序最合理的是______________
a.先加热A装置中的催化剂.再由导管a通入空气
b.先由导管a通入空气,再加热A装置中的催化剂
c.在由导管a通入空气的同时,加热A装置中的催化剂

(1)装置的连接顺序为(用a、b、c、d等字母表示):b接
(2)写出氨气催化氧化的化学方程式
(3)进行实验时,装置A中碱石灰的作用是
(4)能证明有硝酸生成的现象是
(5)实验开始时,下列操作顺序最合理的是
a.先加热A装置中的催化剂.再由导管a通入空气
b.先由导管a通入空气,再加热A装置中的催化剂
c.在由导管a通入空气的同时,加热A装置中的催化剂
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】亚硝酸钠(NaNO2)是一种重要的工业用盐,某同学针对亚硝酸钠设计了如下实验:
已知:①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
③3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
④酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+。
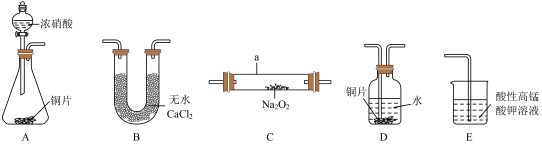
(1)该同学用以上仪器制备NaNO2,则装置的连接顺序为A→___→____→____→___→E。(填序号,可重复)。_______________
(2)仪器a的名称为_____________ 。
(3)D装置的作用___________________ 、_________________ (用化学方程式表示)。
(4)E装置的作用_______________________________________ 。
(5)比色法测定样品中的NaNO2含量:
①在5个有编号的带刻度试管中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2的浓度越大颜色越深),再加蒸馏水至总体积均为10mL并振荡,制成标准色阶:
②称量0.10g制得的样品,溶于水配成500mL溶液,取5mL待测液,加入1mLM溶液,再加蒸馏水至10mL并振荡,与标准比色阶比较:配制上述溶液所需要的玻璃仪器除烧杯、玻璃棒外,还需要___________ (填名称)。
③比色的结果是:待测液的颜色与d组标准色阶相同,则样品中NaNO2的质量分数为________________ 。
已知:①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
③3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
④酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+。

(1)该同学用以上仪器制备NaNO2,则装置的连接顺序为A→___→____→____→___→E。(填序号,可重复)。
(2)仪器a的名称为
(3)D装置的作用
(4)E装置的作用
(5)比色法测定样品中的NaNO2含量:
①在5个有编号的带刻度试管中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2的浓度越大颜色越深),再加蒸馏水至总体积均为10mL并振荡,制成标准色阶:
| 试管编号 | a | b | c | d | e |
| NaNO2含量/(mg·L-1) | 0 | 20 | 40 | 60 | 80 |
②称量0.10g制得的样品,溶于水配成500mL溶液,取5mL待测液,加入1mLM溶液,再加蒸馏水至10mL并振荡,与标准比色阶比较:配制上述溶液所需要的玻璃仪器除烧杯、玻璃棒外,还需要
③比色的结果是:待测液的颜色与d组标准色阶相同,则样品中NaNO2的质量分数为
您最近一年使用:0次
【推荐3】由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用钢材镀铝。工艺流程如下:
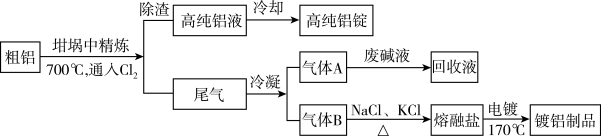
(注:NaCl熔点为801℃;AlCl3在181℃升华)
(1)工业上电解法获得金属铝的过程中,须在氧化铝中加入______ ,其目的是____ 。
(2)精炼前,需清除坩埚内的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,铝与氧化铁反应的化学方程式为:__________ 。
(3)将Cl2连续通入粗铝熔体中,杂质随气泡上浮除去。气泡的成分有____ ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中的物质有________ 。
(4)在用废碱液处理A时,写出主要反应的离子方程式______ 。
(5)镀铝电解池中,以钢材镀件和铝为电极,熔融盐做电解液。则金属铝为________ 极。电镀选择在170℃下进行的原因是_________ 。采用的加热方式最好是_________ 。(填字母选项)
A 水浴 b 油浴 c 直接强热快速升温至170℃
(6)钢材表面镀铝之后,能有效防止钢材腐蚀,其原因是_______ 。

(注:NaCl熔点为801℃;AlCl3在181℃升华)
(1)工业上电解法获得金属铝的过程中,须在氧化铝中加入
(2)精炼前,需清除坩埚内的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,铝与氧化铁反应的化学方程式为:
(3)将Cl2连续通入粗铝熔体中,杂质随气泡上浮除去。气泡的成分有
(4)在用废碱液处理A时,写出主要反应的离子方程式
(5)镀铝电解池中,以钢材镀件和铝为电极,熔融盐做电解液。则金属铝为
A 水浴 b 油浴 c 直接强热快速升温至170℃
(6)钢材表面镀铝之后,能有效防止钢材腐蚀,其原因是
您最近一年使用:0次



