已知乙醇在一定条件下可以还原氧化铜,生成一种产物具有刺激性气味。某实验小组用下列实验装置进行乙醇催化氧化的实验。
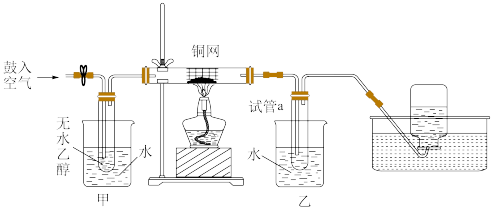
(1) 实验过程中铜网出现红色和黑色交替的现象,请写出铜网由黑色变为红色时发生的化学反应方程式:_______ 。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是_______ (填吸热或放热)反应。
(3)甲和乙两个水浴作用不同。甲的作用是_______ 。
(4)若试管a中收集的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有少量的_______ 。
(5)该反应中两种主要有机物的官能团名称分别是_______ 、_______ 。
(6)当有46g乙醇完全氧化,消耗标况下O2的体积为_______ 。

(1) 实验过程中铜网出现红色和黑色交替的现象,请写出铜网由黑色变为红色时发生的化学反应方程式:
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是
(3)甲和乙两个水浴作用不同。甲的作用是
(4)若试管a中收集的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有少量的
(5)该反应中两种主要有机物的官能团名称分别是
(6)当有46g乙醇完全氧化,消耗标况下O2的体积为
21-22高一下·宁夏银川·期末 查看更多[3]
宁夏银川唐徕回民中学2021-2022学年高一下学期期末考试化学试题(已下线)上海市华东师范大学第二附属中学2022-2023学年高二上学期期末考试化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期11月期中化学试题
更新时间:2022-08-27 18:04:58
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】如下图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。
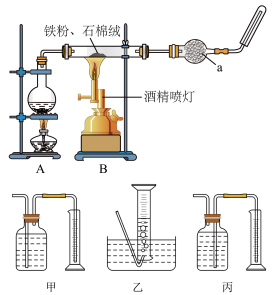
(1)已知该实验的反应方程式为:______________ 。
(2)仪器a的名称是______________ 。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃_____________ (填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用上图中_____________ (填“甲”“乙”或“丙”)装置。
②称取5.6g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448L,则铁粉的转化率为______________ 。


(1)已知该实验的反应方程式为:
(2)仪器a的名称是
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃
②称取5.6g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448L,则铁粉的转化率为

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】某工厂采用如下步骤从海水中提取镁:
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降,过滤,洗涤;
③将沉淀物与盐酸反应,蒸发结晶,过滤,得到含结晶水的晶体;
④将所得晶体在一定条件下加热得到无水氯化镁;
⑤电解熔融氯化镁,得到金属镁。
回答下列问题:
(1)Ca(OH)2所含元素中,质量分数最高的元素为_____ (填元素符号),该元素在地壳中的含量居于第_____ 位。
(2)写出沉淀物中的Mg(OH)2与盐酸反应的离子方程式:_____ ,该反应的基本反应类型为_____ 。
(3)氯化镁溶液在空气中直接加热得到的最终产物为MgO,发生反应的化学方程式为①MgCl2+2H2O Mg(OH)2↓+2HCl;②Mg(OH)2
Mg(OH)2↓+2HCl;②Mg(OH)2 MgO+H2O。反应①利用了盐酸的
MgO+H2O。反应①利用了盐酸的____ (填“酸性”、“还原性”、“氧化性”或“挥发性”),在反应②中,每生成0.4gMgO,此时消耗MgCl2的物质的量为____ mol。
(4)已知海水中镁的含量为1.28g•L-1,每生产1.00t镁,至少需要引入____ L海水(不考虑生产过程中质量的损失)。
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降,过滤,洗涤;
③将沉淀物与盐酸反应,蒸发结晶,过滤,得到含结晶水的晶体;
④将所得晶体在一定条件下加热得到无水氯化镁;
⑤电解熔融氯化镁,得到金属镁。
回答下列问题:
(1)Ca(OH)2所含元素中,质量分数最高的元素为
(2)写出沉淀物中的Mg(OH)2与盐酸反应的离子方程式:
(3)氯化镁溶液在空气中直接加热得到的最终产物为MgO,发生反应的化学方程式为①MgCl2+2H2O
 Mg(OH)2↓+2HCl;②Mg(OH)2
Mg(OH)2↓+2HCl;②Mg(OH)2 MgO+H2O。反应①利用了盐酸的
MgO+H2O。反应①利用了盐酸的(4)已知海水中镁的含量为1.28g•L-1,每生产1.00t镁,至少需要引入
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某工厂废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
已知:还原性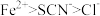
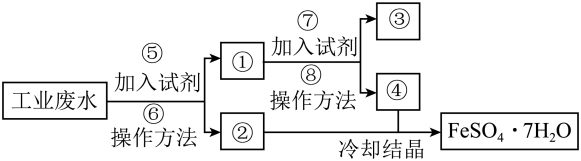
(1)溶液④中溶质的成分为_______ (用化学式表示),操作方法⑥为_______ 。
(2)若取2mL溶液④加入试管中,然后滴入氢氧化钠溶液,产生的现象为_______ ;此过程中属于氧化还原反应的化学方程式是_______ 。
(3)检验溶液②中的金属阳离子时要控制氧化剂用量,若氧化剂过量可能产生的现象是_______ ,请说明产生现象的原因:_______ 。
(4)产品取样研究:取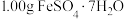 产品加水溶解,滴加
产品加水溶解,滴加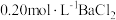 溶液至不再产生沉淀,共消耗
溶液至不再产生沉淀,共消耗 溶液20.00mL,产品的质量分数是
溶液20.00mL,产品的质量分数是_______ ,引起误差的可能原因是_______ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:已知:还原性
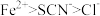

(1)溶液④中溶质的成分为
(2)若取2mL溶液④加入试管中,然后滴入氢氧化钠溶液,产生的现象为
(3)检验溶液②中的金属阳离子时要控制氧化剂用量,若氧化剂过量可能产生的现象是
(4)产品取样研究:取
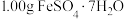 产品加水溶解,滴加
产品加水溶解,滴加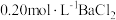 溶液至不再产生沉淀,共消耗
溶液至不再产生沉淀,共消耗 溶液20.00mL,产品的质量分数是
溶液20.00mL,产品的质量分数是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
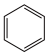
【推荐1】“芬必得”是一种目前很受欢迎的解热、镇痛及抗生素类药物的商品名,其主要成分是化合物对异丁基-α甲基苯乙酸,结构简式如图: ,药名为布洛芬(Brufen),有多种合成路线:已知
,药名为布洛芬(Brufen),有多种合成路线:已知
 +RCl
+RCl
 +HCl
+HCl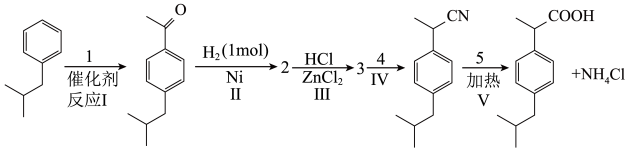
(1)请写出化合物1-5的结构简式(有机物)和分子式(无机物):____________________ ,__________________ ,______________ ,___________________ ,__________________ 。
(2)请写出反应式I,Ⅱ,Ⅲ,IV,V的反应类型:I____________________ ,Ⅱ _________ ,Ⅲ _________ ,Ⅳ_________ ,Ⅴ _________ 。
(3)写出反应Ⅳ的化学方程式_____________________ 。
 ,药名为布洛芬(Brufen),有多种合成路线:已知
,药名为布洛芬(Brufen),有多种合成路线:已知 +RCl
+RCl
 +HCl
+HCl
(1)请写出化合物1-5的结构简式(有机物)和分子式(无机物):
(2)请写出反应式I,Ⅱ,Ⅲ,IV,V的反应类型:I
(3)写出反应Ⅳ的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】X是一种具有果香味的合成香料,如图为合成X的某种流程:

已知:Ⅰ.物质A含有3个碳原子;
Ⅱ.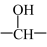 不能最终被氧化为-COOH;
不能最终被氧化为-COOH;
Ⅲ.D的产量可以用来衡量一个国家的石油化工水平。
回答下列问题:
(1)A的结构简式为_______ 。
(2)A→B的反应类型为_______ 。
(3)E分子中官能团的名称为_______
(4)下列关于D和X的说法不正确的是_______。
(5)反应B→C的化学方程式为_______ 。

已知:Ⅰ.物质A含有3个碳原子;
Ⅱ.
 不能最终被氧化为-COOH;
不能最终被氧化为-COOH;Ⅲ.D的产量可以用来衡量一个国家的石油化工水平。
回答下列问题:
(1)A的结构简式为
(2)A→B的反应类型为
(3)E分子中官能团的名称为
(4)下列关于D和X的说法不正确的是_______。
| A.D含有碳碳双键 |
| B.D使酸性高锰酸钾溶液褪色是加成反应 |
| C.X含有酯基。 |
| D.X能发生水解反应 |
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某研究小组按如图路线合成抗抑郁药物吗氯贝胺。
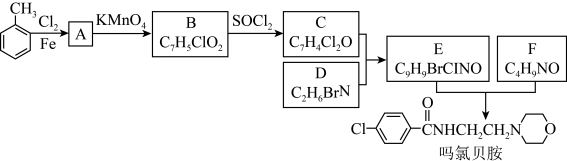
已知:①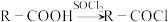 ;
;
②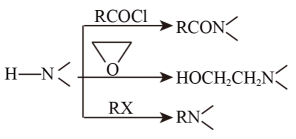
回答下列问题:
(1)A的分子式为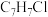 ,且核磁共振氢谱为3组峰,则A的名称为
,且核磁共振氢谱为3组峰,则A的名称为______ 。
(2)A→B的反应类型为______ ,B中含有的官能团名称为______ 。
(3)C的结构简式为______ 。
(4)D具有碱性,核磁共振氢谱峰面积之比为1∶1∶1,写出C+D→E的化学方程式:______ 。
(5)B的同分异构体遇 溶液显色,且结构中存在碳氧双键的共有
溶液显色,且结构中存在碳氧双键的共有______ 种。

已知:①
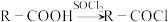 ;
;②

回答下列问题:
(1)A的分子式为
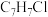 ,且核磁共振氢谱为3组峰,则A的名称为
,且核磁共振氢谱为3组峰,则A的名称为(2)A→B的反应类型为
(3)C的结构简式为
(4)D具有碱性,核磁共振氢谱峰面积之比为1∶1∶1,写出C+D→E的化学方程式:
(5)B的同分异构体遇
 溶液显色,且结构中存在碳氧双键的共有
溶液显色,且结构中存在碳氧双键的共有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】已知A、B、C是中学化学中常见的有机物,它们与乙烯之间有如图的转化关系(图中部分产物已略去)。

请回答下列问题:
(1)A的结构简式为____________ 。
(2)反应②的反应类型为____________ 。
(3)反应③的化学方程式为______________ 。

请回答下列问题:
(1)A的结构简式为
(2)反应②的反应类型为
(3)反应③的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐2】石油是“工业的血液”,是重要的化工原料。
Ⅰ.下图为实验室利用原油合成部分有机物的流程。
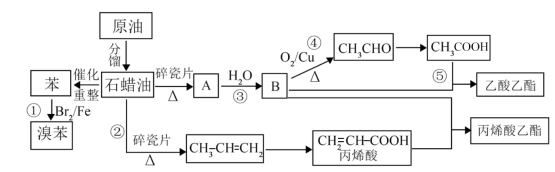
(1)A的产量是衡量一个国家石油化工水平的重要标志,A的结构简式为_______ 。丙烯酸中含氧官能团的名称是_______ 。
(2)写出步骤④的反应方程式:_______ 。
(3)下列说法正确的是_______(填标号)。
(4) 是石油分馏的产物之一,其一氯代物共有
是石油分馏的产物之一,其一氯代物共有_______ 种。
Ⅱ.某化学课外小组用乙醇25g、乙酸30g、浓硫酸适量,在实验室制备并纯化乙酸乙酯。制备装置如图(夹持仪器和加热装置已略去)。
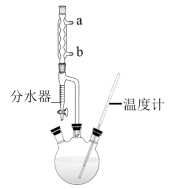
(5)制备乙酸乙酯的化学方程式为_______ ,该反的类型属于_______ 反应。
(6)球形冷凝管中冷凝水从_______ (选填“a”或“b”)处进入。
(7)装置中分水器可实现水和有机层的分离。当分水器中的水层不再增厚时,表明反应_______ 。
(8)乙酸乙酯产品纯化流程如下图。
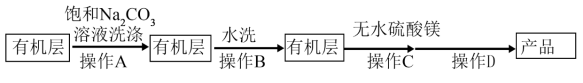
[无水硫酸镁为白色粉末,吸水后形成硫酸镁晶体(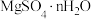 )]
)]
“操作A”为_______ ,“操作C”为_______ 。
(9)实验制得纯乙酸乙酯22g,乙酸乙酯的产率为_______ 。( )
)
Ⅰ.下图为实验室利用原油合成部分有机物的流程。

(1)A的产量是衡量一个国家石油化工水平的重要标志,A的结构简式为
(2)写出步骤④的反应方程式:
(3)下列说法正确的是_______(填标号)。
| A.乙酸与丙烯酸属于同系物 |
| B.苯分子中共有6个原子共面 |
| C.聚丙烯不能使酸性高锰酸钾溶液褪色 |
| D.步骤①中分离苯与溴苯可用分液法 |
 是石油分馏的产物之一,其一氯代物共有
是石油分馏的产物之一,其一氯代物共有Ⅱ.某化学课外小组用乙醇25g、乙酸30g、浓硫酸适量,在实验室制备并纯化乙酸乙酯。制备装置如图(夹持仪器和加热装置已略去)。

(5)制备乙酸乙酯的化学方程式为
(6)球形冷凝管中冷凝水从
(7)装置中分水器可实现水和有机层的分离。当分水器中的水层不再增厚时,表明反应
(8)乙酸乙酯产品纯化流程如下图。

[无水硫酸镁为白色粉末,吸水后形成硫酸镁晶体(
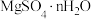 )]
)]“操作A”为
(9)实验制得纯乙酸乙酯22g,乙酸乙酯的产率为
 )
)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D四种有机物在一定条件下的转化关系如图所示(部分反应条件已省略)。已知,A是一种植物生长调节剂,可用于催熟果实,体积分数为75%的B溶液常用于消毒杀菌,C是厨房中一种酸性调味剂的主要成分。B和C在浓硫酸和加热的条件下发生反应,生成的有机物D有特殊的香味。试回答下列问题:
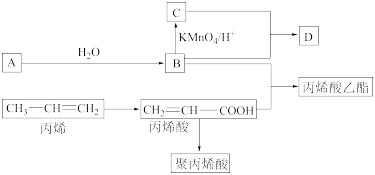
(1)丙烯酸中的含氧官能团名称是___________ 。A在一定条件下与 发生反应的化学方程式
发生反应的化学方程式___________ ;B有很多性质,比较典型的有①能与钠反应;②在铜作催化剂时能与 发生催化氧化,请写出①②中你最熟悉的一个反应的化学方程式
发生催化氧化,请写出①②中你最熟悉的一个反应的化学方程式___________ 。
(2)丙烯在一定条件下与 发生反应的化学方程式为
发生反应的化学方程式为___________ ,判断产物中是否剩余丙烯,可将反应后的混合气体通入___________ (填正确答案标号),然后根据现象判断。
a.酸性高锰酸钾溶液 b.溴水 c.澄清石灰水
(3)B与C反应可生成D,要除去D中混有的B和C可用饱和碳酸钠溶液,该溶液的作用是___________ ;丙烯酸与B反应生成丙烯酸乙酯的化学方程式为___________ ,反应类型为___________ 。
(4)根据丙烯酸的结构判断,丙烯酸可能发生的反应有___________(填正确答案标号)。
①中和反应 ②取代反应 ③加成反应 ④氧化反应

(1)丙烯酸中的含氧官能团名称是
 发生反应的化学方程式
发生反应的化学方程式 发生催化氧化,请写出①②中你最熟悉的一个反应的化学方程式
发生催化氧化,请写出①②中你最熟悉的一个反应的化学方程式(2)丙烯在一定条件下与
 发生反应的化学方程式为
发生反应的化学方程式为a.酸性高锰酸钾溶液 b.溴水 c.澄清石灰水
(3)B与C反应可生成D,要除去D中混有的B和C可用饱和碳酸钠溶液,该溶液的作用是
(4)根据丙烯酸的结构判断,丙烯酸可能发生的反应有___________(填正确答案标号)。
①中和反应 ②取代反应 ③加成反应 ④氧化反应
| A.①③ | B.①②③ | C.①③④ | D.①②③④ |
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
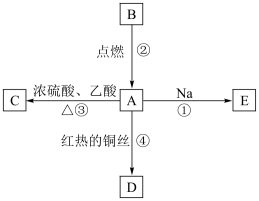
(1)写出A的化学式___________ 。
(2)写出下列反应的化学方程式:反应①___________ ;反应②___________ ;反应③___________ 反应④___________ 。

(1)写出A的化学式
(2)写出下列反应的化学方程式:反应①
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐2】石油是一种重要的资源。A~F是常见有机物,它们之间的转化关系如图1所示(部分产物和反应条件已略去),其中A的产量可以用来衡量一个国家的石油化工发展水平,E是最简单的芳香烃。回答下列问题:
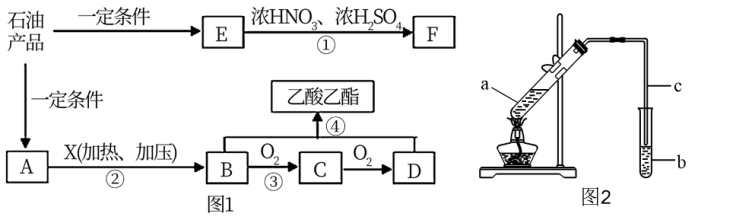
(1)步骤②所用试剂X为___________ (写化学式),D的官能团名称是_______ ;
(2)F的结构简式为________________ ,步骤①的反应类型:___________ ;
(3)写出下列步骤中的化学方程式(注明反应条件):
步骤③_____________________________________ ;
步骤④_______________________________________ ;
(4)用图2所示实验装置制取乙酸乙酯。请回答:试管b中所装溶液应为_____ ,乙酸乙酯生成后,分离出产品时的操作方法是______ 。

(1)步骤②所用试剂X为
(2)F的结构简式为
(3)写出下列步骤中的化学方程式(注明反应条件):
步骤③
步骤④
(4)用图2所示实验装置制取乙酸乙酯。请回答:试管b中所装溶液应为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】如图所示装置,持续通入气体X,可看到a处有红色物质生成,假设各步均反应完全,回答下列问题:
已知: 能还原CuO生成Cu。
能还原CuO生成Cu。
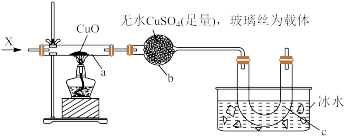
(1)若X为 ,反应前需要先通入
,反应前需要先通入 ,其目的是
,其目的是__________ 。
(2)若X为 ,a处的反应方程式为
,a处的反应方程式为____________ ,b处现象为___________ 。
(3)若X为乙醇蒸气,a处的反应方程式为___________ ;c处收集到的液体有刺激性气味,该液体物质的官能团为_________________ 。
已知:
 能还原CuO生成Cu。
能还原CuO生成Cu。
(1)若X为
 ,反应前需要先通入
,反应前需要先通入 ,其目的是
,其目的是(2)若X为
 ,a处的反应方程式为
,a处的反应方程式为(3)若X为乙醇蒸气,a处的反应方程式为
您最近一年使用:0次



