立德粉 (也称锌钡白),是一种常用白色颜料。以重晶石(
(也称锌钡白),是一种常用白色颜料。以重晶石( )为原料,可按如下工艺生产立德粉:
)为原料,可按如下工艺生产立德粉:
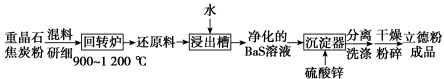
(1)在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,同时生成一种有毒的气体,该过程的化学方程式为_______ 。回转窑尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为 和一种清洁能源气体,该反应的化学方程式为
和一种清洁能源气体,该反应的化学方程式为_______ 。
(2)在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的_______ (填化学式)。
(3)沉淀器中反应的离子方程式为_______ 。
(4)成品中 的含量可以用“碘量法”测得。称取
的含量可以用“碘量法”测得。称取 样品,置于碘量瓶中,移取
样品,置于碘量瓶中,移取 的
的 溶液于其中,并加入乙酸溶液,密闭,置暗处反应
溶液于其中,并加入乙酸溶液,密闭,置暗处反应 ,有单质硫析出。过量的
,有单质硫析出。过量的 用
用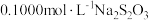 溶液滴定,反应式为
溶液滴定,反应式为 。测定时消耗
。测定时消耗 溶液体积
溶液体积 。样品中
。样品中 的含量为
的含量为_______ (写出表达式)。
(5) 还原性较强,在溶液中易被
还原性较强,在溶液中易被 氧化成
氧化成 。用过量的
。用过量的 作脱氯剂,该反应的离子方程式为
作脱氯剂,该反应的离子方程式为_______ 。
 (也称锌钡白),是一种常用白色颜料。以重晶石(
(也称锌钡白),是一种常用白色颜料。以重晶石( )为原料,可按如下工艺生产立德粉:
)为原料,可按如下工艺生产立德粉:
(1)在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,同时生成一种有毒的气体,该过程的化学方程式为
 和一种清洁能源气体,该反应的化学方程式为
和一种清洁能源气体,该反应的化学方程式为(2)在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的
(3)沉淀器中反应的离子方程式为
(4)成品中
 的含量可以用“碘量法”测得。称取
的含量可以用“碘量法”测得。称取 样品,置于碘量瓶中,移取
样品,置于碘量瓶中,移取 的
的 溶液于其中,并加入乙酸溶液,密闭,置暗处反应
溶液于其中,并加入乙酸溶液,密闭,置暗处反应 ,有单质硫析出。过量的
,有单质硫析出。过量的 用
用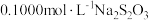 溶液滴定,反应式为
溶液滴定,反应式为 。测定时消耗
。测定时消耗 溶液体积
溶液体积 。样品中
。样品中 的含量为
的含量为(5)
 还原性较强,在溶液中易被
还原性较强,在溶液中易被 氧化成
氧化成 。用过量的
。用过量的 作脱氯剂,该反应的离子方程式为
作脱氯剂,该反应的离子方程式为
更新时间:2022-09-05 23:55:59
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如下:

(1)下列措施无法加快浸取速率的是_______。(填字母)
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______ 。
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是_______。
(4)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______ 。
(5)滤液Ⅱ所含溶质主要是_______ (填化学式)。
(6)该流程中可循环使用的物质是_______ (填化学式)。

(1)下列措施无法加快浸取速率的是_______。(填字母)
| A.延长浸取时间 | B.将辉铜矿粉碎 |
| C.充分搅拌 | D.适当增大硫酸浓度 |
(3)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是_______。
| A.CO2 | B.CuO | C.氨水 | D.HCl |
(5)滤液Ⅱ所含溶质主要是
(6)该流程中可循环使用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。

(1)“煅烧”产生烟气中的SO2用氨水吸收:SO2+NH3·H2O=NH4HSO3。氨水脱硫,并不需要除去烟气中的大量CO2,原因是___________ (用离子方程式表示)。
(2)“还原”步骤除发生铁与 的反应外,还发生反应的离子方程式有
的反应外,还发生反应的离子方程式有___________ 。
(3)检验Fe3+是否完全被还原的实验操作是___________ 。
(4)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的量浓度(写出计算过程)。___________ 。
(5)制备 FeCO3。
①写出“沉铁”步骤发生反应的离子方程式:___________ 。
②设计以FeSO4溶液和NH4HCO3溶液为原料,制备FeCO3的实验方案:___________ 。[FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5]。

(1)“煅烧”产生烟气中的SO2用氨水吸收:SO2+NH3·H2O=NH4HSO3。氨水脱硫,并不需要除去烟气中的大量CO2,原因是
(2)“还原”步骤除发生铁与
 的反应外,还发生反应的离子方程式有
的反应外,还发生反应的离子方程式有(3)检验Fe3+是否完全被还原的实验操作是
(4)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的量浓度(写出计算过程)。
(5)制备 FeCO3。
①写出“沉铁”步骤发生反应的离子方程式:
②设计以FeSO4溶液和NH4HCO3溶液为原料,制备FeCO3的实验方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碳酸锶主要用于彩电显像管的荧屏玻璃和特种玻璃等的制造,通常由天青石矿(主要成分为SrSO4,还含有钡等杂质)制备,制备流程如图所示:

已知:i.锶在“滤液1”“滤液2”中均主要以Sr(HS)2、Sr(OH)2形式存在
ii.SrSO4、BaSO4的KSP分别是3.2×10-7、1.0×10-10
回答下列问题:
(1)步骤①反应:SrSO4+2C SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为
SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为__________________ 。
(2)写出步骤②中“水浸”主要反应的化学方程式:________________________ 。步骤②“过滤”操作需要的主要玻璃仪器为________________________ 。
(3)上述生产工艺的优点是质量好、成本低,但从环保角度考虑该工艺生产存在明显的缺点是______________________________________________________ 。
(4)若向含有Sr2+、Ba2+的“滤液1”中滴加稀硫酸,当两种沉淀共存时,c(Sr2+):c(Ba2+)=________________ 。
(5)写出“碳化”过程中发生反应的化学方程式:_______________________________ 。
(6)某生产企业用a kg的天青石矿(含SrSO4:40%)制备,最终得到b kg碳酸锶产品,产率为______________ (用含a、b的式子表示)。

已知:i.锶在“滤液1”“滤液2”中均主要以Sr(HS)2、Sr(OH)2形式存在
ii.SrSO4、BaSO4的KSP分别是3.2×10-7、1.0×10-10
回答下列问题:
(1)步骤①反应:SrSO4+2C
 SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为
SrS+2CO2↑,若在标准状况下产生3.36 LCO2,则转移电子数为(2)写出步骤②中“水浸”主要反应的化学方程式:
(3)上述生产工艺的优点是质量好、成本低,但从环保角度考虑该工艺生产存在明显的缺点是
(4)若向含有Sr2+、Ba2+的“滤液1”中滴加稀硫酸,当两种沉淀共存时,c(Sr2+):c(Ba2+)=
(5)写出“碳化”过程中发生反应的化学方程式:
(6)某生产企业用a kg的天青石矿(含SrSO4:40%)制备,最终得到b kg碳酸锶产品,产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】重铬酸钾( )是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为
)是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为 ,含
,含 、
、 等杂质)为原料制备重铬酸钾,并进行性质验证实验。
等杂质)为原料制备重铬酸钾,并进行性质验证实验。
已知:相关物质在不同温度时的溶解度/g如下表:
实验一:重铬酸钾的制备
步骤Ⅰ:将一定量NaOH和 的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与
的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与 继续加热50分钟,发生反应:
继续加热50分钟,发生反应: ,自然冷却。
,自然冷却。
步骤Ⅱ:取出坩埚中的熔块,置于烧杯中,加水并加热煮沸15分钟,冷却后抽滤,弃去含铁固体物质。
步骤Ⅲ:用冰醋酸调节上述滤液pH为7到8,产生浑浊,加热后过滤除去 和
和 ,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
步骤Ⅳ:向上述溶液中加KCl,出现少量晶体再次调pH并进行结晶操作,有大量橙色晶体析出,抽滤,用少量冷水洗涤晶体,干燥得 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中下列仪器不需要的是_____ (填仪器名称)。

(2)步骤Ⅲ中调节滤液pH用冰醋酸,不用强酸的原因是_______ ,过滤前先加热的目的是________ 。
(3)步骤Ⅳ中的结晶方法是_______ (填“蒸发结晶”或“冷却结晶”),有同学制得的重铬酸钾晶体颜色偏黄,可能的原因是_______ 。
实验二:用重铬酸钾测定 固体试样中铁的含量
固体试样中铁的含量
已知:二苯胺磺酸钠还原态为无色,氧化态为紫红色。
(4)取重铬酸钾晶体配制成0.02mol/L的标准液。称取2.00g 固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL
固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL 溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
①写出滴定时重铬酸钾和硫酸亚铁反应的离子方程式________ 。
②测定 固体试样中铁的质量分数为
固体试样中铁的质量分数为_____ (保留两位小数)。
③测定结果偏大的可能原因是_______ 。
 )是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为
)是实验室常用的氧化剂。某实验小组以铬铁矿(主要成分为 ,含
,含 、
、 等杂质)为原料制备重铬酸钾,并进行性质验证实验。
等杂质)为原料制备重铬酸钾,并进行性质验证实验。已知:相关物质在不同温度时的溶解度/g如下表:
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| 重铬酸钾 | 4.7 | 12.3 | 26.3 | 45.6 | 73 |
| 重铬酸钠 | 163 | 183 | 215 | 269 | 76 |
步骤Ⅰ:将一定量NaOH和
 的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与
的固体置于铁坩埚内,加热至熔融,再加铬铁矿粉与 继续加热50分钟,发生反应:
继续加热50分钟,发生反应: ,自然冷却。
,自然冷却。步骤Ⅱ:取出坩埚中的熔块,置于烧杯中,加水并加热煮沸15分钟,冷却后抽滤,弃去含铁固体物质。
步骤Ⅲ:用冰醋酸调节上述滤液pH为7到8,产生浑浊,加热后过滤除去
 和
和 ,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。
,将滤液转移至蒸发皿中,加冰醋酸调节pH为5。步骤Ⅳ:向上述溶液中加KCl,出现少量晶体再次调pH并进行结晶操作,有大量橙色晶体析出,抽滤,用少量冷水洗涤晶体,干燥得
 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中下列仪器不需要的是

(2)步骤Ⅲ中调节滤液pH用冰醋酸,不用强酸的原因是
(3)步骤Ⅳ中的结晶方法是
实验二:用重铬酸钾测定
 固体试样中铁的含量
固体试样中铁的含量已知:二苯胺磺酸钠还原态为无色,氧化态为紫红色。
(4)取重铬酸钾晶体配制成0.02mol/L的标准液。称取2.00g
 固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL
固体试样于锥形瓶中,加15.00mL混合酸,再加水配成100mL溶液,取10.00mL 溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。
溶液于锥形瓶,加入几滴二苯胺磺酸钠作指示剂,用重铬酸钾标准液滴定至由绿色变为紫红色,消耗标准液8.00mL。①写出滴定时重铬酸钾和硫酸亚铁反应的离子方程式
②测定
 固体试样中铁的质量分数为
固体试样中铁的质量分数为③测定结果偏大的可能原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酰硫酸( ,
, )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
ⅱ.实验室制备亚硝酰硫酸的原理为 ,
,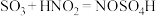 。
。
(1)仪器Ⅰ的名称为______ ,按照气流从左到右的顺序,上述仪器的连接顺序为______ (填仪器接口的字母,字母之间用“→”连接,部分仪器可以重复使用)。
(2)为了控制通入B中的 的通入速率,可以采取的措施是
的通入速率,可以采取的措施是______ 。
(3)装置B中三颈烧瓶需置于冷水浴中并维持反应体系温度不得高于20℃,若装置B中温度过高将导致产品产率降低,可能的原因是______ (任写一个原因即可得分)。
(4)装置C的作用为防止亚硝酰硫酸遇水反应,请写出亚硝酰硫酸与水反应化学方程式______ 。
(5)测定亚硝酰硫酸的纯度:
步骤①:准确称取25.4g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL溶液于锥形瓶中,加入60.00mL未知浓度 溶液(过量)和10.00mL25%的
溶液(过量)和10.00mL25%的 溶液,摇匀,发生反应
溶液,摇匀,发生反应
步骤③:向该溶液中滴加 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。
步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶液的体积为60.00mL。滴定终点时的现象为
溶液的体积为60.00mL。滴定终点时的现象为______ ,亚硝酰硫酸的纯度为______ (精确到0.1%)。
 ,
, )在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
)在重氮化反应中可以代替亚硝酸钠。实验室用如图所示装置(部分夹持仪器略)制备少量亚硝酰硫酸,并测定产品纯度。
ⅱ.实验室制备亚硝酰硫酸的原理为
 ,
,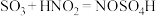 。
。(1)仪器Ⅰ的名称为
(2)为了控制通入B中的
 的通入速率,可以采取的措施是
的通入速率,可以采取的措施是(3)装置B中三颈烧瓶需置于冷水浴中并维持反应体系温度不得高于20℃,若装置B中温度过高将导致产品产率降低,可能的原因是
(4)装置C的作用为防止亚硝酰硫酸遇水反应,请写出亚硝酰硫酸与水反应化学方程式
(5)测定亚硝酰硫酸的纯度:
步骤①:准确称取25.4g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL溶液于锥形瓶中,加入60.00mL未知浓度
 溶液(过量)和10.00mL25%的
溶液(过量)和10.00mL25%的 溶液,摇匀,发生反应
溶液,摇匀,发生反应
步骤③:向该溶液中滴加
 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。步骤④:把亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗
 溶液的体积为60.00mL。滴定终点时的现象为
溶液的体积为60.00mL。滴定终点时的现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】利用酸解法制钛白粉产生的废液[含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4],生产铁红和补血剂乳酸亚铁。其生产步骤如图:
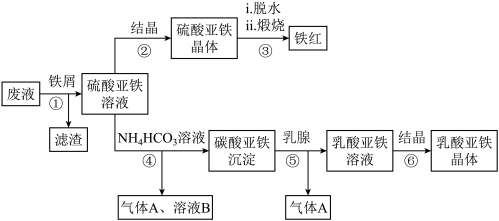
已知:TiOSO4可溶于水,在水中可以电离为TiO2+和 。请回答:
。请回答:
(1)步骤①中分离硫酸亚铁溶液和滤渣的操作是______________________ 。
(2)滤渣的主要成分为TiO2•xH2O,写出TiOSO4水解生成TiO2•xH2O的化学方程式为_____ 。
(3)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为______________ 。
(4)用平衡移动的原理解释步骤⑤中加乳酸能得到乳酸亚铁的原因____________________________ 。
(5)步骤④的离子方程式为___________ 。
(6)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及_________ 。
(7)为测定步骤②中所得晶体中FeSO4·7H2O的质量分数,取晶体样品a g,溶于稀硫酸配成100.00 mL溶液,取出20.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1 KMnO4溶液20.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)___________________ 。

已知:TiOSO4可溶于水,在水中可以电离为TiO2+和
 。请回答:
。请回答:(1)步骤①中分离硫酸亚铁溶液和滤渣的操作是
(2)滤渣的主要成分为TiO2•xH2O,写出TiOSO4水解生成TiO2•xH2O的化学方程式为
(3)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为
(4)用平衡移动的原理解释步骤⑤中加乳酸能得到乳酸亚铁的原因
(5)步骤④的离子方程式为
(6)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及
(7)为测定步骤②中所得晶体中FeSO4·7H2O的质量分数,取晶体样品a g,溶于稀硫酸配成100.00 mL溶液,取出20.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1 KMnO4溶液20.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)
您最近一年使用:0次



