已知X转化为R和W分步进行:① ②
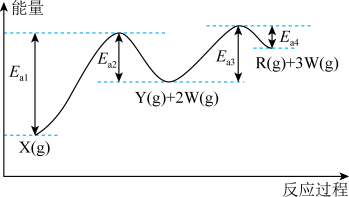
② 。述反应过程中的能量变化如图所示。下列说法正确的是
。述反应过程中的能量变化如图所示。下列说法正确的是
 ②
② 。述反应过程中的能量变化如图所示。下列说法正确的是
。述反应过程中的能量变化如图所示。下列说法正确的是
A.1mol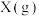 的能量低于1mol 的能量低于1mol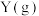 的能量 的能量 |
B.反应过程中,由于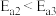 ,反应①的速率大于反应②的速率 ,反应①的速率大于反应②的速率 |
C.断裂1mol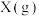 中的化学键吸收的能量小于形成1mol 中的化学键吸收的能量小于形成1mol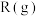 和3mol 和3mol 中的化学键所放出的能量 中的化学键所放出的能量 |
D.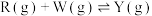 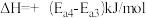 |
更新时间:2022-09-14 08:27:39
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】利用电导法测定某浓度醋酸电离的ΔH。Ka随温度变化曲线如图所示。已知整个电离过程包括氢键断裂、醋酸分子解离、离子水合。下列有关说法不正确的是
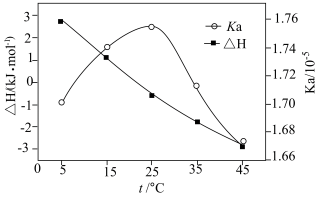

| A.理论上ΔH=0时,Ka最大 |
| B.25 ℃时,c(CH3COOH)最大 |
| C.电离的热效应较小是因为分子解离吸收的能量与离子水合放出的能量相当 |
| D.CH3COOH溶液中存在氢键是ΔH随温度升高而减小的主要原因 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某杂志曾报道过某课题组利用磁性纳米Fe3O4颗粒除去水体中草甘膦污染物的方法,其原理如图所示(Fe3O4颗粒在水中表面会带-OH)。下列说法不正确的是


| A.草甘膦能与氢氧化钠溶液反应 |
| B.Fe3O4纳米颗粒除去草甘膦的过程有化学键的形成和断裂 |
| C.溶液中c(H+)越大,Fe3O4纳米颗粒除污效果越好 |
| D.处理完成后,Fe3O4纳米颗粒可用磁铁回收,经加热活化重复使用 |
您最近一年使用:0次
【推荐1】在一定条件下,N2(g)和O2(g)反应生成NO(g)的能量变化如图所示,总反应的焙变△H>0。下列说法正确的是
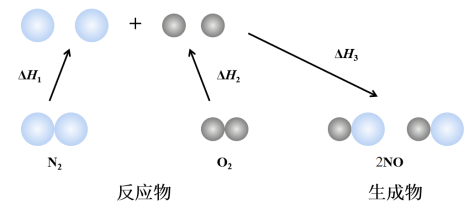

| A.△H1<△H2 | B.△H1<0,△H3>0 |
| C.│△H1+△H2│>│△H3│ | D.△H=△H1+△H2-△H3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】氯、溴、碘及其化合物在自然界广泛存在且具有重要应用。氯、溴主要存在于海水中,工业常通过电解 饱和溶液制备
饱和溶液制备 ,
, 可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为
可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为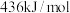 、
、 、
、 )。卤水中
)。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收,
溶液吸收, 能发生水解反应。锂碘电池可供电心脏起搏器,一种
能发生水解反应。锂碘电池可供电心脏起搏器,一种 二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
 饱和溶液制备
饱和溶液制备 ,
, 可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为
可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为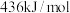 、
、 、
、 )。卤水中
)。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收,
溶液吸收, 能发生水解反应。锂碘电池可供电心脏起搏器,一种
能发生水解反应。锂碘电池可供电心脏起搏器,一种 二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
A. 用 用 溶液吸收: 溶液吸收: |
B. 电池正极放电时的电极反应有: 电池正极放电时的电极反应有: |
C. 与 与 反应: 反应: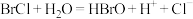 |
D.氯气制氯化氢: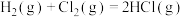  |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】利用下列两个反应可实现资源综合利用
已知:Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
Ⅱ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH2=-165.0kJ·mol-1
在一定的温度和压力下,将按一定比例混合的CO2和H2混合气体通过装有催化剂的反应器,反应相同时间,CO2转化率和CH4选择性随温度变化关系如图所示。 ×100%,下列说法正确的是
×100%,下列说法正确的是
已知:Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
Ⅱ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH2=-165.0kJ·mol-1
在一定的温度和压力下,将按一定比例混合的CO2和H2混合气体通过装有催化剂的反应器,反应相同时间,CO2转化率和CH4选择性随温度变化关系如图所示。
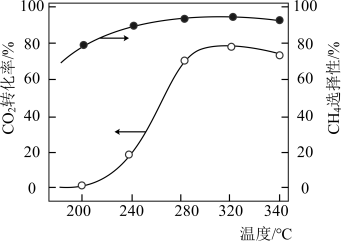
 ×100%,下列说法正确的是
×100%,下列说法正确的是| A.反应Ⅰ:2E(C=O)+E(H-H)<E(C-O)+2E(H-O)(E表示键能) |
| B.240℃时,其他条件不变,增大压强将减小CO2的转化率 |
| C.在260~300℃间,其他条件不变,升高温度CH4的产率增大 |
| D.320℃时CO2的转化率最大,说明反应Ⅰ和反应Ⅱ一定都达到了平衡状态 |
您最近一年使用:0次




