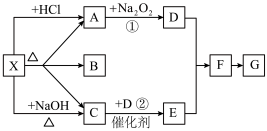
如图的各方框表示一种反应物或生成物(某些物质已经略去),已知化合物X只由非金属元素组成,常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。
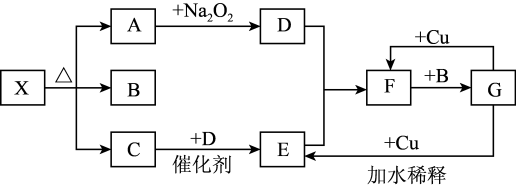
(1)写出物质X的化学式(写一种即可)_______ ;X属于_______ (离子或共价)化合物。
(2)写出C+D→E的化学方程式_______ ;写出G→F的离子方程式_______ ;
(3)F+B→G的反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)实验室里,常用加热固体混合物的方法制取气体C,写出化学方程式_______ 。
(5)实验室中,检验X中阳离子的操作方法是_______ 。

(1)写出物质X的化学式(写一种即可)
(2)写出C+D→E的化学方程式
(3)F+B→G的反应中氧化剂与还原剂的物质的量之比为
(4)实验室里,常用加热固体混合物的方法制取气体C,写出化学方程式
(5)实验室中,检验X中阳离子的操作方法是
更新时间:2022/08/21 10:23:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】在稀硫酸 、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、生石灰、铁片和木炭粉9种物质间存在如图所示关系,给①~⑤选择适当的物质,使有连线的两种物质之间能发生反应。
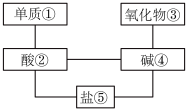
(1)它们的化学式分别为①_______ ③_______ ④_______ ⑤_______ 。
(2)写出下列物质之间反应的化学方程式:
①和②_______ 。
②和④_______ 。
②和⑤_______ 。
④和⑤_______ 。

(1)它们的化学式分别为①
(2)写出下列物质之间反应的化学方程式:
①和②
②和④
②和⑤
④和⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
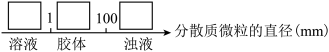
【推荐2】几种中学化学常见的单质及其化合物相互转化的关系图如下:
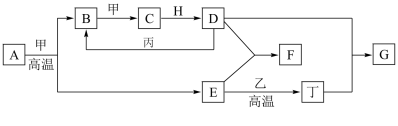
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
②A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为___________ ,每反应lmol的A转移的电子数为_____________ mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式:______________________ ;
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
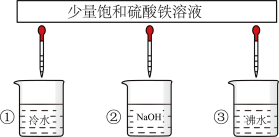
试将①、②、③对应的分散质具体的化学式填人下列方框中:________________
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:________________

可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
②A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式:
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。

试将①、②、③对应的分散质具体的化学式填人下列方框中:

(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】根据下图所示的A、B、C、D、E 五种物质的相互转化关系,按如下关系填写相应的物质和有关反应的化学方程式:
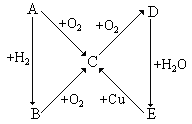
(1)当A是气体单质时,B是_________ ,C是____________ ,E是______________ ,由D 生成E的反应的化学方程式是__________________ 。
(2)当A是固体单质时,A是_________ ,B是____________ ,D是______________ ,由E 生成C的反应的化学方程式是__________________ 。

(1)当A是气体单质时,B是
(2)当A是固体单质时,A是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氨基甲酸铵是一种重要化工产品,常温时为白色晶体或粉末,易溶于水,难溶于CCl4,59℃时分解为氨及二氧化碳,其制备原理:2NH3(g)+CO2(g) NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:
NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:

(1)仪器组装完毕后,首先应进行的操作是_______ 。仪器b的名称是_______ 。
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为_______ 。
(3)装置F中试剂的名称为_______ 。
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为_______ ,装置D采用冰水浴的原因为_______ 。
(5)生成的氨基甲酸铵悬浮于CCl4中,下列操作可实现产品分离的是_______ 。(填字母)
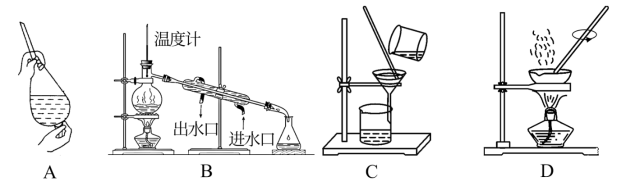
(6)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种杂质。
设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
 NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:
NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:
(1)仪器组装完毕后,首先应进行的操作是
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为
(3)装置F中试剂的名称为
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为
(5)生成的氨基甲酸铵悬浮于CCl4中,下列操作可实现产品分离的是

(6)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种杂质。
设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中, 加入蒸馏水至固体溶解。 | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,证明固体中不含碳酸铵 |
| 步骤3:向试管中继续加入 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室欲利用下图装置探究 还原CuO。
还原CuO。 与
与 制备
制备 的反应方程式为
的反应方程式为___________ ,下列方法还可以制备 的有
的有___________ (填字母)。
a.加热 b.加热浓氨水 c.向生石灰中滴加浓氨水
b.加热浓氨水 c.向生石灰中滴加浓氨水
(2)装置的连接顺序为a→___________ →de
(3)在检查装置气密性后,应先点燃装置___________ (填“A”或“B”)的酒精灯,其目的是___________ 。
(4)证明 能还原CuO的现象为装置B中黑色粉末变为红色,装置E中白色固体变为蓝色。反应还产生一种无污染气体,请写出反应方程式
能还原CuO的现象为装置B中黑色粉末变为红色,装置E中白色固体变为蓝色。反应还产生一种无污染气体,请写出反应方程式___________ 。
(5)装置C的作用是___________ 。
 还原CuO。
还原CuO。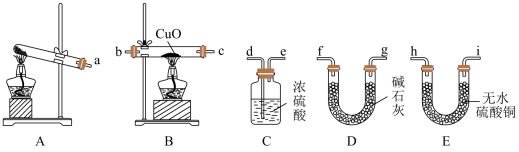
 与
与 制备
制备 的反应方程式为
的反应方程式为 的有
的有a.加热
 b.加热浓氨水 c.向生石灰中滴加浓氨水
b.加热浓氨水 c.向生石灰中滴加浓氨水(2)装置的连接顺序为a→
(3)在检查装置气密性后,应先点燃装置
(4)证明
 能还原CuO的现象为装置B中黑色粉末变为红色,装置E中白色固体变为蓝色。反应还产生一种无污染气体,请写出反应方程式
能还原CuO的现象为装置B中黑色粉末变为红色,装置E中白色固体变为蓝色。反应还产生一种无污染气体,请写出反应方程式(5)装置C的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示A、B、C、D、E五种含氮物质相互转化的关系。其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式。
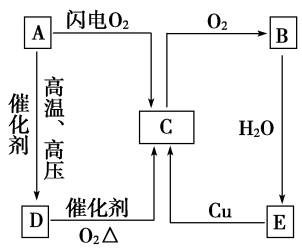
(1)除去C中的B所用的试剂为_______
(2)写出A的电子式_______
(3)检验试管中盛装的是D的方法为_______
(4)E→C的离子方程式_______
(5)写出实验式制备D的化学方程式_______

(1)除去C中的B所用的试剂为
(2)写出A的电子式
(3)检验试管中盛装的是D的方法为
(4)E→C的离子方程式
(5)写出实验式制备D的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】中学化学常见物质A、B、C、D、X、Y,存在如下图转化关系(部分物质和条件略去)
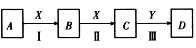
(1)若A为NaOH溶液,X为CO2,D是沉淀,则Y可为________ (填序号)。
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
(2)若A为黄铁矿(FeS2),D是H2SO4,则反应Ⅱ的化学方程式为_________________________ 。
(3)若A为溶于水呈碱性的气体,则A与D反应生成的一种化肥的化学式为_____________ ,反应Ⅰ的化学方程式为__________________ ,D的浓溶液与炭反应的化学方程式__________________________ 。
(4)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,则反应II的离子方程式为_____________________ 。

(1)若A为NaOH溶液,X为CO2,D是沉淀,则Y可为
A.SO3 B.Ba(OH)2 C.H2SO4 D.CaO
(2)若A为黄铁矿(FeS2),D是H2SO4,则反应Ⅱ的化学方程式为
(3)若A为溶于水呈碱性的气体,则A与D反应生成的一种化肥的化学式为
(4)若A和X均为单质,反应Ⅲ的现象是白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,则反应II的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】研究金属与硝酸的反应,实验如下。
(1)I中的无色气体是_________ 。
(2)II中生成H2的离子方程式是_________ 。
(3)研究II中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于 ,所以
,所以 没有发生反应。乙同学依据I和II证明了甲的说法不正确,其实验证据是
没有发生反应。乙同学依据I和II证明了甲的说法不正确,其实验证据是________ 。
②乙同学通过分析,推测出 也能被还原,依据是
也能被还原,依据是__________ ,进而他通过实验证实该溶液中含有 ,其实验操作是
,其实验操作是__________ 。
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有_______ 。
| 实验(20℃) | 现象 |
| I.过量铜粉、2mL0.5mol/LHNO3 | 无色气体(遇空气变红棕色),溶液变为蓝色 |
| II.过量铁粉、2mL0.5mol/LHNO3 | 6mL无色气体(经检测为H2),溶液几乎无色 |
(2)II中生成H2的离子方程式是
(3)研究II中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于
 ,所以
,所以 没有发生反应。乙同学依据I和II证明了甲的说法不正确,其实验证据是
没有发生反应。乙同学依据I和II证明了甲的说法不正确,其实验证据是②乙同学通过分析,推测出
 也能被还原,依据是
也能被还原,依据是 ,其实验操作是
,其实验操作是(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有
您最近一年使用:0次
【推荐1】铅蓄电池是最常见的二次电池,以废旧铅蓄电池中的铅膏(主要含PbO、PbO2、PbSO4等)为原料回收铅,对保护环境和发展循环经济意义重大。某工艺流程如下:
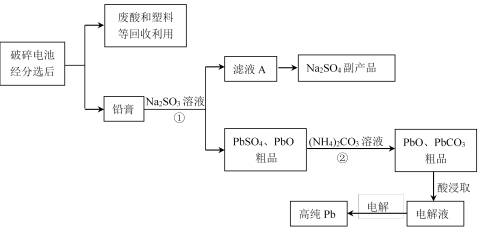
(1)已知铅蓄电池总反应:Pb+PbO2+2H2SO4 2PbSO4+2H2O,充电时,阳极的电极反应式为
2PbSO4+2H2O,充电时,阳极的电极反应式为________ 。
(2)过程①体现Na2SO3的_________ 性。
(3)由滤液A可获得Na2SO4·10H2O粗品,检验粗品中SO42-离子的实验方法是________ 。
(4)结合化学用语解释过程②中PbSO4转化为PbCO3的原因________ 。
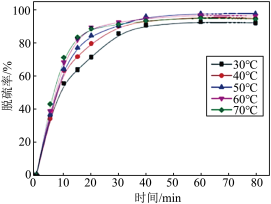
(5)反应温度对过程②转化率(脱硫率)的影响如图所示,实际生产中温度选择在50℃,若温度过高,脱硫率下降的原因可能是:________ 。
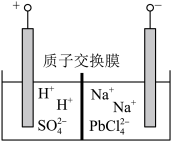
(6)将PbO 、PbCO3粗品置于一定浓度HCl和NaCl浸取液中溶解,得到含Na2PbCl4的电解液,如图电解可得高纯Pb,同时再生浸取液。请结合化学用语解释浸取液再生的原理________ 。

(1)已知铅蓄电池总反应:Pb+PbO2+2H2SO4
 2PbSO4+2H2O,充电时,阳极的电极反应式为
2PbSO4+2H2O,充电时,阳极的电极反应式为(2)过程①体现Na2SO3的
(3)由滤液A可获得Na2SO4·10H2O粗品,检验粗品中SO42-离子的实验方法是
(4)结合化学用语解释过程②中PbSO4转化为PbCO3的原因
(5)反应温度对过程②转化率(脱硫率)的影响如图所示,实际生产中温度选择在50℃,若温度过高,脱硫率下降的原因可能是:

(6)将PbO 、PbCO3粗品置于一定浓度HCl和NaCl浸取液中溶解,得到含Na2PbCl4的电解液,如图电解可得高纯Pb,同时再生浸取液。请结合化学用语解释浸取液再生的原理

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
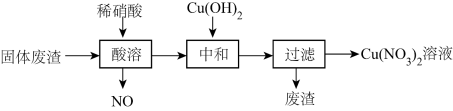
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知:①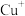 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。
② 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。
(1)写出 与稀硝酸反应的离子反应方程式为
与稀硝酸反应的离子反应方程式为___________ ;
(2)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是___________ ;
(3)酸溶试剂改用绿色氧化剂(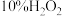 和
和 稀硝酸的混合液),基本无氮氧化物排放,写出废渣中
稀硝酸的混合液),基本无氮氧化物排放,写出废渣中 与绿色氧化剂反应的离子反应方程式
与绿色氧化剂反应的离子反应方程式___________ ;
(4)中和试剂选择 ,若改为
,若改为 ,缺点是
,缺点是___________ 。
 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知:①
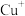 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。②
 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。(1)写出
 与稀硝酸反应的离子反应方程式为
与稀硝酸反应的离子反应方程式为(2)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(3)酸溶试剂改用绿色氧化剂(
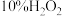 和
和 稀硝酸的混合液),基本无氮氧化物排放,写出废渣中
稀硝酸的混合液),基本无氮氧化物排放,写出废渣中 与绿色氧化剂反应的离子反应方程式
与绿色氧化剂反应的离子反应方程式(4)中和试剂选择
 ,若改为
,若改为 ,缺点是
,缺点是
您最近一年使用:0次