Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子化学性质相对稳定的是_______ (填离子符号),解释原因_______ 。
(2)浓磷酸在常温下呈粘稠状,原因_______ ,浓磷酸在200~ 300°C时脱水生成焦磷酸(化学式: H4P2O7),焦磷酸的结构式为_______ ,其中P的价层电子对数为_______ ,杂化轨道类型为_______ 。
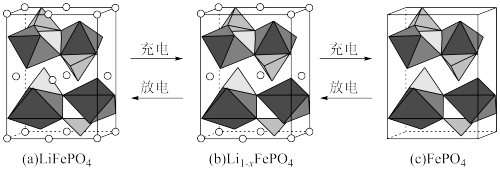
(3)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。图(a)晶胞参数单位为pm,NA表示阿伏加德罗常数数值,其密度为_______ g·cm-3。电池充电时,LiFePO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=_______ ,n(Fe2+):n(Fe3+)=_______ 。
(1)基态Fe2+与Fe3+离子化学性质相对稳定的是
(2)浓磷酸在常温下呈粘稠状,原因
(3)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。图(a)晶胞参数单位为pm,NA表示阿伏加德罗常数数值,其密度为

更新时间:2022-08-18 15:06:02
|
相似题推荐
【推荐1】盐酸氯丙嗪是一种多巴胺受体的阻断剂,临床有多种用途。化合物Ⅲ是盐酸氯丙嗪制备的原料,可由化合物I和Ⅱ在铜作催化剂条件下反应制得。

(1) Cu基态核外电子排布式为________________ 。
(2) 1 mol化合物Ⅰ分子中含有σ键数目为________ 。
(3) 化合物Ⅲ分子中sp3方式杂化的原子数目是____________ 。
(4) 向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该白色沉淀中Cu、S、N的物质的量之比为1∶1∶1,沉淀中有一种三角锥形的阴离子和一种正四面体形的阳离子。
①[Cu(NH3)4]SO4中存在的化学键类型有________ (填字母)。
A. 共价键 B. 氢键 C. 离子键 D. 配位键 E. 分子间作用力
② 上述白色沉淀的化学式为____________________________ 。
(5) 铜的氢化物的晶体结构如图所示,写出此氢化物在氯气中燃烧的化学方程式:__________________________________________________________ 。


(1) Cu基态核外电子排布式为
(2) 1 mol化合物Ⅰ分子中含有σ键数目为
(3) 化合物Ⅲ分子中sp3方式杂化的原子数目是
(4) 向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该白色沉淀中Cu、S、N的物质的量之比为1∶1∶1,沉淀中有一种三角锥形的阴离子和一种正四面体形的阳离子。
①[Cu(NH3)4]SO4中存在的化学键类型有
A. 共价键 B. 氢键 C. 离子键 D. 配位键 E. 分子间作用力
② 上述白色沉淀的化学式为
(5) 铜的氢化物的晶体结构如图所示,写出此氢化物在氯气中燃烧的化学方程式:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答问题
(1)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电子数与Al相同的有_______ 。
(2)亚铁氰化钾(K4[Fe(CN)6])中的作用力除共价键外,还有_______ 和_______ 。
(3)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有_______ 种不同运动状态的电子。
②Li、Be、B元素的第一电离能由大到小排列顺序为____ ,电负性由大到小的顺序是_____ 。
③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_______ (填元素符号)。
(1)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电子数与Al相同的有
(2)亚铁氰化钾(K4[Fe(CN)6])中的作用力除共价键外,还有
(3)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有
②Li、Be、B元素的第一电离能由大到小排列顺序为
③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 |
| 580 | 1820 | 2750 | 11600 |
M是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】KMnO4是一种高效氧化剂,可用来氧化吸附有机异味物,也可以与水中的杂质如二价铁、锰、硫、氰、酚等反应。实验室常用Na2C2O4标准溶液标定未知浓度的KMnO4溶液,发生反应:5C2O +2MnO
+2MnO +16H++4H2O=2[Mn(H2O)6]2++10CO2↑。根据以上信息,完成下列问题:
+16H++4H2O=2[Mn(H2O)6]2++10CO2↑。根据以上信息,完成下列问题:
(1)基态Mn2+的核外电子排布式可表示为___________ ,上述反应方程式中的各原子的电负性由大到小的关系是___________ 。
(2)1mol[Mn(H2O)6]2+中所含有的共价键数目为___________ 。
(3)CO2的电子式是___________ ,C2O 中碳原子的轨道杂化类型是
中碳原子的轨道杂化类型是___________ 。
(4)同主族元素氧、硫、硒对应最简单氢化物的沸点由高到低顺序是___________ ,原因是___________ 。
(5)β—MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。
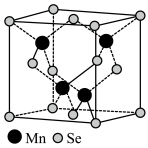
①β—MnSe中Mn的配位数为___________ 。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为___________ pm。
 +2MnO
+2MnO +16H++4H2O=2[Mn(H2O)6]2++10CO2↑。根据以上信息,完成下列问题:
+16H++4H2O=2[Mn(H2O)6]2++10CO2↑。根据以上信息,完成下列问题:(1)基态Mn2+的核外电子排布式可表示为
(2)1mol[Mn(H2O)6]2+中所含有的共价键数目为
(3)CO2的电子式是
 中碳原子的轨道杂化类型是
中碳原子的轨道杂化类型是(4)同主族元素氧、硫、硒对应最简单氢化物的沸点由高到低顺序是
(5)β—MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。

①β—MnSe中Mn的配位数为
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】金属催化剂在生产生活中有着广泛的用途
(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用•标注。

可知水煤气变换的
___________ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)
___________  ,写出该步骤的化学方程式
,写出该步骤的化学方程式___________ 。
(2) 加氢制水煤气
加氢制水煤气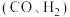 时发生下列反应:
时发生下列反应:
已知:①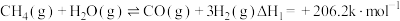
②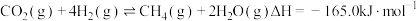
则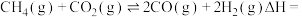
___________  。
。
(3)我国科学家发现催化剂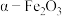 可高效活化
可高效活化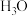 ,实现物质的高选择性氧化,为污染物的去除提供了新策略。污染物X去除的催化反应过程示意图如下。
,实现物质的高选择性氧化,为污染物的去除提供了新策略。污染物X去除的催化反应过程示意图如下。

①基态 原子的价层电子排布式是
原子的价层电子排布式是___________ 。
②污染物 在电极
在电极 上的反应式是
上的反应式是___________ 。
(4)科研团队研究了 分别为
分别为 和
和 [也可以写作
[也可以写作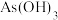 ]的反应能力,发现中心原子含有孤电子对的物质易被氧化。
]的反应能力,发现中心原子含有孤电子对的物质易被氧化。
① 中的键角
中的键角___________ (填“>”“<”或“=”) 中的键角,理由为
中的键角,理由为___________ 。
②比较反应能力:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
(5)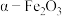 晶胞的体积为
晶胞的体积为 ,晶体密度为
,晶体密度为 阿伏加德罗常数的值为
阿伏加德罗常数的值为 ,一个晶胞中
,一个晶胞中 原子的个数为
原子的个数为___________ ( 的摩尔质量:
的摩尔质量: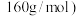 。
。
(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用•标注。

可知水煤气变换的


 ,写出该步骤的化学方程式
,写出该步骤的化学方程式(2)
 加氢制水煤气
加氢制水煤气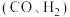 时发生下列反应:
时发生下列反应:已知:①
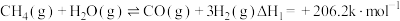
②
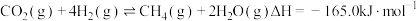
则
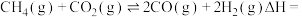
 。
。(3)我国科学家发现催化剂
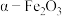 可高效活化
可高效活化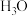 ,实现物质的高选择性氧化,为污染物的去除提供了新策略。污染物X去除的催化反应过程示意图如下。
,实现物质的高选择性氧化,为污染物的去除提供了新策略。污染物X去除的催化反应过程示意图如下。
①基态
 原子的价层电子排布式是
原子的价层电子排布式是②污染物
 在电极
在电极 上的反应式是
上的反应式是(4)科研团队研究了
 分别为
分别为 和
和 [也可以写作
[也可以写作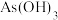 ]的反应能力,发现中心原子含有孤电子对的物质易被氧化。
]的反应能力,发现中心原子含有孤电子对的物质易被氧化。①
 中的键角
中的键角 中的键角,理由为
中的键角,理由为②比较反应能力:

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(5)
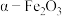 晶胞的体积为
晶胞的体积为 ,晶体密度为
,晶体密度为 阿伏加德罗常数的值为
阿伏加德罗常数的值为 ,一个晶胞中
,一个晶胞中 原子的个数为
原子的个数为 的摩尔质量:
的摩尔质量: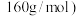 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】短周期元素X、Y的价电子数相同,且原子序数之比等于1∶2;元素Z是人体必需的微量元素,位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)与X同周期且第一电离能比X大的元素有_____ 种。
(2)基态Y原子中,能量最高的核外电子占据的能级的电子云轮廓图形状为____ 。
(3)X与Y可形成多种微粒,其中微粒的立体构型为正四面体形的是____ (写化学式),写出两种与它互为等电子体的粒子的化学式_____ (写一种分子和一种离子)
(4)Y与Z形成的某种晶体的晶胞如图所示,该晶胞中Z微粒的配位数为_____ ,该化合物的化学式为_____ 。

(5)已知ZY晶体的熔点约为1700℃,ZX与ZY结构相似,其熔点为1975℃,构成ZY晶体的作用力是_____ ,ZX熔点较高的原因是_____ 。
(1)与X同周期且第一电离能比X大的元素有
(2)基态Y原子中,能量最高的核外电子占据的能级的电子云轮廓图形状为
(3)X与Y可形成多种微粒,其中微粒的立体构型为正四面体形的是
(4)Y与Z形成的某种晶体的晶胞如图所示,该晶胞中Z微粒的配位数为

(5)已知ZY晶体的熔点约为1700℃,ZX与ZY结构相似,其熔点为1975℃,构成ZY晶体的作用力是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】锰(Mn)、钴(Co)、镍(Ni)等过渡金属元素化合物的应用研究是前沿科学之一,回答下列问题:
(1) 的价电子排布式为
的价电子排布式为_______ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用“_______ 理论”解释。
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列_______ (填序号),Mn原子的配位数为_______ 。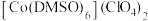 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为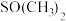 。DMSO中硫原子的杂化轨道类型为
。DMSO中硫原子的杂化轨道类型为_______ ,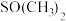 中键角
中键角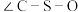
_______  中键角
中键角 (填“大于”“小于”或“等于”),
(填“大于”“小于”或“等于”), 的中心原子价层电子对数为
的中心原子价层电子对数为_______ ,元素S、Mn、N的电负性由大到小的顺序为_______ 。
(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(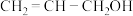 ),该物质与丙醛(
),该物质与丙醛(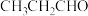 )相比,两者沸点相差较大,原因是
)相比,两者沸点相差较大,原因是_______ 。
(5) 的晶胞结构如图甲所示,其中离子坐标参数A为
的晶胞结构如图甲所示,其中离子坐标参数A为 ,B为
,B为 ,则C的离子坐标参数为
,则C的离子坐标参数为_______ 。一定温度下, 晶体可以自发地分散并形成“单分子层”,可以认为
晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为
的半径为 ,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为
,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为_______ g(用含a、NA的代数式表示)。
(1)
 的价电子排布式为
的价电子排布式为(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列
A.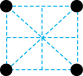 B.
B. C.
C.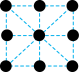 D.
D.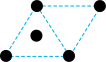
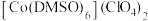 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为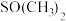 。DMSO中硫原子的杂化轨道类型为
。DMSO中硫原子的杂化轨道类型为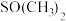 中键角
中键角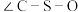
 中键角
中键角 (填“大于”“小于”或“等于”),
(填“大于”“小于”或“等于”), 的中心原子价层电子对数为
的中心原子价层电子对数为(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(
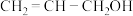 ),该物质与丙醛(
),该物质与丙醛(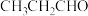 )相比,两者沸点相差较大,原因是
)相比,两者沸点相差较大,原因是(5)
 的晶胞结构如图甲所示,其中离子坐标参数A为
的晶胞结构如图甲所示,其中离子坐标参数A为 ,B为
,B为 ,则C的离子坐标参数为
,则C的离子坐标参数为 晶体可以自发地分散并形成“单分子层”,可以认为
晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为
的半径为 ,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为
,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为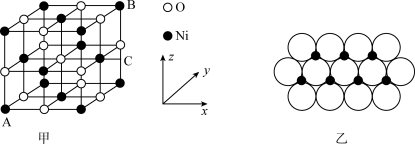
您最近一年使用:0次



